Clear Sky Science · ar
بنية مركب SHOC2-KRAS-PP1C تكشف محددات خاصة بأنواع RAS ورؤى حول استهداف تجميع المركب بواسطة مثبطات RAS
كيف تقرر الخلايا متى تنمو
تعتمد خلايانا على نظام داخلي لتحديد متى تنمو أو تنقسم أو تبقى خاملة. في قلب هذا النظام تقف بروتينات RAS، مفاتيح جزيئية صغيرة تنحرف غالبًا في السرطان. تدرس هذه الدراسة بعمق كيف تتجمع مجموعة معينة من البروتينات—SHOC2 وRAS وPP1C—معًا لقلب مفتاح نمو أساسي، وكيف يمكن ضبط أدوية السرطان الحديثة لعرقلة هذه العملية بشكل أكثر فعالية ومنع الأورام من التحايل على العلاج.
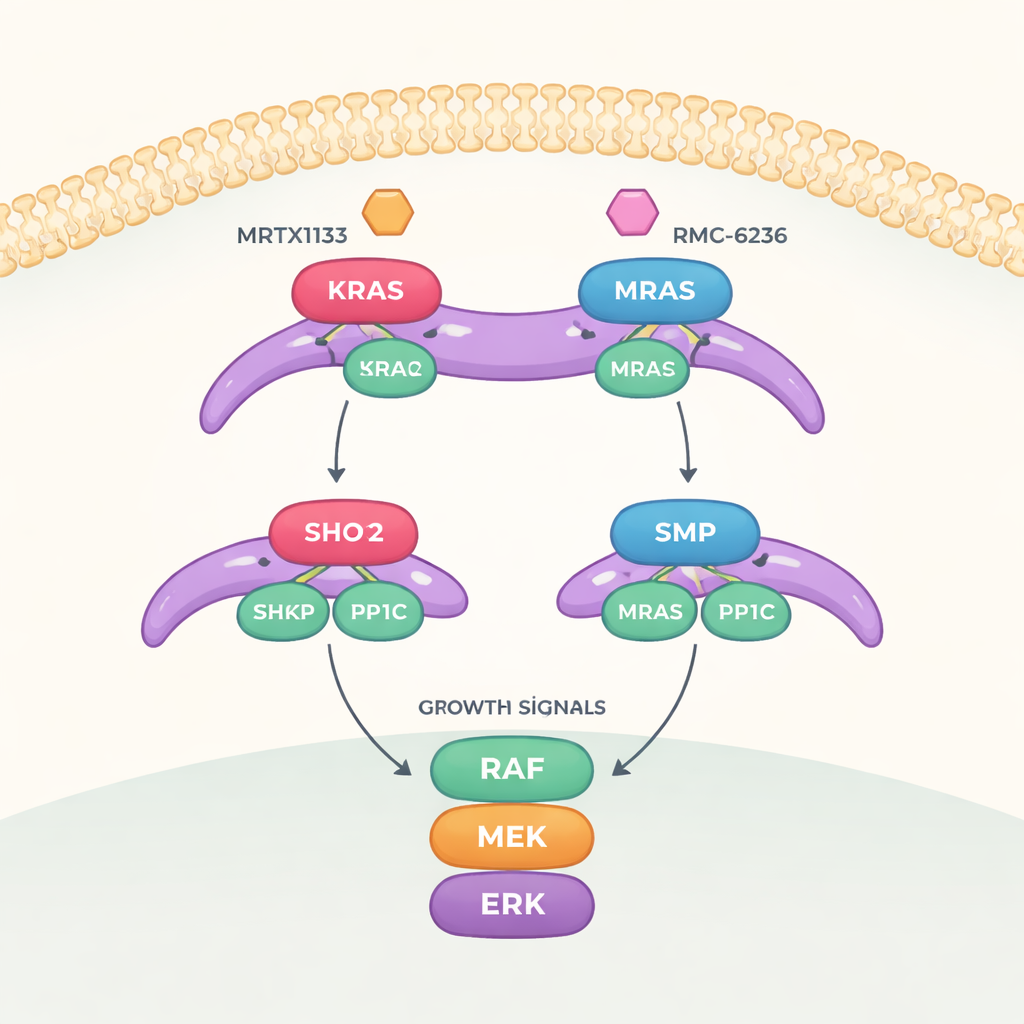
مفتاح نمو يتكوّن من ثلاثة أجزاء حاسمة
تركز الدراسة على مسار إشارة يسمى مسار MAPK، الذي ينقل رسائل النمو من سطح الخلية إلى النواة. لتشغيل هذا المسار بالكامل، يجب تحويل بروتين آخر اسمه RAF من حالة "مطفأة" إلى حالة "مفعّلة". يتحكم في هذا التحول مركب ثلاثي يتألف من SHOC2 (هيكل داعم يربط المكونات)، وPP1C (إنزيم يزيل علامة الفسفور)، وRAS النشط. عندما يتجمع هذا الثلاثي، يزيل علامة فسفرة محددة من RAF، ما يحرره لتفعيل سلسلة الإشارات التي تقود النمو.
لماذا يظل الشريك منخفض التقارب مهمًا في السرطان
هناك عدة أنواع من بروتينات RAS. يشكل MRAS مركبًا محكمًا جدًا مع SHOC2 وPP1C، بينما تشكل أنواع RAS الأكثر شهرة في السرطان—KRAS وHRAS وNRAS—نسخًا أضعف من نفس المركب. والمفاجئ أن الخلايا السرطانية التي تدفعها طفرات في KRAS أو HRAS أو NRAS تعتمد بشدة على SHOC2، رغم أن مركباتها أقل استقرارًا. تُظهر مجموعات بيانات فحص جيني واسعة أن العديد من الأورام ذات طفرات معينة في RAS—وخاصة تلك التي تؤثر على مواقع رئيسية مثل Q61 وG13—شديدة الحساسية لفقدان SHOC2، ما يعني أن هذا التجمع ضروري لبقائها.
كشف شكل مركب KRAS
حتى الآن، شاهد العلماء بنية عالية الدقة لمركب MRAS المحكم فقط. أما نسخة KRAS الأضعف فكانت تنهار بسهولة بالغة بحيث لا يمكن تصويرها. في هذه الدراسة، استخدم الباحثون طفرات مرتبطة بالمرض تُقوّي بشكل طفيف التماسّات بين المكونات لتثبيت مركب SHOC2–KRAS–PP1C لفترة كافية لتصويره بالمجهر الإلكتروني بالتبريد. وجدوا أن البنية العامة تشبه إلى حد كبير مركب MRAS، لكن KRAS يفتقر إلى عدة ميزات بنيوية صغيرة يستخدمها MRAS للإمساك بـSHOC2 وPP1C بقوة أكبر. نتيجة لذلك، يخفي مركب KRAS مساحة اتصال أقل ويكوّن روابط أقل، مما يفسر سبب كونه أقل استقرارًا بطبيعته، رغم أنه يظل مهمًا للغاية في الأورام التي يكون فيها KRAS مفرط النشاط.
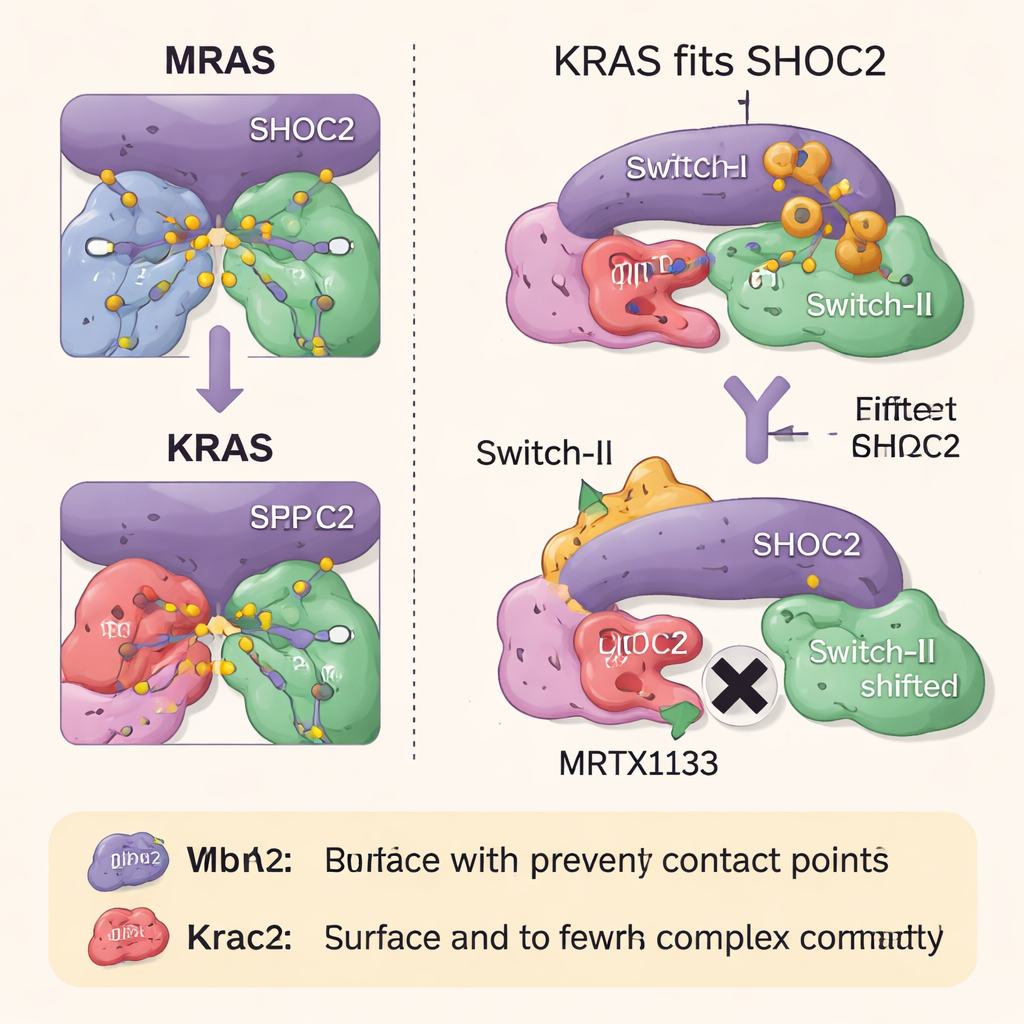
كيف تمنع عقاقير RAS تجميع المركب
استكشف الفريق بعد ذلك كيف تؤثر فئتان من الأدوية المستهدفة لـRAS على هذا المركب الثلاثي. يعمل MRTX1133، المصمم ليرتبط بمنفذ قرب منطقة مرنة من KRAS تُعرف باسم Switch-II، على قفل هذه المنطقة في شكل يتصادم مع سطح SHOC2. هذا يمنع بقوة تكوّن مركبات SHOC2–KRAS–PP1C جديدة، رغم أنه أقل فعالية في تفكيك المركبات الموجودة بالفعل. يعمل دواء ثانٍ، RMC-6236، بالتعاون مع بروتين مساعد (سيكلوفيلين A) ويمنع أيضًا نفس أسطح KRAS اللازمة لارتباط SHOC2. ومع ذلك، لا يرتبط أي من الدواءين بطبيعة الحال بـMRAS، لذا يبقى مركب MRAS عالي التقارب سليمًا ويمكنه المساعدة في إعادة تنشيط مسار النمو عندما يُثبط KRAS.
نحو استهداف مزدوج لمنع المقاومة
لاختبار إمكانية الاستهداف المزدوج، صنع الباحثون نسخة مهندسة من MRAS تم تعديل منفذ Switch-II فيها بحيث يمكن أن يرتبط بها MRTX1133 الآن. هذا الطفر المُهندس ظل يشكل مركبًا قويًا مع SHOC2 وPP1C، لكن الدواء أصبح الآن يمنع تجميعه ويقلل قدرته على تفعيل RAF في تجارب أنبوبية. إلى جانب بيانات عن مركبات ترتبط بـSHOC2، تظهر هذه النتائج أن من الواقعي تصميم أدوية تغلق كلًا من مركبات KRAS وMRAS. للقراء غير المتخصصين، الرسالة الأساسية هي أن الخلايا السرطانية تستخدم مفاتيح متعددة ومتقاربة للحفاظ على تدفق إشارات النمو، خصوصًا عندما يُستهدف أحد المفاتيح بدواء. من خلال فهم الأشكال والاتصالات الدقيقة داخل هذه التجمعات البروتينية، يمكن للباحثين الآن التخطيط لعلاجات تضرب كلا المسارين الاحتياطيين معًا، مما يصعّب على السرطانات المدفوعة بـRAS التكيف وتطوير المقاومة للعلاج.
الاستشهاد: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
الكلمات المفتاحية: إشارات RAS, مثبطات KRAS, مسار MAPK, مجموعات البروتين, مقاومة الأدوية