Clear Sky Science · ar
آلية مقاومة SARS-CoV-2 للأدوية المضادة للفيروسات المعتمدة على نظائر النيوكليوتيد
كيف يتفوق الفيروس على أدوية مضادة رئيسية
ينتمي فيروس كوفيد-19 إلى مجموعة نادرة من فيروسات الـRNA القادرة على تدقيق مادتها الجينية، مما يجعله جيدًا بشكل غير معتاد في مقاومة بعض أفضل أدوية مضادات الفيروسات لدينا. تتعمق هذه الدراسة في التفاصيل على المستوى الذري لكيفية اكتشاف SARS‑CoV‑2 وإزالة فئة مستخدمة على نطاق واسع من الأدوية تُسمى نظائر النيوكليوتيد، موضحة لماذا الأدوية الفعّالة ضد فيروسات أخرى غالبًا ما تؤدي أداءً أقل أمام عدوى الفيروسات التاجية.
شِد وجذب على حمض الفيروس الريبي
ينسخ SARS‑CoV‑2 جينومه الـRNA الذي يتكون من نحو 30,000 حرف باستخدام آلة جزيئية كبيرة تسمى مركب النسخ–التكرار. في مركزها يوجد بوليمراز RNA المعتمد على RNA (RdRp) الذي يبني سلاسل RNA جديدة، ووحدة منفصلة، الإكسونوكلياز (ExoN)، التي تقوم بتدقيق وقطع الأخطاء. العديد من أقراص مضادات الفيروسات، بما في ذلك أدوية طورت أصلاً لالتهاب الكبد الوبائي C، تحاكي لبنات بناء الحمض النووي الريبي الطبيعية بما يكفي ليقوم RdRp بإدخالها، لكن مع تغييرات طفيفة تتسبب في توقف النسخ أو إدخال أخطاء. للأسف، تمتلك الفيروسات التاجية ExoN، الذي يمكنه التعرف على هذه المحاكيات بمجرد وجودها في سلسلة RNA وقطعها للخارج، مما ينقذ عملية تكرار الفيروس.
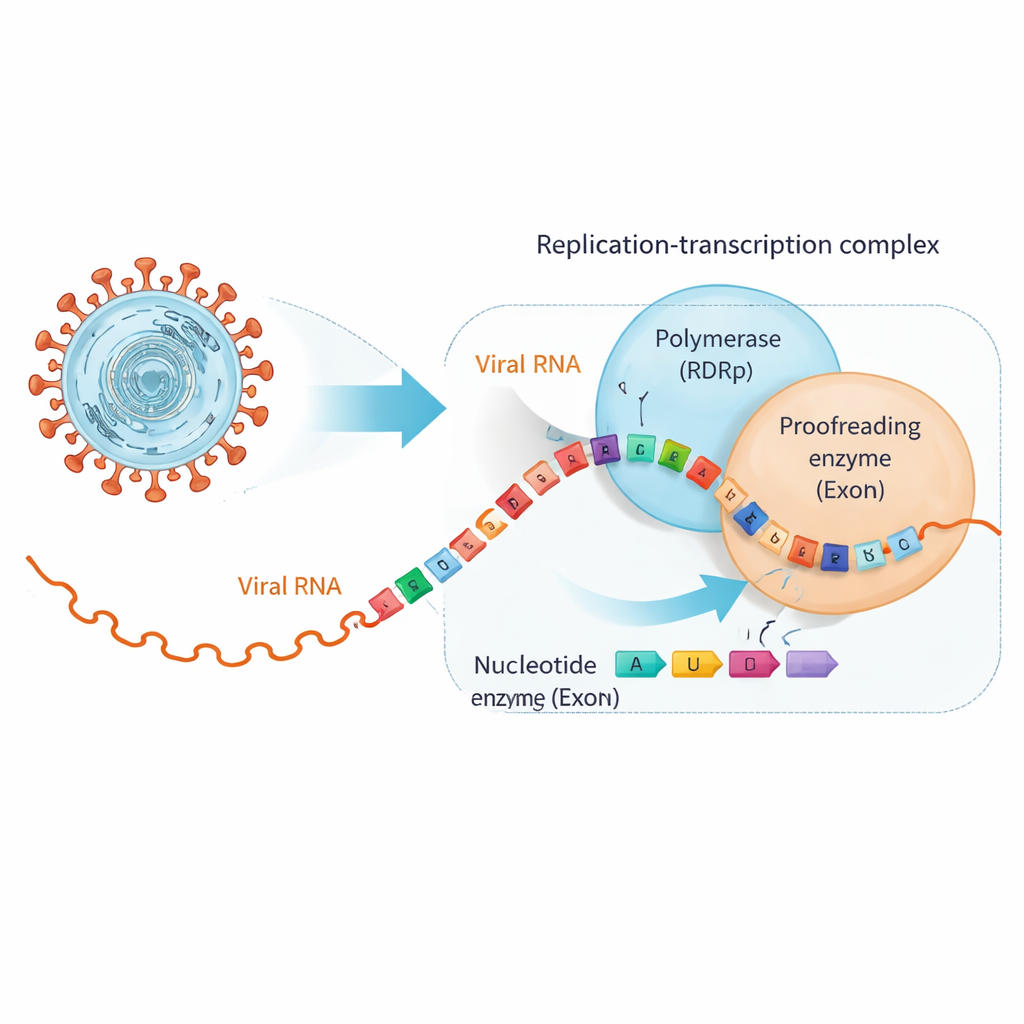
عندما تدفع الأدوية المفيدة الحمض الريبي لتغيير الشريك
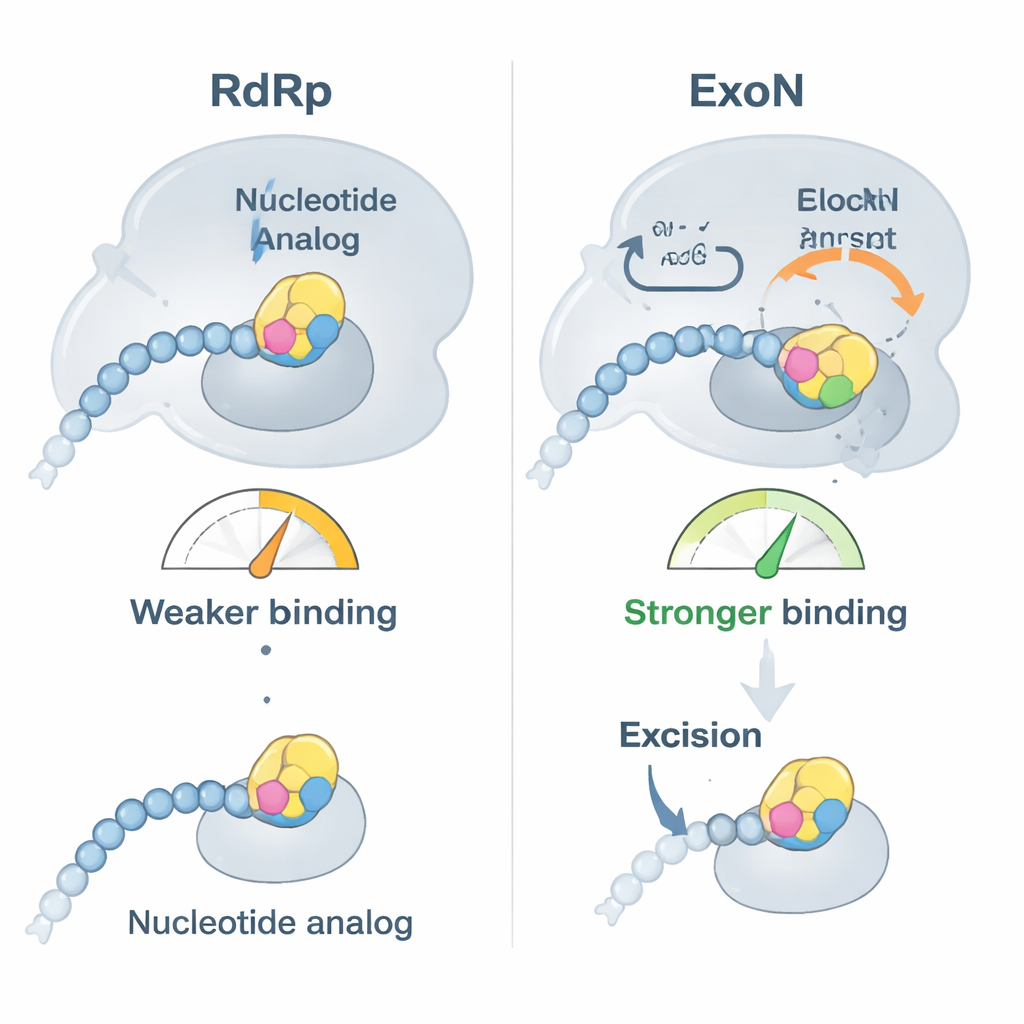
ركز الباحثون على دوائين مضادين للفيروسات مهمين سريريًا، بيمنيفوسبوڤير وسوفوسبوڤير، كلاهما مصممان للعمل كبِنَىِ بناء RNA معطوبة. أظهروا أولًا أن بوليمراز SARS‑CoV‑2 يُدخل هذه النظائر بسهولة في نهاية شريط RNA ثم يتوقف إلى حد كبير عن تمديد السلسلة، كما هو المقصود. ومع ذلك، كشفت اختبارات الارتباط عن مفاجأة: بمجرد أن تجلس النظير على طرف الـRNA، لم يعد الـRNA مرتبطًا بقوة مع البوليمراز بل أصبح يرتبط بإحكام أكبر مع ExoN. فعليًا، يتم دفع الـRNA المعدل بالدواء بعيدًا عن آلة النسخ وتسليمه إلى المدقِّق، الذي يحصل عندها على فرصة لاقتطاع النيوكليوتيد المشكل والسماح باستمرار التكرار.
تصحيح أخطاء يتباطأ لكنه لا يتوقف
أظهرت تجارب المسار الزمني الكيميائي الحيوي أن ExoN يزيل بيمنيفوسبوڤير وسوفوسبوڤير من الـRNA، لكن ببطء أكثر مما يزيل النيوكليوتيدات الطبيعية. في تفاعلات خالية من الخلايا، أعاق كلا النظيرين بشدة مزيد نسخ الـRNA—ومع ذلك، عندما تمت إضافة ExoN فعال، تم إنقاذ جزء كبير من سلاسل الـRNA المتوقفة وتمت مدّها. لم يكن الطفرة المعطلة في ExoN قادرة على القيام بذلك، مما يؤكد أن نشاط التدقيق هو المسؤول عن التراجع عن جزء كبير من تأثير الأدوية. وجود البوليمراز جنبًا إلى جنب مع ExoN سرّع فعليًا إزالة النظائر، مما يشير إلى أن الإنزيمين الفيروسيَّين يعملا معًا لإزالة العقبات والحفاظ على استمرار التكرار.
مراقبة المدقِّق بدقة ذرية
لفهم كيف يتعرف ExoN على هذه الأدوية ويستجيب لها، استخدم الفريق مجهر إلكتروني مجمّد عالي الدقة لحل تراكيب مركب ExoN المرتبطة بسلاسل RNA المنتهية إما ببِمنيفوسبوڤير أو بسوفوسبوڤير. كشفت هذه التراكيب، الواضحة بما يكفي لرؤية مجموعات كيميائية فردية، أن الحَلَق السكرية المعدلة في كل دواء تلائم جيبًا هيدروفوبيًا يتكوَّن من حلقة قصيرة لبروتين ExoN. يشرح هذا الثبات الأكبر لارتباط الـRNA المحتوي على الدواء بـExoN. لكنه أيضًا له تأثير جانبي غير متوقع: عبر سحبه لتلك الحلقة، تُزعزع الأدوية الترتيب الدقيق لحلقة تحفيزية مجاورة التي تُثبّت بقايا هستيدين مهمة في موضعها. عندما يتأرجح هذا الهستيدين بعيدًا عن موقع القطع، يصبح المركز النشط لـExoN معطلاً جزئيًا، مما يبطئ لكن لا يمنع بالكامل اقتطاع النظير.
مفتاح مدمج يعدِّل تدقيق الفيروس
أكد تغيير أحماض أمينية مفردة داخل الحلقة الحساسة أهميتها. أدت تغييرات في أربع بقايا محفوظة إلى تقليل كبير في قدرة ExoN على قطع نهايات الـRNA العادية ونهايات الـRNA المنتهية بالدواء، كما غيرت أي النيوكليوتيد النهائي الذي يفضّل ExoN إزالته. هذا يُحدد الحلقة كمُنظّم كلوسيري—مفتاح ميكانيكي مدمج يستشعر نوع النيوكليوتيد الموجود على طرف الـRNA ويعدّل نشاط الإنزيم وفقًا لذلك. تُظهر التراكيب أيضًا أن ExoN يتعرف على قواعد مختلفة (A، U، C، أو G) عبر ارتباطات هيدروجينية مرنة، لكنه يواجه أصعبية في استيعاب القواعد الشبيهة بالغوانين، وهو أمر ذو صلة لأن بيمنيفوسبوڤير يُحاكي الجوانين.
ماذا يعني هذا لأقراص كوفيد‑19 المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن SARS‑CoV‑2 يحمل "مدقِّق هجائي" متطورًا يمكنه اقتلاع بعض الأدوية من جينومه بعد أن تؤدي دورها في إيقاف التكرار. تضعف بيمنيفوسبوڤير وسوفوسبوڤير آلة النسخ لدى الفيروس، لكن في الوقت نفسه توجهان الـRNA نحو المدقِّق الذي يمكنه التراجع جزئيًا عن آثارهما. من خلال الكشف بالضبط عن كيفية امساك المدقِّق الفيروسي بهذه الأدوية، وكيف يقوم مفتاح تنظيمي صغير بتبديل الإنزيم بين حالات نشطة وأقل نشاطًا، تقدم هذه الدراسة خارطة طريق لتصميم نيوكليوتيدات مضادة للفيروسات جديدة إما ترتبط ضعيفًا بـExoN، أو تُقفلها في حالة غير نشطة، أو تستغل صعوبة ExoN في التعامل مع هياكل شبيهة بالغوانين. قد تكون مثل هذه الجزيئات من الجيل التالي أصعب بكثير على الفيروس في أن "يمحوها"، مما يحسّن قدرتنا على علاج كوفيد‑19 وتفشي الفيروسات التاجية المستقبلي.
الاستشهاد: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
الكلمات المفتاحية: SARS-CoV-2, مقاومة مضادات الفيروسات, نظائر النيوكليوتيد, تصحيح أخطاء الحمض النووي الريبي, تكرار الفيروسات التاجية