Clear Sky Science · ar
تحفيز حمضي لويس لتسريب الهيدروكسيل يمكّن التأكسد الكهربائي الانتقائي لقَيِّ الأسيد إلى نتريت مع إنتاج هيدروجين موفِّر للطاقة بشكل متزامن
تحويل النفايات إلى مواد مفيدة ووقود نظيف
تُعرف اليوريا عادةً كمكوّن في البول والأسمدة، لكن في مياه الصرف تصبح ملوِّثًا عنيدًا. تُظهر هذه الدراسة كيف يمكن تحويل اليوريا من عبء إلى مورد: باستخدام محفز مصمم بشكل ذكي، يحول الباحثون اليوريا إلى نتريت، وهو مركب قيّم يستخدم في الأسمدة والأدوية، بينما يُنتجون في الوقت نفسه وقود الهيدروجين باستخدام كهرباء أقل مما تتطلبه طرق تفكيك الماء التقليدية. تُقدم هذه العمل لمحة عن محطات معالجة مستقبلية تنظف المياه وتنتج منتجات مفيدة وتولّد طاقة نظيفة في آنٍ واحد.
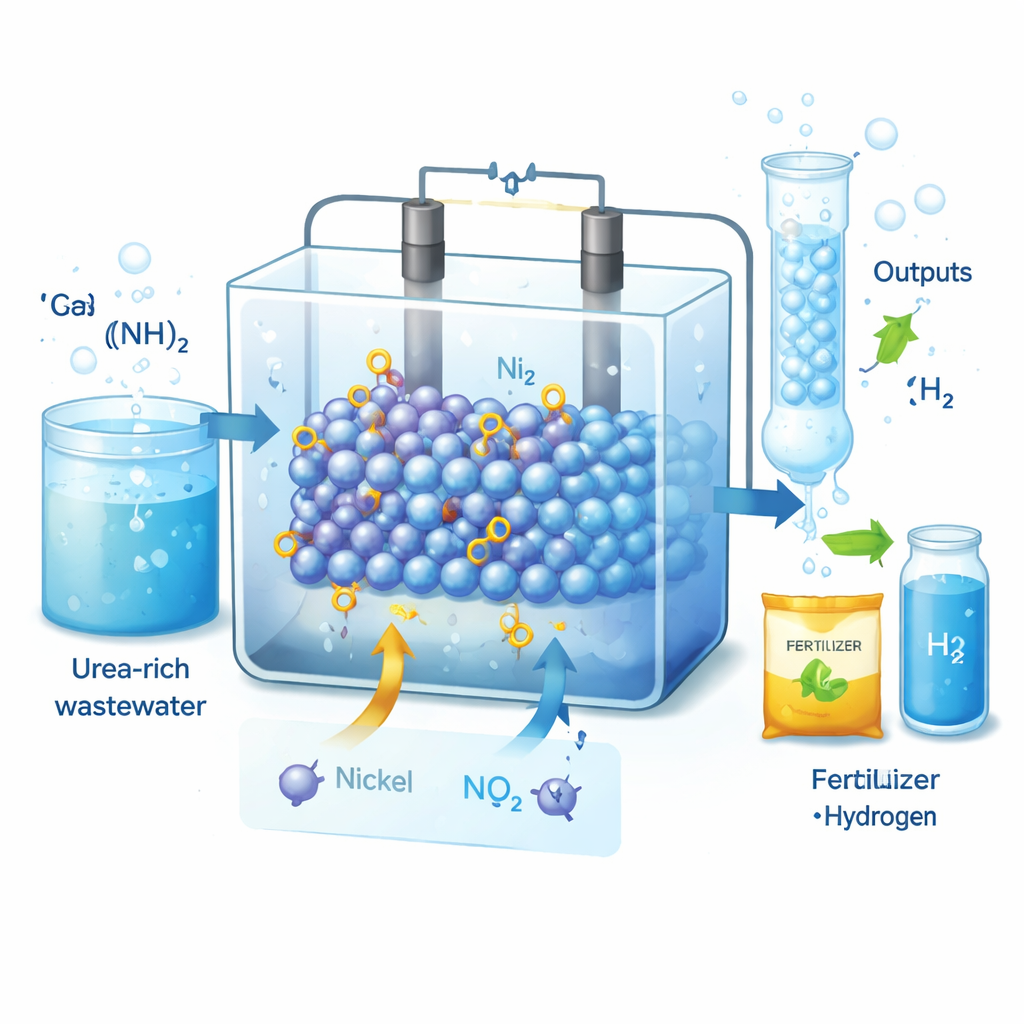
لماذا يهم النتريت والهيدروجين
النتريت مكوّن أساسي في الزراعة وحفظ الأغذية والصناعات الدوائية، والطلب العالمي عليه يقاس بملايين الأطنان سنويًا. اليوم يتم إنتاج معظم النتريت عبر عملية أوستوالد، التي تعمل عند درجات حرارة عالية وتستهلك كميات كبيرة من الطاقة وتطلق أكاسيد النيتروجين الملوِّثة. وفي الوقت نفسه، تحمل مياه الصرف من المنازل والصناعات حمولة ثقيلة من اليوريا، التي تمثل 70–80% من الملوِّثات النيتروجينية. إذا أمكن ترقية تلك اليوريا كهربائيًا إلى نتريت مع إنتاج غاز الهيدروجين، فسنتمكن من تنظيف المياه وتوفير منتجين ذوي قيمة عالية—بشرط أن تكون العملية فعّالة وانتقائية بما فيه الكفاية.
توجيه التفاعلات في المسار الصحيح
عند أكسدة اليوريا في محلول قلوي، يمكن أن تسلك مسارين رئيسيين. أحدهما يؤدي إلى غاز النيتروجين غير الضار وثاني أكسيد الكربون؛ بينما المسار الآخر، الأكثر رغبة، يؤدي إلى النتريت والنيترات، وهما مركبان قابلان للتسويق. المشكلة أن معظم المحفزات القائمة على النيكل، وهي عناصر العمل في هذا التفاعل، ليست انتقائية بدرجة كافية—تميل إلى إنتاج خليط من المنتجات كما تُهدر الطاقة بتحفيز تفاعل تطوُّر الأكسجين، الذي ينتج غاز الأكسجين بدون قيمة تجارية. سعى المؤلفون لإعادة تصميم سطح المحفز بحيث تُتركَّز أيونات الهيدروكسيد (OH⁻) وتُوجَّه بطريقة تُفضّل قطع روابط الكربون–النتروجين وتكوين النتريت بدلًا من السماح بذوبان ذرات النيتروجين في N₂.
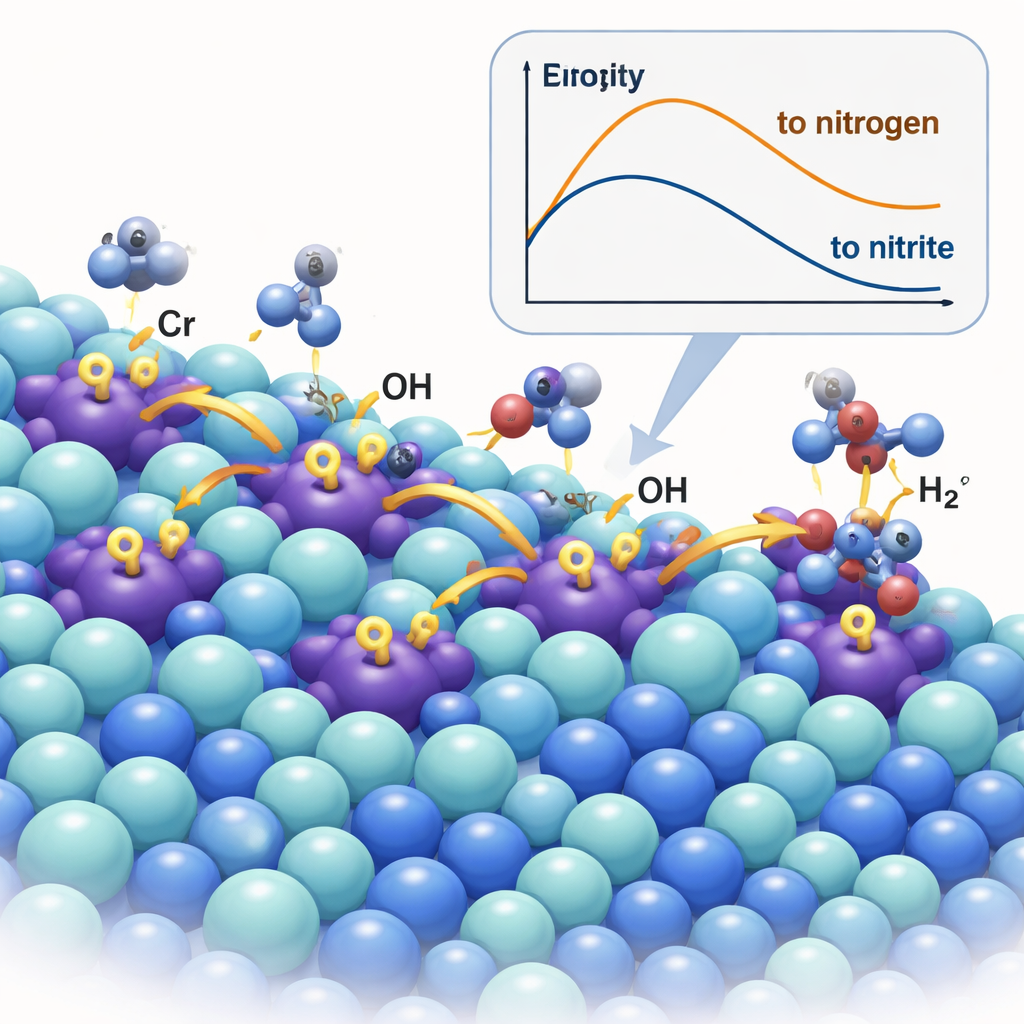
محفز يضخ أنواع نشطة
طوَّر الفريق مادة جديدة عن طريق تطعيم كبريتيد النيكل (Ni₃S₂) بكمية صغيرة من الكروم، مكوِّنين Cr–Ni₃S₂. تعمل أيونات الكروم كمواقع حمض لويس—مراكز فقيرة بالإلكترونات تجذب أيونات الهيدروكسيد بقوة. باستخدام مجاهر متقدمة وتقنيات أشعة X والمطيافية، أكَّد الباحثون أن ذرات الكروم تجلس داخل شبكة كبريتيد النيكل وتسبب انكماشًا وتشوهًا طفيفين فيها، مغيرةً توزيع الإلكترونات. في ظروف التفاعل، تعمل مواقع الكروم مثل مضخات صغيرة: تلتقط OH⁻ ثم «تسرّبها» إلى مواقع النيكل المجاورة، حيث تحدث أكسدة اليوريا فعليًا. تُبَين قياسات رامن والمرتفعة التخصيص في الموقع وكذلك قياسات الأشعة تحت الحمراء، إلى جانب تجارب وسم النظائر، مباشرةً هذا التسريب للهيدروكسيد من الكروم إلى النيكل وأظهرت أنه يسرّع تشكيل مواقع أوكسيدهيدروكسيد النيكل (NiOOH) النشطة التي تدفع الكيمياء المرغوبة.
عوائد عالية، طاقة أقل، وثبات قوي
لأن OH⁻ يُوَصَّل بكفاءة إلى الأماكن الصحيحة، يُحوِّل محفز Cr–Ni₃S₂ اليوريا إلى نتريت بانتقائية مبهرة. عند كثافات تيار ذات صلة صناعيًا، يحقق المحفز إنتاجًا للنتريت يقارب 121 مليغرامًا في الساعة لكل سنتيمتر مربع مع كفاءات فارادية للنتريت فوق 80%، مع إبقاء تطوُّر الأكسجين المتنافس أقل من 1.5%. يظل المحفز مستقرًا على مدى مئات الساعات من التشغيل المستمر مع تسرب كروم ضئيل للغاية. تخفض نفس المادة أيضًا الجهد المطلوب بشكل كبير عندما تُزاوج مع قطب مهبطي لتطور الهيدروجين في جهاز فصل المياه بمساعدة اليوريا، مما يقلل تكلفة الكهرباء لإنتاج الهيدروجين إلى حوالي 3.7 كيلوواط-ساعة لكل متر مكعب من H₂—أقل من التحليل الكهربائي القلوي التقليدي. تشير تحليلات تقنية-اقتصادية إلى أنه عند 400 ملي أمبير لكل سنتيمتر مربع، قد يؤدي معالجة طن واحد من اليوريا في هذا النظام إلى توليد قيمة صافية على ترتيب 1,200 دولار عند احتساب كل من النتريت والهيدروجين.
من خلية مخبرية إلى أجهزة طاقة عملية
لإظهار الإمكانات العملية، بنى المؤلفون خلية تدفق للفصل المستمر لمياه مساعدة باليوريا وبطارية Zn–يوريا–هواء. في البطارية، أدى استبدال تفاعل تطور الأكسجين المعتاد أثناء الشحن بتفاعل أكسدة اليوريا إلى خفض جهد الشحن بنحو 0.3 فولت مع الحفاظ على أداء مستقر لأكثر من 100 ساعة. هذا يعني أن الجهاز يمكنه تنظيف تيارات محتوية على اليوريا وتوفير تخزين كهربائي بكفاءة طاقية أعلى. نجحت نفس استراتيجية تصميم حمض لويس أيضًا عند استخدام معادن أخرى مثل القصدير والتيتانيوم، أو مضيف مختلف مثل كبريتيد النحاس، مما يشير إلى أن المنهجية قابلة للتطبيق على نطاق واسع.
فكرة بسيطة وراء تفاعل معقد
بالنسبة لغير المتخصصين، الفكرة الأساسية هي أن الباحثين تعلّموا كيف يوجّهون أين وكيف يهبط ويتحرك مكوّن تفاعلي شائع—الهيدروكسيد—على سطح المحفز. بإضافة مواقع كروم تعمل كجاذبات وموصلات قوية لـ OH⁻، يسهلون تقطيع جزيئات اليوريا إلى نتريت بدلًا من حرقها بالكامل إلى غاز النيتروجين. وفي الوقت نفسه، يتطلب هذا المسار طاقة كهربائية أقل وينتج وقود الهيدروجين بشكل طبيعي. في جوهره، تُظهر الدراسة أن التصميم الذري الدقيق لأنماط «حركة المرور» على المحفز يمكن أن يحوّل مياه الصرف إلى مصدر لكل من الكيماويات والطاقة النظيفة.
الاستشهاد: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
الكلمات المفتاحية: أكسدة اليوريا, إنتاج النتريت, توليد الهيدروجين, التحفيز الكهربائي, استغلال مياه الصرف