Clear Sky Science · ar
خريطة متعددة الأوميك المتكاملة تكشف تسلسل شبكات التنظيم الزمكانية خلال تكوّن جنين الفأر
كيف يبني الجنين مخطط جسمه
كل ثديي، بما في ذلك البشر، يبدأ حياته كمجموعة صغيرة من الخلايا التي يجب أن تنظم بسرعة إلى جسم معقد ذو رأس وذيل وظهر وبطن وأعضاء داخلية. يحدث هذا التشكّل الجذري خلال نافذة زمنية قصيرة تُسمى الغاسترولايشن. الورقة التي نلخّصها هنا تبني خريطة مفصّلة ومتعددة الطبقات لهذه العملية في أجنة الفأر، مبيّنة كيف تتعاون الجينات ومفاتيح الحمض النووي والإشارات الكيميائية في المكان والزمان لتوجّه الخلايا نحو مصائرها المستقبلية.
مراقبة آلاف الخلايا وهي تختار مصائرها
لمتابعة الغاسترولايشن أثناء حدوثه، حلل الباحثون أكثر من 35,000 خلية فردية من أجنة فأر عبر خمس مراحل متقاربة زمنياً، من بدايات إلى نهايات الغاسترولايشن. لكل خلية، قاسوا ليس فقط أي الجينات كانت مفعلة، بل أيضاً أي مقاطع من الحمض النووي كانت مفتوحة وسهلة الوصول—مؤشر على إمكانية عملها كمفاتيح تنظيمية. باستخدام هذه البيانات، حدّدوا 31 نوع خلية مميزة وتتبعوا كيف تتفرع الخلايا المبكرة المرنة تدريجياً إلى الطبقات الجرثومية الثلاث الرئيسية—الظهارية (ectoderm)، الميزودرم، والاندودرم—التي تشكّل لاحقاً كل الأنسجة والأعضاء. كما طوروا طريقة حاسوبية جديدة، BioCRE، لربط الجينات بعناصر الحمض النووي المسيطرة عليها بدقة أكبر، كاشفين أن العديد من المفاتيح المهمة تقع بعيداً عن الجينات التي تنظّمها.
بناء أطلس جزيئي ثلاثي الأبعاد في فضاء الجنين الحقيقي
تفقد معظم طرق الخلية الواحدة موقع كل خلية الأصلي داخل الجنين، لكن الموقع أمر حاسم لفهم النمطية. تغلّب الفريق على ذلك بمواءمة بيانات الخلية الواحدة مع خريطة ثلاثية الأبعاد قائمة لنشاط الجينات في أجنة الفأر. النتيجة هي ST-MAGIC، «جنين رقمي» تُعلَّم فيه كل نقطة صغيرة بأنواع الخلايا المحتملة الموجودة، والجينات التي تعبّر عنها، وإتاحة مقاطع الحمض النووي المحيطة. يظهر هذا الأطلس، على سبيل المثال، كيف تظهر تحتأنواع ميزودرم مختلفة—قلب مستقبلي وعضلات وأنسجة داعمة—في مناطق مميزة وكيف تستخدم جينات واسعة التعبير مثل Otx2 عناصر تنظيمية مختلفة على السطح الخارجي للجنين (الإيبيبلست) والسطح الداخلي (الاندودرم الحشوي).
عندما ينكسر التناظر ويصبح اليسار مختلفاً عن اليمين
سمة لافتة في مخططات الأجسام أن الجانبين الأيسر والأيمن ليسا متطابقين—فكر في القلب الموضوع قليلاً نحو اليسار. استخدم المؤلفون أطلسهم المكاني للتعمّق في الميزودرم الجانبي، حيث تظهر فروق اليسار–اليمين لأول مرة. وجدوا تفاوتات دقيقة لكنها متسقة في أنواع الخلايا المنتمية لكل جانب وفي مناطق الحمض النووي الأكثر انفتاحاً. على الجانب الأيمن، كانت المناطق المرتبطة بمسار إشارة نمو يسمى BMP أكثر قابلية للوصول؛ وعلى الجانب الأيسر، كانت المناطق المرتبطة بجينات مطلوبة لتكوين الفقرات وبنى القلب مهيمنة. بعض هذه العناصر في الحمض النووي، بما في ذلك عناصر مكتشفة حديثاً تتحكم في الجين Lefty2، تفتح قبل ظهور فروق في التعبير الجيني يمكن رؤيتها، ما يقترح أن «تهيئة» مبكرة للكروماتين تُعدّ كل جانب من الجنين لتفسير الإشارات بشكل مختلف.
تتابع من العوامل يوجّه منتصف الجسم
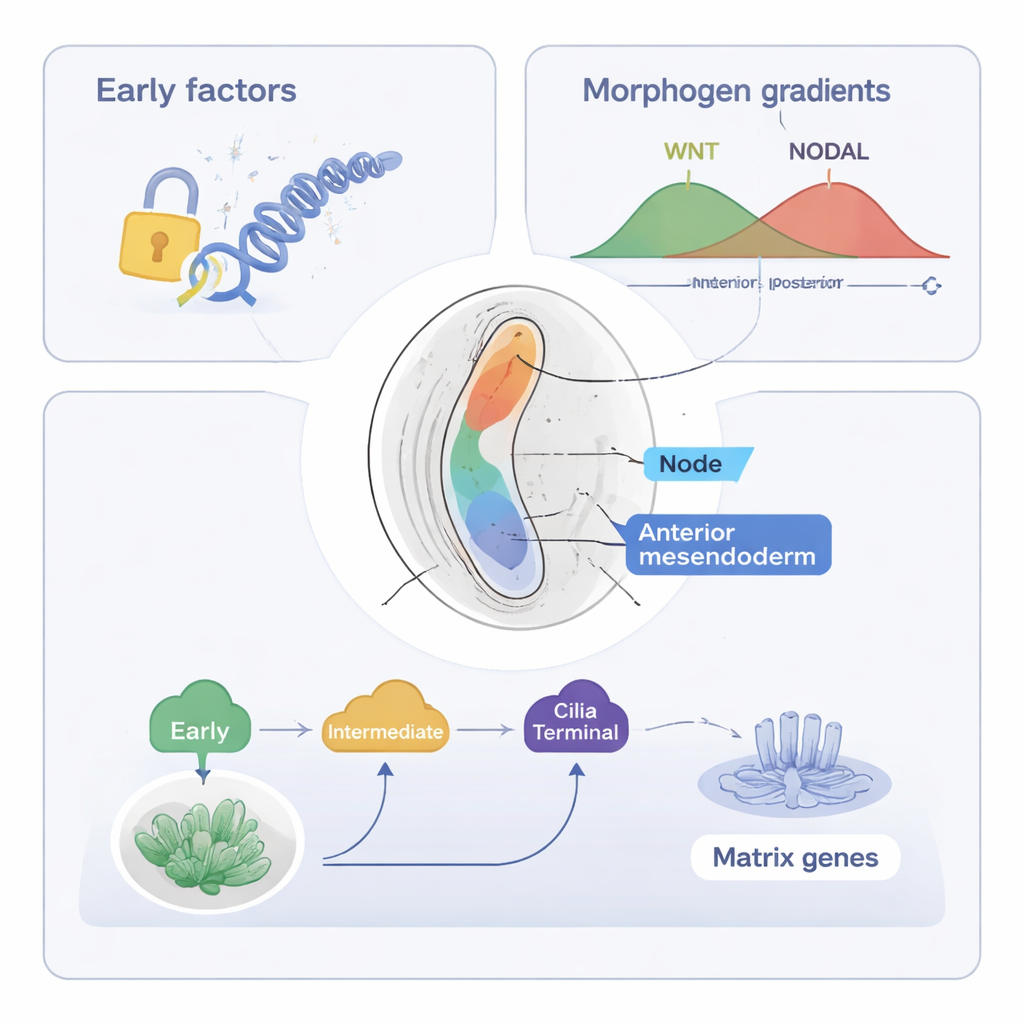
تركّز الدراسة بعد ذلك على الميزندودرم المحوري، مجموعة من الخلايا التي ستكوّن النوتوكد—بنية عصوية تمتد على طول الخط المتوسط وتساعد في تنظيم العمود الفقري والجهاز العصبي. باستخدام أدواتهم المدمجة (ST-MAGIC وإصدار موسّع يسمى ST-MAGIC (+))، تتبع المؤلفون كيف تنشأ هذه الخلايا من الشريط البدائي الأمامي وتتشقّق إلى فرعين: خلايا العقدة، التي تبني بنية مهدّبة مهمة لحسّ اليسار–اليمين، والميزندودرم الأمامي، الذي يساهم في أنسجة الخط المتوسط. كشفوا عن تسلسل هرمي من عوامل النسخ—بروتينات تتحكم في نشاط الجينات. العوامل المبكرة، مثل EOMES، والعوامل الوسطية، بما في ذلك FOXA2 وLHX1، تفتح أولاً مناطق رئيسية من الحمض النووي وتؤسس الاستجابة لإشارات كبرى مثل WNT وNODAL. لاحقاً، عوامل «نهائية» مثل NOTO وSOX9 وعامل جديد مرتبط POU6F1 تشغّل برامج جينية متخصصة، على سبيل المثال تلك اللازمة للأهداب أو للمادة خارج الخلوية.
الإشارات والكروماتين والمتخصّصون الذين يعملون في وقت متأخر
بدمج مجموعات بيانات منشورة عن مواقع ارتباط عوامل وساطة إشارة WNT وNODAL بالحمض النووي، أظهر المؤلفون أن استجابة الجنين لهذه الإشارات تتحرّك مكانياً قبل أن تتحرّك مصادر الإشارة نفسها. في المنطقة المهيأة لتصبح ميزندودرم محوري، تُفتح مواقع الحمض النووي المستجيبة لـNODAL وWNT مبكراً، ويحتوي العديد منها على نماذج ارتباط لعوامل مثل FOXA2 وZfp281 ومنظمات أخرى، مما يوحي بسيطرة تعاونية. الحذف التجريبي للعوامل العاملة متأخراً NOTO وPOU6F1 في الفأر أعاق التعبير عن جينات خاصة بالعقدة والمتعلقة بالأهداب وقصّر أهداب العقدة، ومع ذلك بقيت الخريطة الأساسية لمقاطع الحمض النووي المفتوحة سليمة إلى حد كبير. هذا يشير إلى أن العوامل المبكرة تضع الأساس الأبجيني، بينما تعمل العوامل المتأخرة أساساً على تنقيح التعبير الجيني دون إعادة تشكيل الكروماتين.
لماذا يهم هذا لفهم التطور
لغير المتخصص، يمكن اعتبار هذا العمل بمثابة بناء «مخطط أسلاك» عالي الدقة لكيفية تخطيط الجنين لمخطط جسمه. يُظهر المؤلفون أن قرارات مصير الخلايا خلال الغاسترولايشن تُحكم ليس فقط بالإشارات الموجودة، بل أيضاً بموعد ومكان فتح مفاتيح الحمض النووي وبأي عوامل نسخ تعمل بالتتابع. توفر أطلسات ST-MAGIC وST-MAGIC (+) مورداً لاستكشاف هذه العلاقات عبر المكان والزمان، مقدمين إطاراً يمكن أن يوجه دراسات عن عيوب الولادة ونماذج الأجنة القائمة على الخلايا الجذعية، وفي النهاية جوانب من التطور البشري.
الاستشهاد: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
الكلمات المفتاحية: التكوّن البطني (غاسترولايشن), شبكات تنظيم الجينات, تعدد الأوميك على مستوى الخلية الواحدة, نمطية الجنين, تطور الفأر