Clear Sky Science · ar
التحورات الجديدة في جين عامل القص SF3B1 مرتبطة باضطرابات النمو العصبي
حين يعطل جين واحد المخطة المبكرة للدماغ
لماذا يصاب بعض الأطفال بصعوبات تعلم أو نوبات صرع أو مشاكل في التغذية رغم أن الحمل والولادة بديا طبيعيين؟ تفحص هذه الدراسة جيناً واحداً يُدعى SF3B1، يساعد الخلايا على معالجة الرسائل الجينية. يوضح الباحثون أن تغيّرات جديدة وعفوية في هذا الجين يمكن أن تشوّه بشكل طفيف الطريقة التي تقرأ بها خلايا الدماغ تعليمات الـDNA، ما يؤدي إلى متلازمة نمو عصبي لم تكن معروفة سابقاً.
محرّر رئيسي للرسائل الجينية
تحتاج كل خلية في أجسامنا إلى تحويل النص الجيني الخام إلى تعليمات واضحة قبل أن تتمكن من تصنيع البروتينات. تُعرف هذه الخطوة التحريرية باسم قصّ الحمض النووي الريبوزي (RNA splicing)، التي تزيل المقاطع غير المشفرة وتلصق الأجزاء المفيدة معاً. يُعد SF3B1 مكوّناً مركزياً في “آلة القص” الخلوية. حتى الآن، كانت التغيّرات في SF3B1 معروفة أساساً بدورها في السرطانات، حيث تكتسب خلايا الورم طفرات في هذا الجين خلال الحياة. تطرح العمل الجديد سؤالاً مختلفاً: ماذا يحدث عندما يكون تغيير ضار في SF3B1 موجوداً منذ لحظة التكوين في كل خلية من خلايا الجسم؟
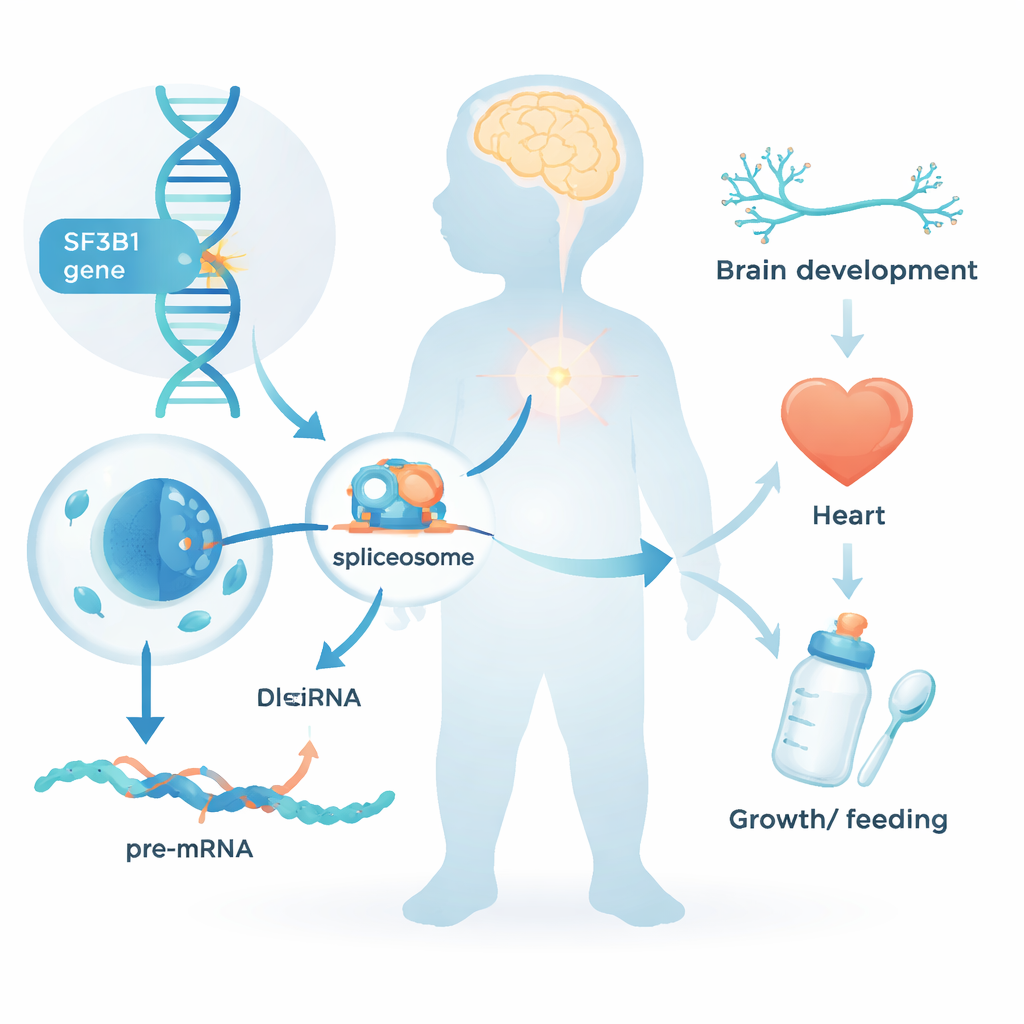
متلازمة طفولية معترف بها حديثاً
جمع الفريق بيانات من 26 طفلاً وشاباً يحملون جميعاً نسخاً نادرة من SF3B1، نشأت معظمها de novo — أي لم تُورَث من أي من الوالدين. كان لدى ما يقرب من جميعهم مشاكل في النمو العصبي: تأخّر في الجلوس أو المشي أو الكلام؛ اضطراب عقلي بدرجة خفيفة إلى متوسطة في معظمه؛ وفي نحو نصف الحالات، نوبات صرع. عانى كثيرون من توتر عضلي منخفض واحتاجوا مساعدة إضافية في التغذية، أحياناً عبر أنبوب المعدة. كانت الملامح الوجهية غير عادية بشكل طفيف لكنها لم تكن متطابقة من طفل لآخر؛ وُجدت سمة شائعة لافتة هي ارتفاع أو شقّ في سقف الحلق. كما كان لدى عدة مشاركين عيوب قلبية، أو قِصْر في النمو، أو صغر حجم الرأس، ما يدل على أن تأثير تغيّرات SF3B1 يمتد إلى ما وراء الدماغ.
نوعان من التغيّرات الجينية، نمطان سريريان
ميّز الباحثون بين نوعين عريضين من متغيرات SF3B1. تضمنت المجموعة الأولى تغيّرات «فقدان الوظيفة»، مثل إشارات التوقف المبكرة، التي يُتوقع أن تقلل كمية بروتين SF3B1 الفعّال. احتوت المجموعة الثانية على متغيرات مُغيّرة للحمض الأميني (missense)، حيث يتغير حمض أميني واحد في البروتين. من خلال تجميع السمات الطبية للأطفال، لاحظ الفريق أن الذين لديهم متغيرات من نوع missense يميلون إلى أن يعانوا من مشاكل أشد وأعقد، بما في ذلك معدل أعلى من عيوب القلب والجهاز الهضمي، قصر القامة، وصغر حجم الرأس. في المقابل، كانت متغيرات فقدان الوظيفة تُرِث أحياناً من والد أو والدة متأثرين بشكل طفيف أو حتى بدا عليهما الصحة، مما يوحي بأن تقليل كمية SF3B1 قد يتوافق مع أعراض معتدلة نسبياً لدى بعض الأفراد.
أخطاء في الضبط الدقيق بدلاً من انهيار كامل
لفهم ما تفعله متغيرات الـmissense داخل الخلايا، أعاد العلماء خلقها في خطوط خلوية مختبرية. بشكل مفاجئ، كانت هذه البروتينات المُعدّلة من SF3B1 قادرة على أداء وظيفة القص الأساسية بما يكفي لإنقاذ خلايا تم إخماد SF3B1 الطبيعي فيها. هذا استبعد تفسير فقدان الوظيفة البسيط. باستخدام تسلسل RNA العميق، نظر الفريق بعد ذلك عبر مجموعة الرسائل الخلوية بأكملها. وجدوا أن متغيرات الـmissense حوّلت قصّ مئات الجينات بشكل طفيف، لا سيما بتغيير مواقع القصّ التي تُختار عند نهايات الإكسونات والتسبب أحياناً في تخطّي إكسونات. كان حجم الاضطراب أصغر من ذلك المرصود مع الطفرة المتعلقة بالسرطان K700E، لكنه لا يزال ملحوظاً: العديد من الجينات المتأثرة تشارك في نمو الدماغ، وتوصيل الأعصاب، وعمليات أساسية مثل التعامل مع RNA وتركيب البروتين.
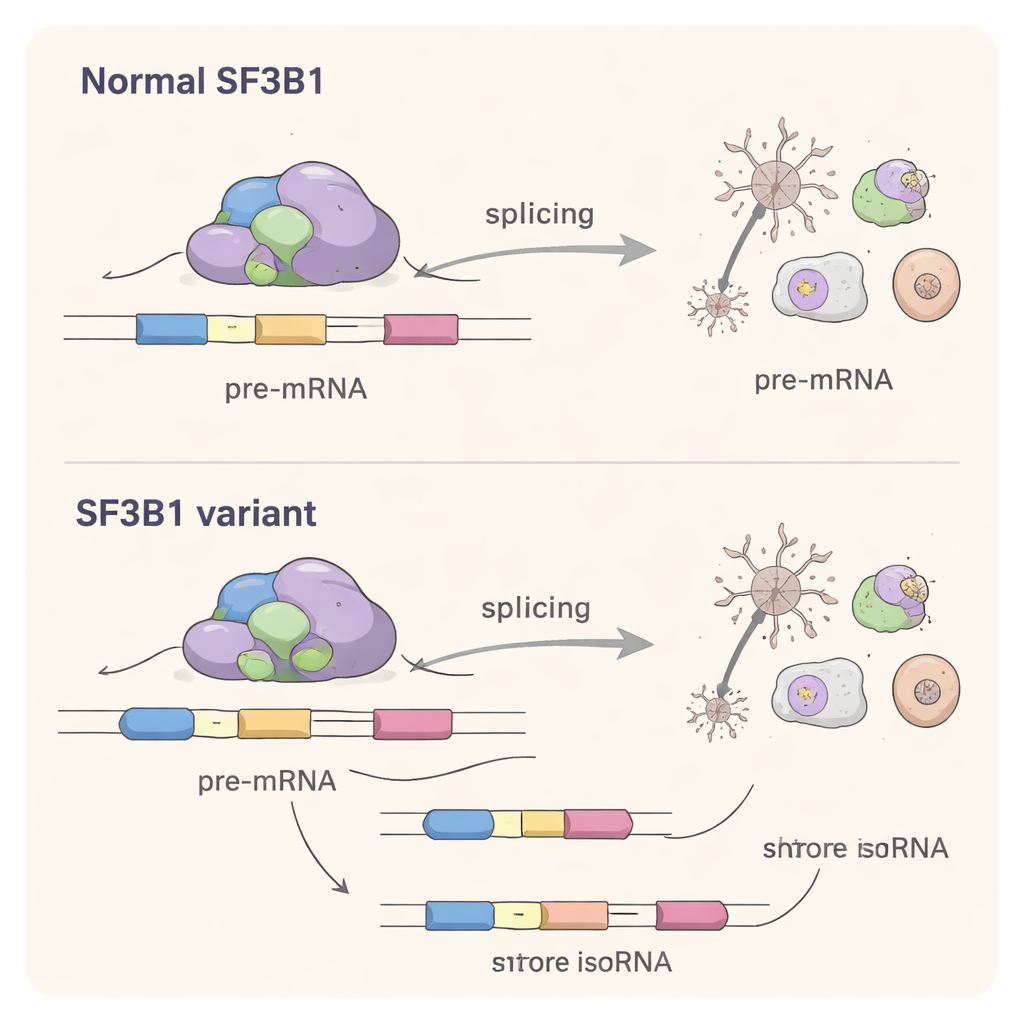
آلية مشتركة بين السرطان واضطرابات الدماغ
على الرغم من أن معظم متغيرات SF3B1 المرتبطة بالنمو العصبي تحدث في مواقع مختلفة عن الطفرات المعروفة في السرطان، فإنها تُعطّل نفس العملية الجوهرية: التعرف الدقيق على مواقع القص في RNA. تُظهر الدراسة أن لهذه المتغيرات التطويرية «بصمة قصّ» خاصة بها، تختار مواقع قص بديلة غالباً ما تكون أقرب إلى المواقع الطبيعية مما هو مفضل في السرطان. يشير هذا إلى آلية تغير الوظيفة، حيث تتنافس النسخة المحوّلة من البروتين مع النسخة الطبيعية وتدفع آلة القص نحو اختيارات خاطئة إلى حد ما في العديد من الجينات دفعة واحدة.
ماذا يعني هذا للعائلات وللبحث المستقبلي
بالنسبة للعائلات المتأثرة، تُحدّد هذه الدراسة SF3B1 كسبب جديد لاضطرابات النمو العصبي يمكن اختباره الآن في عيادات الوراثة، مما قد يُنهي بحثاً تشخيصياً طويلاً. وعلى نطاق أوسع، تضيف الدراسة SF3B1 إلى قائمة صغيرة لكنها متنامية من جينات القصّ التي يمكن لتغيّراتها أن تُسبب إما السرطان أو اضطرابات دماغية طفولية، حسب زمن وكيفية حدوث التغيير. من خلال رسم خريطة الكيفية التي تعيد بها متغيرات SF3B1 تشكيل قصّ RNA، تمهد الدراسة الطريق لعلاجات مستقبلية تهدف إلى تصحيح الأخطاء في القصّ بشكل مستهدف.
الاستشهاد: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
الكلمات المفتاحية: قصّ الحمض النووي الريبوزي, SF3B1, اضطرابات النمو العصبي, تحورات جديدة, أمراض متعلقة بالجسيم الطيّفي