Clear Sky Science · ar
هيدروجيل لزج-مرن يُهيّئ البلاعم المُعدّلة بمستقبلات CAR لعلاج التليف الرئوي
تحويل عمال النظافة في الجسم إلى فرق إصلاح دقيقة
التليف الرئوي مرض رئوي مدمر تتحول فيه الأنسجة الهوائية المرنة تدريجياً إلى ندب صلبة. يكافح المرضى من أجل التنفس، وفي الوقت الحالي تقتصر الأدوية غالباً على إبطاء التدهور. تستكشف هذه الدراسة فكرة جديدة: تحويل خلايا التنظيف الذاتية في الجسم، البلاعم، إلى «عمال نظافة ذكيين» مهندَسين ثم تعزيز قدرتهم بواسطة هيدروجيل طري مصمَّم خصيصاً. معاً، تساعد هذه الحيل الخلايا على تتبُّع مسببات التندب وحتى تليين الأنسجة الصلبة في الرئتين المتضررتين.
عندما يصبح الشفاء ضاراً
في الرئتين السليمتين، تساعد الخلايا الليفية في الحفاظ على شبكة دقيقة من الكولاجين تدعم الحويصلات الهوائية. في التليف الرئوي، تصبح هذه الخلايا مفرطة النشاط، فترسخ خيوطاً سميكة من الكولاجين تخنق الفراغات الهوائية. يمكن للأدوية الحالية أن تخفف هذه العمليات لكنها نادراً ما تعكسها. يركز المؤلفون على علامة سطحية خلوية تسمى بروتين تنشيط الخلايا الليفية (FAP)، وهو وفير على الخلايا الليفية المفرطة النشاط ونادر في الأنسجة الطبيعية. إذا أمكن تدريب خلايا المناعة على التعرف على FAP، فقد تزيل بشكل انتقائي الخلايا الليفية «الهاربة» التي تحفز التندب مع ترك الخلايا السليمة محفوظة.
إعادة برمجة البلاعم لاستهداف باني التندب
البلاعم خلايا مناعية متجولة تبلع عادة الخلايا الميتة والميكروبات وحطام الخلايا. جهز الفريق هذه البلاعم بمستقبل مضاد خلطي (CAR) يتعرف على FAP، مكوّناً بلاعم‑CAR (CAR‑Ms). في الأطباق المخبرية، بلعت هذه البلاعم المعدلة بكفاءة الخلايا الليفية الغنية بـFAP وقتلتها، بينما تجاهلت إلى حد كبير الخلايا ذات مستويات FAP المنخفضة. كما أنهت هياكل هلامية غنية بالكولاجين بقوة أكبر من البلاعم غير المعدلة، ما يوحي بفائدتين: إزالة الخلايا المولدة للتندب وتفكيك مصفوفة الندبة نفسها مباشرة. ثبتت هذه التأثيرات سواء في خطوط خلوية قياسية أو في بلاعم فأرية أولية، الأقرب إلى الوضع الطبيعي في الأنسجة. 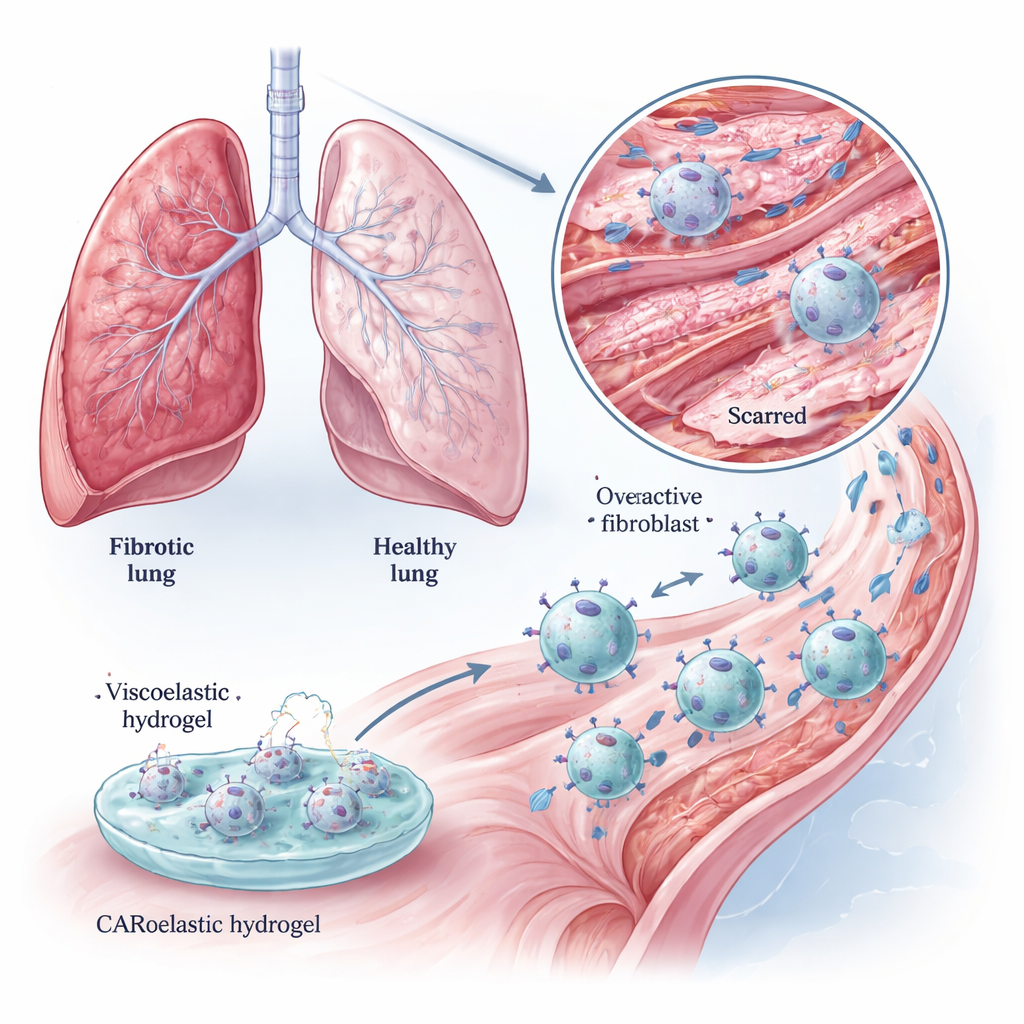
تهيئة خلايا المناعة بهيدروجيل طري لزج-مرن
الهندسة الجينية للخلايا قوية لكنها معقدة. لذلك تساءل الباحثون عما إذا كان مؤشّرٌ فيزيائي بحت — هيدروجيل طري لزج‑مرن — يمكنه ضبط سلوك بلاعم‑CAR بشكل إضافي. بنوا هيدروجيل من الجيلاتين والألجinate يمكن ضبط «معاوقة الفقدان» فيه، وهي مقياس لمدى استرخائه التدريجي تحت الإجهاد، بدقة دون تغيير الصلابة الكلّية. عندما حُضّرت بلاعم‑CAR لفترة وجيزة على هياكل هلامية ذات لزوجة مناسبة، زادت قدرتها على قتل الخلايا الليفية المستهدفة أكثر من المنشطات الكيميائية الشائعة، ودام هذا التعزيز على الأقل يومين. كما شغّلت هذه «Gel‑CAR‑Ms» جينات مرتبطة بتنشيط المناعة وإعادة تشكيل الأنسجة، بينما قللت التعبير عن جينات مرتبطة بالتليف، مما يوحي بأن تجربة الجل طبعت هوية أكثر مقاومة للتندب على هذه الخلايا.
كيف يعيد سطح أطرى توصيل سلوك الخلية
لفهم سبب تأثير الجل، فحص الفريق الحالة الفيزيائية لمستقبلات CAR على سطح الخلية. أظهر مسبار فلوريسنتي أن بلاعم‑CAR المُهيأة على الهيدروجيل كانت أقل توتراً غشائياً — أي أن الغشاء الخارجي للخلايا كان أكثر استرخاءً. في هذه الحالة، انتشرت جزيئات CAR من تجمعات ضيقة إلى وحدات مفردة وأزواج أكثر عزلة. أظهرت اختبارات بيوكيميائية أن هذه المستقبلات المشتتة فضّلت أشكالاً تُثير الإشارة الداخلية بسهولة أكبر، وخصوصاً على طول مسارات مثل ERK التي تتحكم في التنشيط والقدرة على القتل. وقد كرر محاكاة انخفاض التوتر باستخدام جزيء صغير نفس انتشار المستقبلات وتحسن القتل للخلايا المستهدفة، داعماً الفكرة القائلة إن استرخاء الغشاء الميكانيكي يكفي لـ«تسليح» الخلايا قبل أن تلتقي بأهدافها. 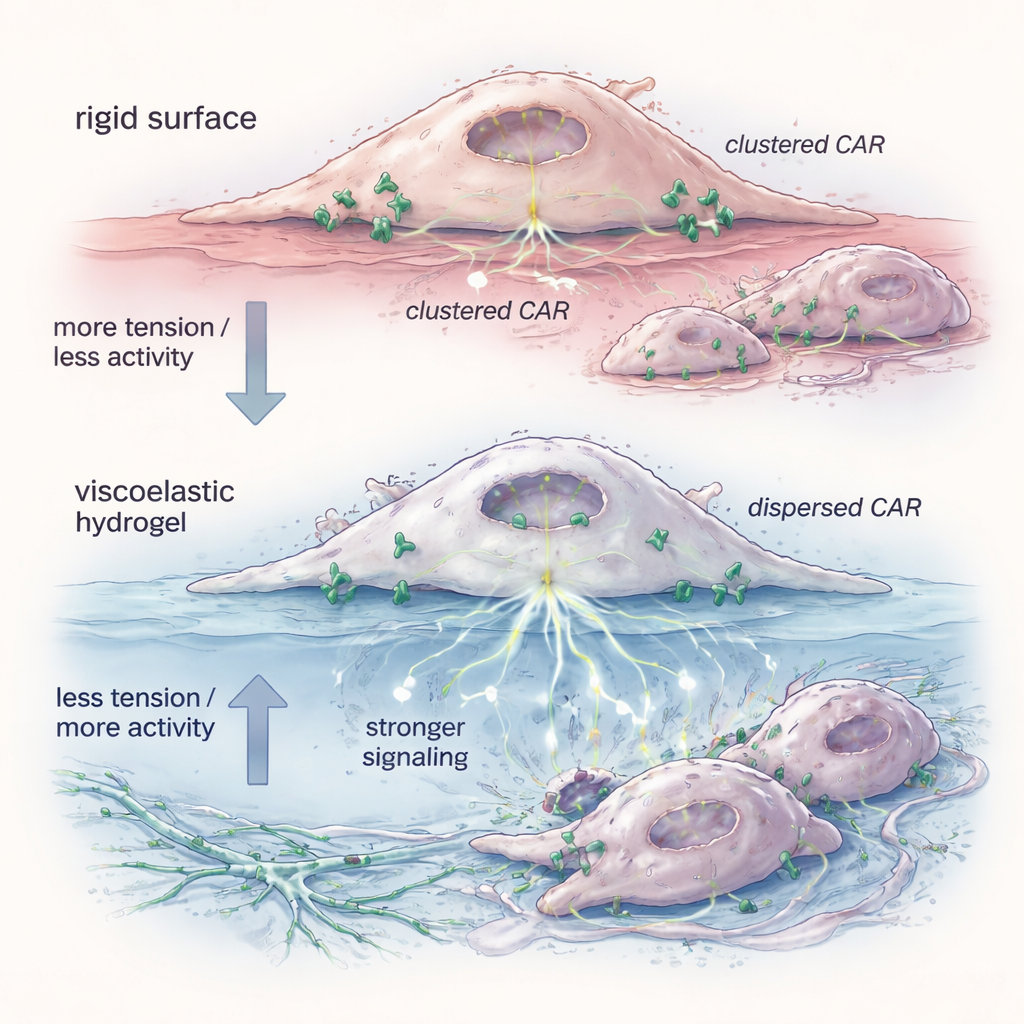
إصلاح الرئتين المتندبتين في الفئران
الاختبار الحاسم كان نموذج فأري لتليف رئوي ناتج عن دواء. تلقت الحيوانات إما بلاعم عادية، أو بلاعم‑CAR قياسية، أو Gel‑CAR‑Ms المُهيأة بالهيدروجيل. تحسنت كل الحيوانات المعالجة مقارنةً بالمجموعة غير المعالجة، لكن أداء Gel‑CAR‑Ms كان الأفضل: احتوت رئاتها على كولاجين أقل، ومساحات هوائية أكثر طبيعية، وعدداً أقل من الخلايا الليفية الإيجابية لـFAP. أظهرت تحليلات التعبير الجيني في أنسجة الرئة أن Gel‑CAR‑Ms هدّأت الإشارات الالتهابية وخفّضت تعبير جينات مرتبطة بالندبة أكثر فعالية من البلاعم‑CAR القياسية. استمرت الخلايا المتتبعة في الرئتين لمدة أسبوع على الأقل، وفحوصات السلامة الممتدة على مدار 12 أسبوعاً لم تكشف عن أضرار رئيسية في الأعضاء أو شذوذات دموية أو علامات لأمراض مناعية ذاتية.
اتجاه جديد لعلاجات مضادة للتليف معتمدة على الخلايا
لغير المتخصصين، الرسالة الأساسية هي أن الجمع بين هندسة الخلايا المستهدفة والمواد الذكية يمكن أن يحول الخلايا المناعية الفطرية إلى أدوات فعّالة للغاية لمكافحة الندب من دون تعقيد جيني مفرط. من خلال إراحة البلاعم المُهندَسة لفترة وجيزة على هيدروجيل طري مضبوط بعناية، ضبط الباحثون ميكانيكياً مستقبلاتها السطحية إلى وضع أكثر استجابة. في فئران مصابة بتليف رئوي، تُرجم هذا إلى إزالة أفضل للخلايا الليفية الضارة، وتحلل للكولاجين الزائد، واستعادة جزئية للهيكل الرئوي الطبيعي — دون مشكلات سلامة واضحة. ورغم أن ثمة عملاً كثيراً قبل التجارب البشرية، تشير هذه الاستراتيجية إلى أن ضبط البيئة الفيزيائية للخلايا العلاجية قد يجعل علاجات أمراض الرئة التليفية أكثر قوة ودقة يوماً ما.
الاستشهاد: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
الكلمات المفتاحية: التليف الرئوي, علاج البلاعم بمستقبلات CAR, هيدروجيل لزج-مرن, بروتين تنشيط الخلايا الليفية, ميكانيوبايولوجيا الخلايا