Clear Sky Science · ar
الأساس الجزيئي لكبح ترميز الدنا الجديد بواسطة TCL1A
كيف تقرر الخلايا ما الذي تحتفظ به في الذاكرة
تحمل كل خلية في جسدك تقريبًا نفس الحمض النووي، ومع ذلك تتصرف خلايا الدماغ والدم والجلد بشكل مختلف تمامًا. إحدى الطرق التي "تتذكر" بها الخلايا هويتها هي من خلال علامات كيميائية تُضاف إلى الحمض النووي، وهي عملية تسمى ميثلة الحمض النووي. تكشف هذه الدراسة، بتفاصيل ذرية، كيف يمكن لبروتين صغير يسمى TCL1A أن يوقف عمل الإنزيمات التي تضيف تلك العلامات الميثيلية. وبما أن كلًا من ميثلة الحمض النووي وTCL1A مرتبطان بالسرطان واضطرابات الخصوبة، فإن فهم هذا الصراع الجزيئي قد يلهم في نهاية المطاف علاجات جديدة.
آلية وسم الحمض النووي في الخلية
تعمل ميثلة الحمض النووي مثل علامة قلم رصاص على هامش الجينوم، تساعد في إخماد بعض الجينات وتثبيت الجينوم أثناء تطور الخلايا. إنزيمان، DNMT3A وDNMT3B، هما الكاتبان الرئيسيان اللذان يضعان علامات ميثيل جديدة خلال التطور المبكر وعندما تتمايز الخلايا الجذعية. إذا عُدتلت أو سُيّرت هذه الإنزيمات بشكل خاطئ، فقد تُخلط أنماط علامات الحمض النووي، مساهِمةً في متلازمات تطورية وسرطانات دموية. يُعرف TCL1A كبروتين له دور في سرطانات خلايا الجهاز المناعي حيث يُنتج بكثرة في كثير من الأحيان. أشارت أعمال سابقة إلى أن TCL1A يمكن أن يرتبط بـDNMT3A وDNMT3B ويقلل من نشاطهما، لكن لم يكن معروفًا كيف ينجز هذا الحجب بالضبط.
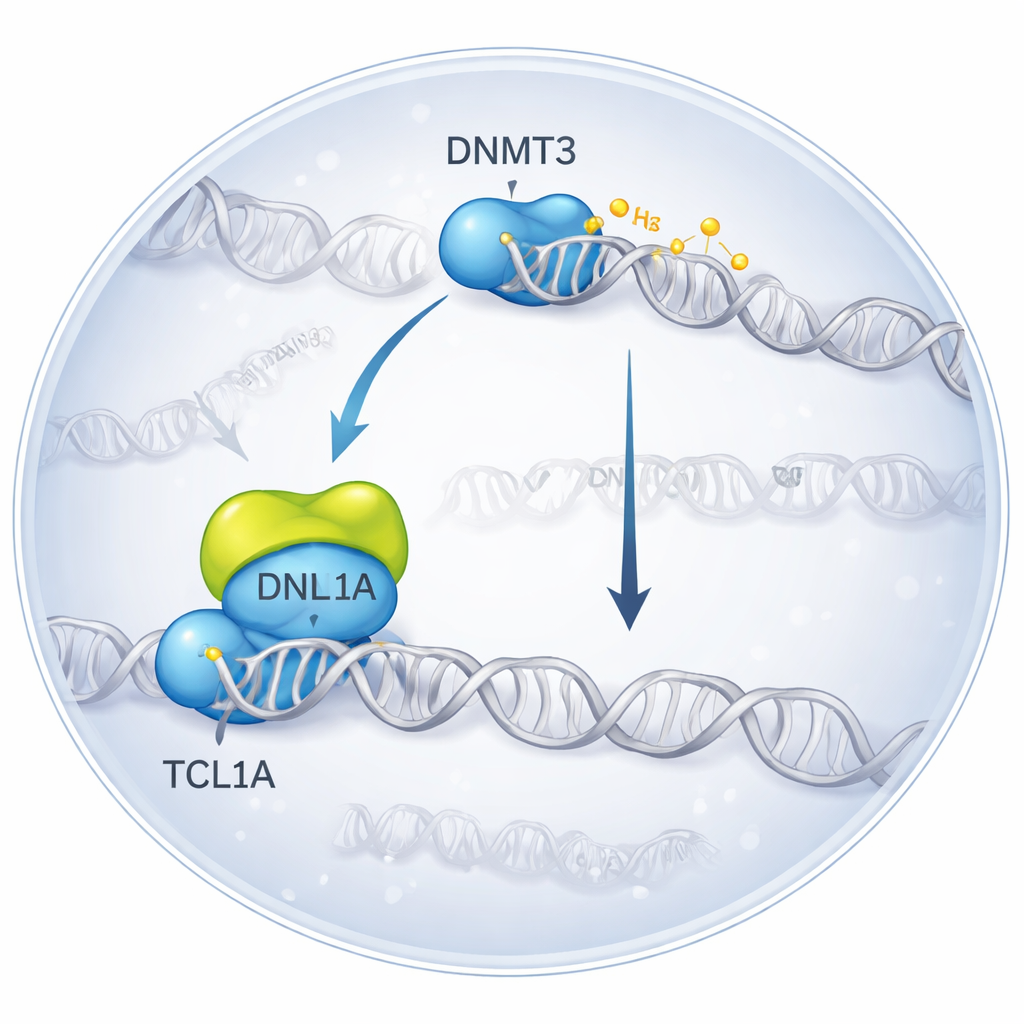
تجميد لقاء جزيئي ثلاثي الأبعاد
استخدم الباحثون المجهر الإلكتروني بالتبريد، تقنية تصوّر الجزيئات المجمدة بسرعة، لرؤية البنية المعقّدة عندما يرتبط DNMT3A بـTCL1A. وجدوا أن جزيئَي DNMT3A يتزاوجان، وعلى كل جانب يرسو ثنائٍ لـTCL1A على الجزء التحفيزي من DNMT3A—وهو نفس النطاق الذي يتفاعل عادة مع بروتينات مساعدة والحمض النووي. يتداخل سطح الارتباط هذا مع الموقع الذي يرتبط به شريك آخر، DNMT3L، عادةً لتعزيز نشاط DNMT3A. في اختبارات بيوكيميائية، قلل إضافة TCL1A بشدة من قدرة كل من DNMT3A وDNMT3B على ميثلة الحمض النووي، حتى في وجود DNMT3L، مؤكدةً أن التركيب البنيوي المقصود يمثل حالة مثبطة بقوة.
تغير شكلي يعرقل الإنزيم
عند التدقيق أكثر، رأى الفريق أن ارتباط TCL1A لا يجلس ببساطة فوق الموقع النشط كغطاء. بل يطلق تغييرًا دقيقًا ولكنه واسع النطاق في شكل DNMT3A. منطقتان مرنتان في الإنزيم، تعرفان بحلقة تعرف الهدف والحلقة التحفيزية، تنحرفان عن المواضع التي تشغلانها عندما يكون DNMT3A مرتبطًا بالحمض النووي. في الشكل النشط، تحتضن هاتان الحلقات الحمض النووي وتشكلان جيبًا لجزيء وقود صغير يسمى SAM، الذي يتبرع بمجموعة الميثيل. مع ارتباط TCL1A، تطوى الحلقة التحفيزية بدلًا من ذلك داخل جيب SAM وتسدّه، كما تجعل وصول الحمض النووي إلى الإنزيم أصعب. أكدت قياسات الارتباط أن DNMT3A المرتبط بـTCL1A لم يعد قادرًا على الإمساك بالحمض النووي أو بـSAM بشكل يمكن اكتشافه.
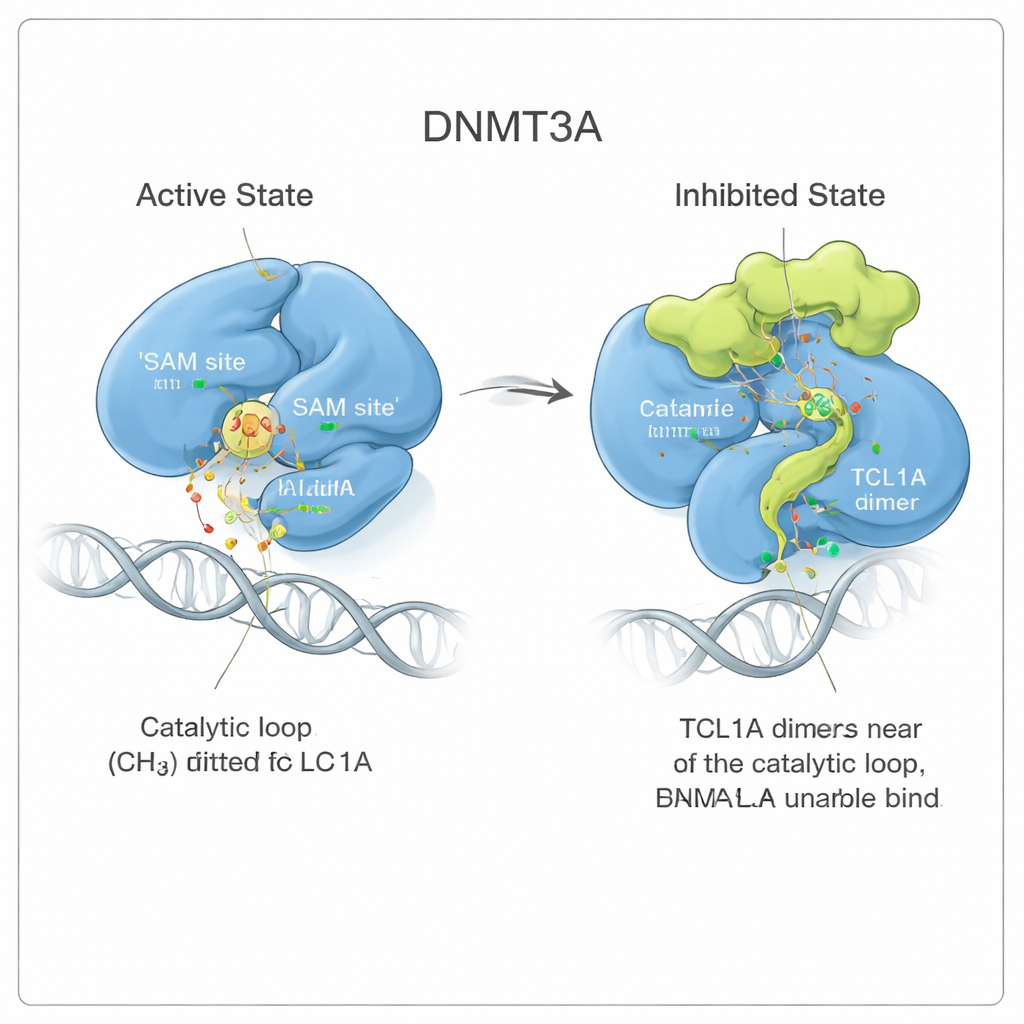
مراقبة حاجز ديناميكي في حركة
لفهم مدى ثبات هذا التشكّل المثبط، أجرا المؤلفون محاكاة ديناميات جزيئية طويلة، وهي في الأساس أفلام فيزيائية للجزيئات في المحلول. عندما كان DNMT3A مرتبطًا بمنشطه DNMT3L، بقيت الحلقة التحفيزية متماسكة في وضعها النشط. عندما تواجد TCL1A، أصبحت تلك الحلقة أكثر حركة بكثير، ترفرف حول نفسها لكنها تشغل جيب SAM بشكل متكرر كما الطحالب البحرية المتمايلة التي لا تزال تسد مصرفًا. قلّص هذا التحرك المستمر المساحة المتاحة لـSAM بأكثر من عشرة أضعاف، مما يدعم نموذجًا يستغل فيه TCL1A مرونة DNMT3A الطبيعية ليفرض شكلًا مثبطًا ديناميكيًا، لا جامدًا.
العواقب على الخلايا النامية والمرض
سأل الفريق بعد ذلك ماذا يعني هذا الحصار الجزيئي للخلايا الحقيقية. هندسوا خلايا جذعية جنينية فأرية لإنتاج TCL1A البشري خلال مرحلة تعزّز فيها الخلايا عادةً ميثلة الحمض النووي كلما بدأت بالتمايز. أظهر رسم خريطة الميثلة على مستوى الجينوم أن الخلايا التي تُفرز TCL1A بكثرة فشلت في اكتساب المستوى العالي المعتاد من ميثلة الحمض النووي، متماثلةً إلى حدٍ كبير مع الخلايا التي حُذفت فيها جينات Dnmt3a وDnmt3b معًا. نسخة طفيفة من TCL1A ترتبط بإنزيمات DNMT3 بشكل ضعيف كان لها تأثير قليل، مما يؤكد أن التفاعل الفيزيائي هو الأساس. تربط هذه النتائج الآلية البنيوية بتغيرات فوق جينية واسعة النطاق عبر الجينوم.
ما الذي يعنيه هذا للصحة
تُظهر هذه الدراسة مجتمعة كيف يمكن أن يعمل TCL1A كمكبح قوي على الإنزيمات التي تضيف علامات ميثيل جديدة إلى الحمض النووي. عبر الالتحام على واجهة حرجة، يعيد TCL1A تموضع حلقات مرنة في DNMT3A وDNMT3B بحيث لم يعد بإمكانهما الارتباط بقالب الحمض النووي أو بوقودهما الكيميائي، مما يؤدي إلى فقدان شامل لعلامات الميثلة في الخلايا. في التطور الطبيعي، قد يساعد هذا النوع من التحكم الدقيق في موازنة توقيت ومواقع إضافة الميثلة. عندما يُساء تموضع TCL1A أو يُنتج بكثرة، كما في بعض سرطانات الدم واضطرابات تكاثرية نادرة، يمكن أن يخرّ هذا الآلية برنامج الخلايا فوق الجيني. يفتح فهم هذا التفاعل بدقة ذرية الباب أمام تصميم جزيئات تُحاكي أو تُعاكس تأثيرات TCL1A، مما قد يعيد أنماط ميثلة الحمض النووي إلى مسارها الصحي.
الاستشهاد: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
الكلمات المفتاحية: ميثلة الحمض النووي, DNMT3A, TCL1A, علم التغيرات الوراثية فوق الجينية, السرطان