Clear Sky Science · ar
خفض RAD23A يطيل العمر ويخفف الأمراض في نموذج فأري لاعتلال بروتين TDP-43
لماذا يهم هذا البحث العائلات والمرضى
تتضمن العديد من أشكال الخَرَف ومرض العصبون الحركي، بما في ذلك التصلب الجانبي الضموري (ALS) والخَرَف الجبهي الصدغي (FTD)، بروتينات داخل خلايا الدماغ تتعرض لطي غير طبيعي وتتكتل وتسمم الخلايا العصبية ببطء. أحد الجناة الرئيسيين هو بروتين يدعى TDP-43، الذي يساعد عادةً في تنظيم الحمض النووي الريبي (RNA) لكنه يصبح سامًا عندما يتجمع. تطرح هذه الدراسة سؤالًا واعدًا: هل يمكننا جعل خلايا الدماغ أكثر مرونة عن طريق خفض مستوى بروتين آخر، RAD23A، الذي يشارك في كيفية تعامل الخلية مع البروتينات التالفة؟ تظهر النتائج في الفئران أن تقليل RAD23A يمكن أن يطيل العمر، ويحسن الحركة، ويقلل تلف الدماغ في نموذج مرض مدفوع بـTDP-43، مما يلمّح إلى استراتيجية علاجية جديدة.
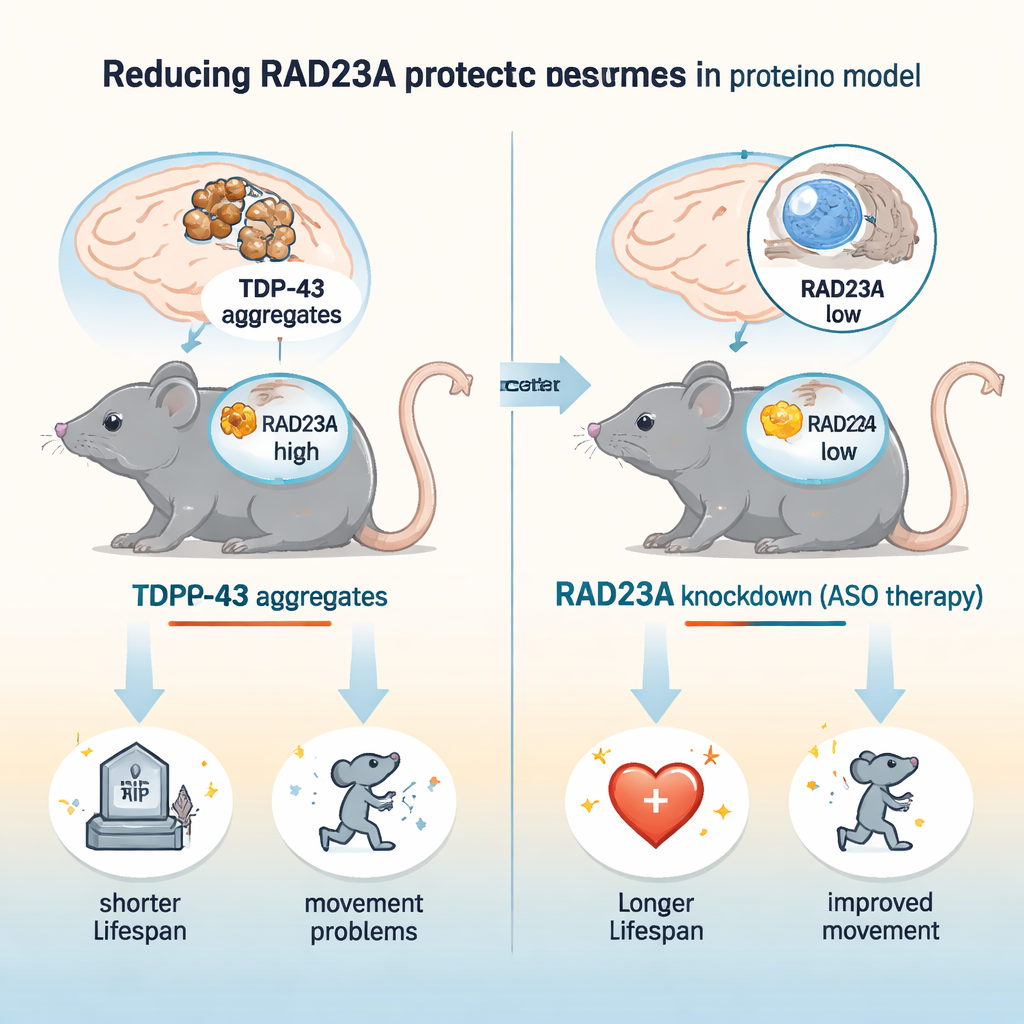
اختناق مرور البروتينات في الخلايا العصبية المريضة
غالبًا ما تُميّز الأمراض العصبية التنكسية بتراكم البروتينات المَطوية بطرق خاطئة التي يفشل جهاز التخلص من النفايات في الخلية في إزالتها. في ALS وFTD، ينتقل TDP-43 من النواة، ويكوّن تكتلات لزجة، ويُوسم بكثافة باليوبيكويتين، وهو إشارة عادةً ما توجه البروتينات إلى المُحلِّل البروتيازومي، الجهاز الرئيسي لتفكيك البروتين في الخلية. RAD23A هو واحد من عدة بروتينات «ناقلة» يمكنها حمل الحمولة الموسومة باليوبيكويتين إلى البروتيازوم. ومع ذلك، أشارت دراسات سابقة في الديدان والخلايا العصبية المزروعة إلى أن فقدان بروتينات مشابهة لـRAD23 قد يحمي بالفعل من الأذى الناجم عن TDP-43، وهو تناقض هدفت هذه الدراسة إلى استكشافه في دماغ ثديي حي.
خفض RAD23A في نموذج فأري لـTDP-43
استخدم الباحثون نموذجًا فأريًا راسخًا يُسمى TAR4/4، يزيد فيه التعبير عن TDP-43 البشري في الخلايا العصبية ويطوّر مشاكل حركة، وانحناء في العمود الفقري، ورعشة، وموتًا مبكرًا، ما يعكس سمات رئيسية لـALS/FTD. خفضوا RAD23A بطريقتين: حقن الجراء حديثي الولادة بأحماض نووية مضادة للتسلسل (ASOs) تقلل RNA لـRad23a، وتربية فئران تحمل حذفًا جينيًا لـRad23a. أدت معالجة واحدة بـASO إلى خفض مستويات RAD23A في الدماغ والحبل الشوكي بنحو ثلاثة أرباع. في هذه الفئران المصابة بتجاوز TDP-43، أدى هبوط RAD23A إلى إطالة العمر بنحو 50% وتأخير بداية وشدة مشاكل المشي والرعشة وانحناء العمود الفقري والتقاطع الخلفي للأطراف. ومن المثير للاهتمام أن الفقدان الجيني الكلي لـRAD23A لم يضف فائدة إضافية، ما يشير إلى أن الخفض الجزئي هو الأفضل وأن الغياب التام طويل الأمد قد يحرّض تغييرات تعويضية.
التهاب أقل، معالجة بروتينية أنظف، وجينوم أكثر هدوءًا
أظهر الفحص المجهري لقشرة الفص الحركي أن فئران TDP-43 فقدت خلايا عصبية وظهرت تنشيطات قوية للنجميات والميكروغليا، خلايا الدعم والمناعة في الدماغ. حافظ خفض RAD23A على عدد الخلايا العصبية وقلّل مؤشرات الالتهاب وموت الخلايا. كشفت التحليلات الكيميائية الحيوية أن الإفراط في إنتاج TDP-43 أغرق الخلايا ببروتينات موسومة باليوبيكويتين وغير قابلة للذوبان في المنظفات وسحب وحدات البروتيازوم إلى هذه التكتلات، مما أضعف قدرة الخلية على إزالة البروتينات التالفة. أدى تقليل RAD23A إلى خفض الحمل الكلي للبروتينات الميوبيكويتينة، والحفاظ على مزيد من البروتيازومات في المجموعة القابلة للذوبان والفعالة، واستعادة عدة أنواع من نشاط البروتيازوم باتجاه الحالة الطبيعية. في الوقت نفسه، خفض هبوط RAD23A كلًا من الأشكال الكلية والمتكتلة لـTDP-43، بما في ذلك قطعة سامّة بوزن 25 كيلو دالتون، وحوّل موقع TDP-43 بعيدًا عن السيتوبلازم نحو النواة. أظهر التسلسل الشامل للـRNA أن آلاف التغيرات في التعبير الجيني التي أحدثها TDP-43 انعكست جزئيًا عندما تم تقليل RAD23A، خاصةً الجينات المشاركة في وظيفة الخلايا العصبية وإنتاج الطاقة الميتوكوندرية ومسارات إزالة التكتلات مثل aggrephagy.
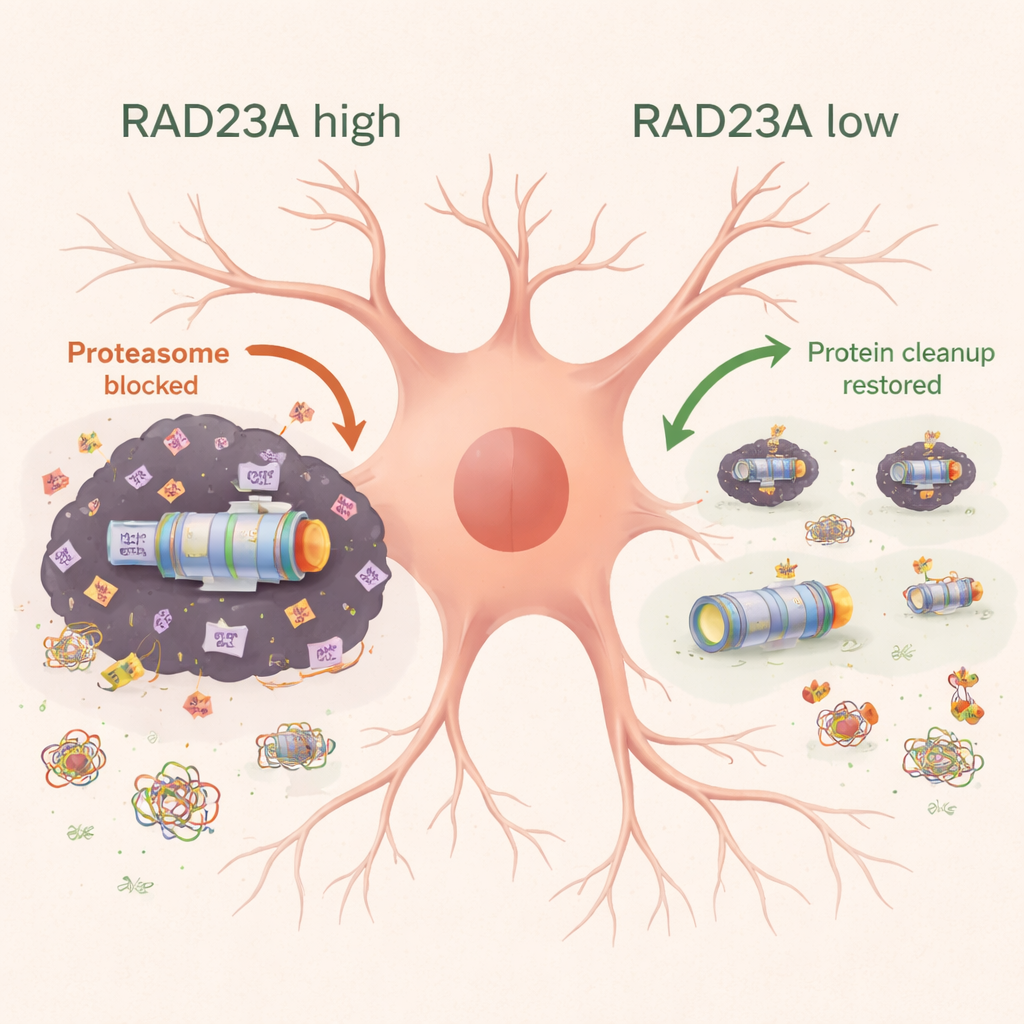
إعادة تشكيل البروتيوم «غير القابل للذوبان» الخفي
للنظر عن كثب إلى التكتلات العنيدة المقاومة للمنظفات الاعتيادية، استخدم الفريق قياس الطيف الكتلي مع نظائر ثقيلة لتسجيل البروتينات المحبوسة في الجزء غير القابل للذوبان من قشرة الفأر. جذب تعبير TDP-43 البشري مكونات البروتيازوم وبروتينات الهيكل الخلوي والنقل وآلات خلوية أخرى. عندما تم خفض RAD23A، تغيّرت التكوينات العامة لهذا البروتيوم غير القابل للذوبان: احتُجزت بروتينات مرتبطة بالبروتيازوم والنقل بدرجة أقل، في حين زادت بعض البروتينات الريبوسومية والمرتبطة بالإجهاد داخل التكتلات. ومن الجدير بالذكر أن هذا إعادة التشكيل لم تكن مجرد انعكاس لتغيرات في مستويات RNA، مما يوحي بأن RAD23A يؤثر أساسًا في كيفية توزيع البروتينات الموجودة بين الحالات القابلة للذوبان والمتجمعة، بدلًا من تحديد كمية كل بروتين المصنوع.
ماذا قد يعني هذا للعلاجات المستقبلية
تجمل هذه النتائج RAD23A كمنظِّم قوي لجودة البروتين في الخلايا العصبية تحت الإجهاد. من خلال خفض جزئي لـRAD23A في نموذج فأري محرك بـTDP-43، تمكن الباحثون من تقليل التكتلات البروتينية السامة، واستعادة نشاط جهاز التخلص من البروتينات، وتهدئة التغيرات الضارة في التعبير الجيني، والحد من التهاب الدماغ، وتمديد العمر والوظيفة الحركية. وبما أن تراكم TDP-43 غير الطبيعي واسع الانتشار في كل من الأشكال الوراثية والعشوائية لـALS وFTD والاضطرابات ذات الصلة، فقد يوفر استهداف RAD23A بأدوية مضادة للتسلسل المتوافقة مع البشر وسيلة لحماية الخلايا العصبية دون منع TDP-43 نفسه مباشرةً، إذ إنه بروتين أساسي. وبينما لا يزال الكثير للاختبار في نماذج أخرى وفي البشر، تشير هذه الدراسة إلى أن RAD23A هو هدف واعد لدخول مسار مشترك في التنكس العصبي.
الاستشهاد: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
الكلمات المفتاحية: TDP-43, التصلب الجانبي الضموري (ALS), تراكم البروتين, المُحلِّل البروتيازومي, علاج مضاد للتسلسل (antisense)