Clear Sky Science · ar
طريق طويل نحو جينومات نباتية دوائية موثوقة وكاملة
لماذا خرائط الحمض النووي للنباتات مهمة لصحة الإنسان
العديد من أقوى الأدوية الحالية — من أدوية السرطان مثل باكليتاكسيل إلى المسكنات مثل المورفين والدواء المضاد للملاريا أرتيميسينين — مصدرها النباتات. ومع ذلك، لا يزال العلماء يفتقرون إلى "دليل التعليمات" الكامل للحمض النووي لمعظم النباتات الدوائية. تستعرض هذه المراجعة كيف تغير تقنيات الجينوم الجديدة قدرتنا على قراءة هذه الأدلة، ولماذا كثير من جينومات النباتات الحالية لا تزال غير مكتملة أو معيبة، وكيف يمكن للجينومات الدقيقة حقاً أن تفتح الباب أمام أدوية أفضل وإنتاج أكثر استدامة وحفظ محسّن للأنواع القيّمة.
وعد قراءة المخططات الوراثية للنباتات الدوائية
لمدار طويلة، اعتمد الناس على العلاجات العشبية، ولا يزال علم الأدوية الحديث يستمد كثيراً من المنتجات الطبيعية النباتية. تُنتَج هذه الجزيئات المتخصصة — مثل القلويات والتربينويدات والمركبات الفينولية وغيرها الكثير — عبر مسارات أيضية معقدة مشفرة في حمض النبات النووي. حتى وقت قريب، كان على العلماء تجميع هذه المسارات باستخدام أدوات بطيئة ومكثفة بالعمل مثل تتبّع النظائر واستنساخ جين واحد في كل مرة. غيّرت تقنية تسلسل الحمض النووي عالية الإنتاجية والميسورة التكلفة المشهد. بحلول فبراير 2025، تم تسلسل جينومات 431 نباتاً دوائياً (عبر 203 أنواع)، ما منح الباحثين وسيلة منهجية للبحث عن جينات المسارات، وفهم كيفية تنظيم المركبات القيّمة، واستكشاف كيف تطورت هذه الكيميائيات.
طفرة في التسلسل، لكن كثير من الجينومات غير كاملة
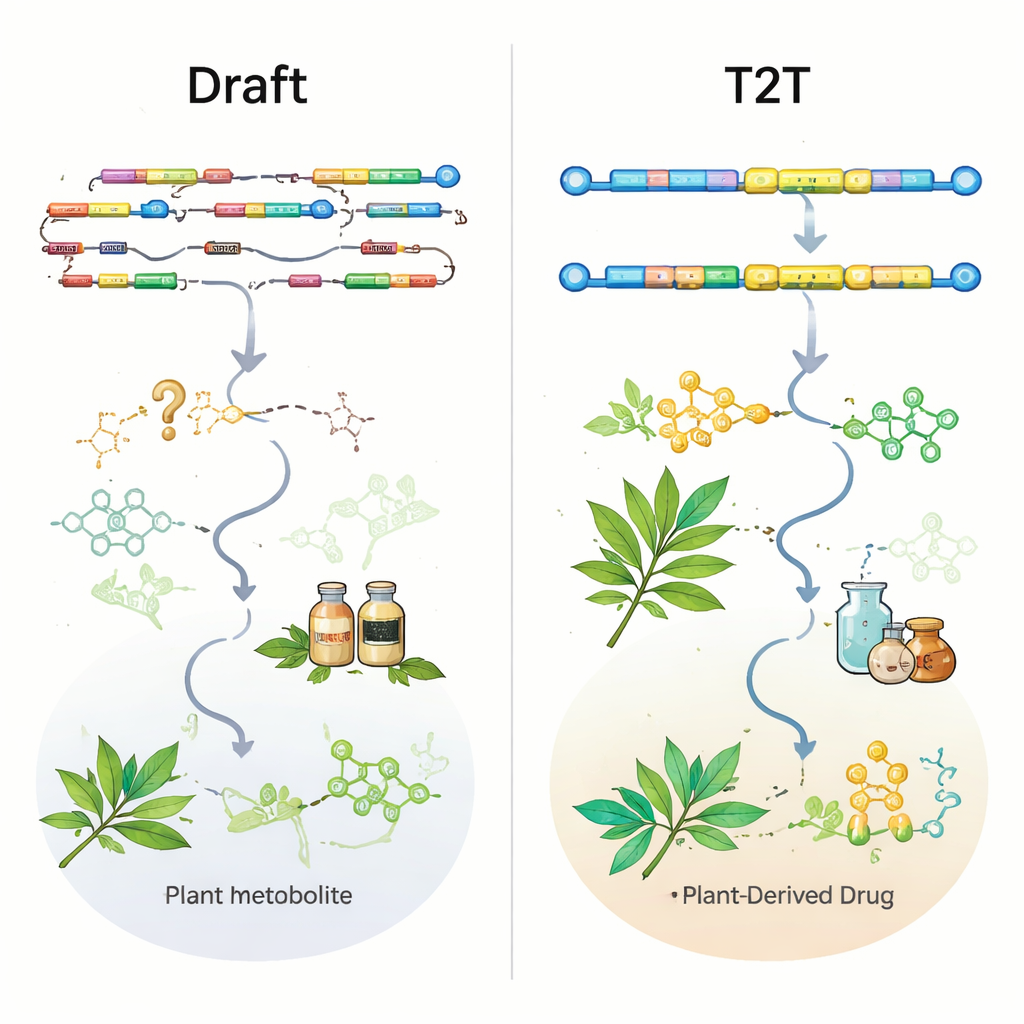
حسّنت تقنيات التسلسل طويلة القراءة من PacBio وOxford Nanopore، مقترنة ببيانات قصيرة القراءة من Illumina وأساليب رسم خرائط على مستوى الكروموسوم مثل Hi‑C، جودة جينومات النباتات بشكل كبير. نُشِرَت ما يقرب من نصف تراكيب الجينومات النباتية الدوائية في السنوات الثلاث الماضية فقط، والعديد من الجينومات الحديثة مُنشأة الآن على مقياس الكروموسوم. مع ذلك، تُظهر المراجعة أن الكم تفوّق على الكيف. أكثر من نصف الجينومات موجودة كإصدار أولي فقط، وكثير منها لا يزال على مستوى المسودة، وفقط 11 نباتاً دوائياً لديهم تراكيب "من تلومير إلى تلومير" (T2T) خالية من الفجوات تلتقط المراكز الكروموسومية والمناطق التكرارية الأخرى بالكامل. تبدو مقاييس معيارية مثل N50 (مقياس الترابط) ودرجات BUSCO (مقياس الجينات المحافظة) مبشرة عموماً، لكنها قد تخفي فجوات حرجة تحديداً حيث توجد جينات التخليق الحيوي الرئيسية.
فجوات مخفية حيث ينبغي أن تكون جينات الدواء
لاختبار مدى فائدة الجينومات الحالية فعلاً، فحص المؤلفون جينات مسارات معروفة ومؤكدة تجريبياً في تسعة نباتات دوائية مدروسة جيداً. حتى في بعض التراكيب على مستوى الكروموسوم، كانت إنزيمات مهمة لمركبات مثل الجينسينوسيدات في الجنسنغ أو الأرتيميسينين في Artemisia annua إما مفقودة تماماً أو مُلتقطة جزئياً فقط. في حالات أخرى، وُجِدت الجينات في تسلسل الجينوم الخام لكنها غائبة أو مبتورة في التعليقات الجينية الرسمية، ما يجعل العثور عليها صعباً. مثال بارز من العشبة المنتجة للكومارين Peucedanum praeruptorum: جينوم قديم على مستوى الكروموسوم كسر أحد الجينات الأساسية وفشل في اكتشاف اثنين آخرين؛ جينوم T2T أحدث لم يستعد هذه الجينات فحسب، بل كشف أيضاً أن عدة منها تقع معاً في كتلة جينية ضيقة للتخليق الحيوي. هذا النوع من خرائط الكتل بالضبط ما يحتاجه الباحثون لهندسة النباتات أو الميكروبات لإنتاج الأدوية بكفاءة أكبر.
لماذا يصعب تجميع جينومات النباتات
تطرح النباتات الدوائية تحديات خاصة تتجاوز تلك الموجودة في العديد من الأنواع الزراعية. غالباً ما تحمل جينوماتها مستويات عالية من التغاير (اختلافات حمض نووي بين النسختين من كل كروموسوم)، وتكرار الصيغة الصبغية (تعدد مجموعات الكروموسومات)، ونسباً كبيرة من الحمض النووي التكراري — وهي ميزات تشتت خوارزميات التجميع وتؤدي إلى انقطاعات أو وصلات خاطئة. حوالي ثلث النباتات الدوائية المتسلسلة تحتوي جينوماتها على أكثر من 70% محتوى تكراري، وأكثر من ربعها تظهر تغايراً عالياً جداً. قد يساعد تربية سلالات شديدة التهجين أو عزلة الأنسجة أحادية المجموعة الكروموسومية، لكن هذا بطيء ومكلف أو صعب بيولوجياً لكثير من الأنواع. بدأت استراتيجيات جديدة تجمع كل الأمبليوتيب الأبوي على حدة، وخوارزميات أقوى مضبوطة للجينومات الغنية بالتكرار والمتعددة الصيغة الصبغية، في تخفيف هذه العقبات لكنها ليست روتينية بعد.
من الجينومات إلى أدوية جديدة والتوجهات المستقبلية
عندما تكون الجينومات جيدة بما فيه الكفاية، تصبح محركات قوية للاكتشاف. يمكن للباحثين دمج بيانات الجينوم الكامل مع علم النسخ، والميتوبولوميكس، والأحياء التركيبية لتحديد الإنزيمات، وجينات التنظيم، ومجمّعات الجينات المسؤولة عن التخليق الحيوي التي تتحكم في إنتاج مركبات ذات قيمة عالية. لقد مكّنت هذه الرؤى بالفعل إعادة بناء مسارات نباتية معقدة — مثل تلك الخاصة بالفينبلاستين والباكليتاكسيل والعديد من الأدوية الأخرى — في خمائر أو نباتات نموذجية، فاتحةً طريقاً نحو التصنيع الحيوي المستقر واسع النطاق. فيما بعد، يجادل المؤلفون بضرورة التحول من نهج "جِنوم واحد تقريبي لكل نوع" إلى عدة تراكيب عالية الجودة، T2T ومحلولة حسب النمط الهابلوطيبي، تلتقط التنوع داخل النوع، على غرار البان-جينومات في أبحاث المحاصيل. ربط هذه الجينومات المرجعية بإعادة تسلسل واسعة النطاق، وفينوتيبينغ متقدم، وتقنيات النسخ المستحدثة على مستوى الخلية الواحدة والمكاني يجب أن يضيء كيف يتفاعل الوسط، ونوع الخلية، وشبكات الجينات لتشكيل الكيمياء الدوائية.
ما يعنيه هذا للمرضى والكوكب
الرسالة المركزية للمراجعة هي أن الجينومات النباتية الدوائية الموثوقة والكاملة ليست رفاهية؛ بل هي أساس تحويل قرون من المعرفة العشبية إلى علاجات حديثة دقيقة. ستساعد الجينومات الأفضل العلماء على إيجاد الخطوات المفقودة في مسارات الأدوية، وهندسة إمدادات أكثر أماناً ووفرة من الأدوية الحرجة، وتحديد أنواع بديلة يمكنها إنتاج نفس المركبات. كما سترشد حفظ الأنواع والاستخدام المستدام للنباتات الدوائية المهددة، التي لا تزال معظمها تفتقر لأي مورد جينومي. باختصار، إتمام مهمة رسم هذه الجينومات بدقة قد يسرّع اكتشاف الأدوية، ويثبت سلاسل التوريد، ويحفظ التنوع النباتي — وكل ذلك يعود بالنفع في نهاية المطاف على صحة الإنسان.
الاستشهاد: Cheng, LT., Wang, ZL., Zhu, QH. et al. A long road ahead to reliable and complete medicinal plant genomes. Nat Commun 16, 2150 (2025). https://doi.org/10.1038/s41467-025-57448-8
الكلمات المفتاحية: علم جينومات النباتات الدوائية, مجمّعات الجينات المسؤولة عن التَّخليق الحيوي, جينومات من تسارع إلى تسارع (تلومير إلى تلومير), تَّخليق المنتجات الطبيعة, الأحياء التركيبية