Clear Sky Science · ar
إلقاء الضوء على تأثير أسيتلة الطرف N: من البروتين إلى الفسيولوجيا
كيف يمكن لعلامات كيميائية صغيرة أن تغيّر سلوك البروتين
كل خلية في جسمك مليئة بالبروتينات التي يجب أن تنطوي بشكل صحيح، وتذهب إلى المكان المناسب، وتجمع لتكوّن آلات جزيئية، وأن تُزال عند تلفها. تستعرض هذه المقالة المراجعية تغييرًا كيميائيًا دقيقًا لكنه منتشر للغاية في أحد طرفي العديد من البروتينات — يُسمى أسيتلة الطرف N — وتبيّن كيف يساعد هذا «الغلاف» الصغير في التحكم بكل شيء من نمو الخلايا واستجاباتها للإجهاد إلى تطور القلب ووظيفة الدماغ.
الغلاف البروتيني الذي لم نسمع عنه معظمنا
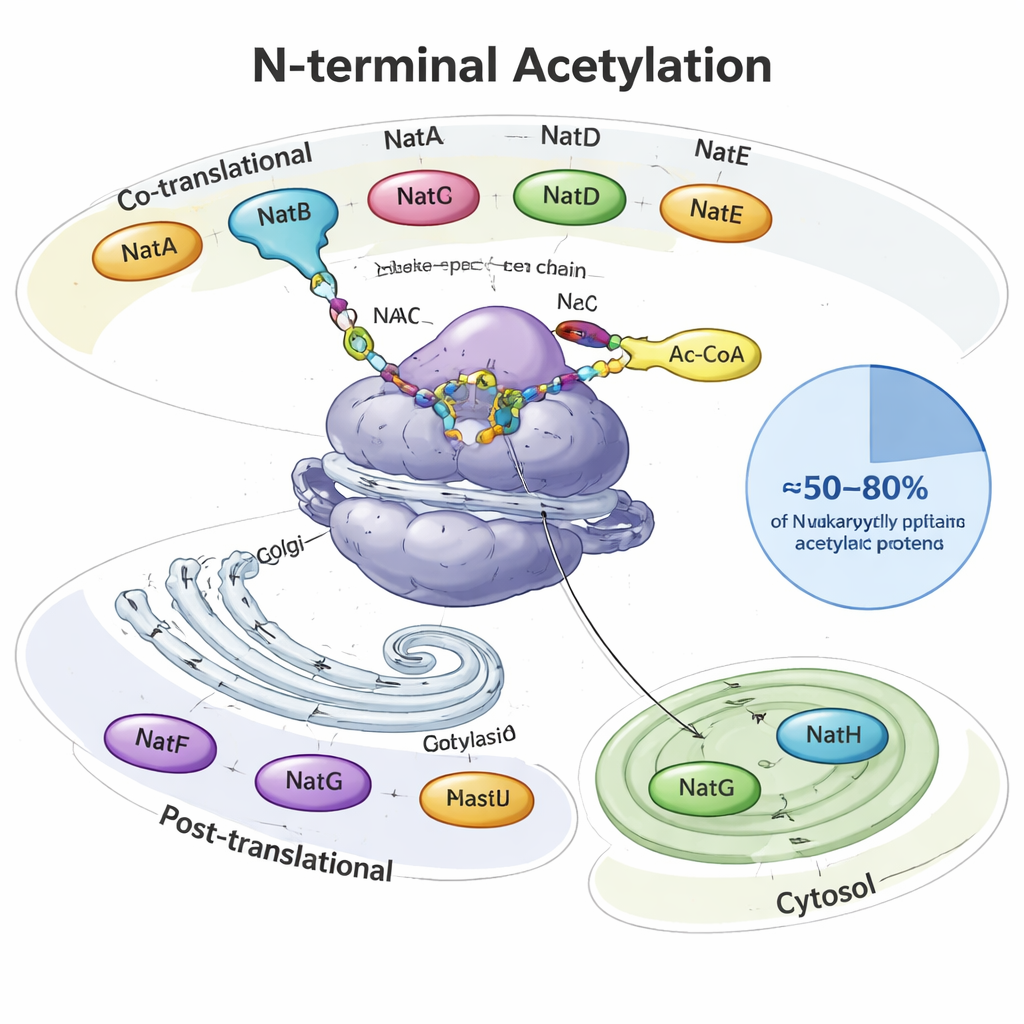
عندما يُصنَع البروتين، يخرج من مصنع البروتين في الخلية، الريبوسوم، كخيط ينمو. في بدايته تمامًا — الطرف N — تتلقى العديد من بروتينات الخلايا حقيقية النواة مجموعة أسيتيل، قبّعة صغيرة ذات ذرتي كربون. تقوم إنزيمات متخصصة تُسمى ناقلات أسيتيل الطرف N (NATs) بهذه الوظيفة، مستخدمة جزيئًا أيضيًا شائعًا (أسيتيل‑CoA) كمانح. في الخمائر والنباتات والحيوانات، تنقسم المهمة بين ثمانية أنواع رئيسية من NATs (NatA–NatH). يعمل بعضها أثناء تصنيع البروتين، بينما يعمل البعض الآخر بعده ويكون مرابطًا في مواقع محددة مثل جهاز جولجي أو البلاستيدات النباتية. معًا، تُعدِّل هذه الإنزيمات نحو نصف إلى أربعة أخماس البروتينات الخلوية، حيث يتعرف كل NAT على تسلسلات بداية مفضلة تتألف من حمضين أمينيين إلى أربعة.
العديد من الإنزيمات، كل منها بتخصصه
NatA وNatB وNatC هي الفاعلون الرئيسيون، تعمل مباشرة عند الريبوسوم وتشمل أجزاء كبيرة من «أسيتيلوم الطرف N». يمكن أن يعدِّل NatA وحده نحو 40% من بروتينات الإنسان، عادة تلك التي تُزال منها الميثيونين الأولية. يتصرف NatB وNatC على بروتينات تحتفظ بالميثيونين المبدئي، لكنهما يختلفان في الأحماض الأمينية المجاورة التي يفضلانها. أما NATs الأخرى فهى أكثر انتقائية: يركز NatD على عدد قليل من بروتينات الهيستون التي تُعقِم الحمض النووي، يستهدف NatF البروتينات الغشائية في جهاز جولجي، يعمل NatG داخل البلاستيدات النباتية، ويُكمل NatH (NAA80) عملية نضوج خاصة من خطوتين على الأكتين، المكوّن الرئيسي لهيكل الخلية. تجمع المقالة دراسات بنيوية وكيميائية حيوية تُظهر كيف تثبت وحدات مساعدة هذه الإنزيمات على الريبوسومات أو الأغشية وتضبط بدقة البروتينات التي تعمل عليها.
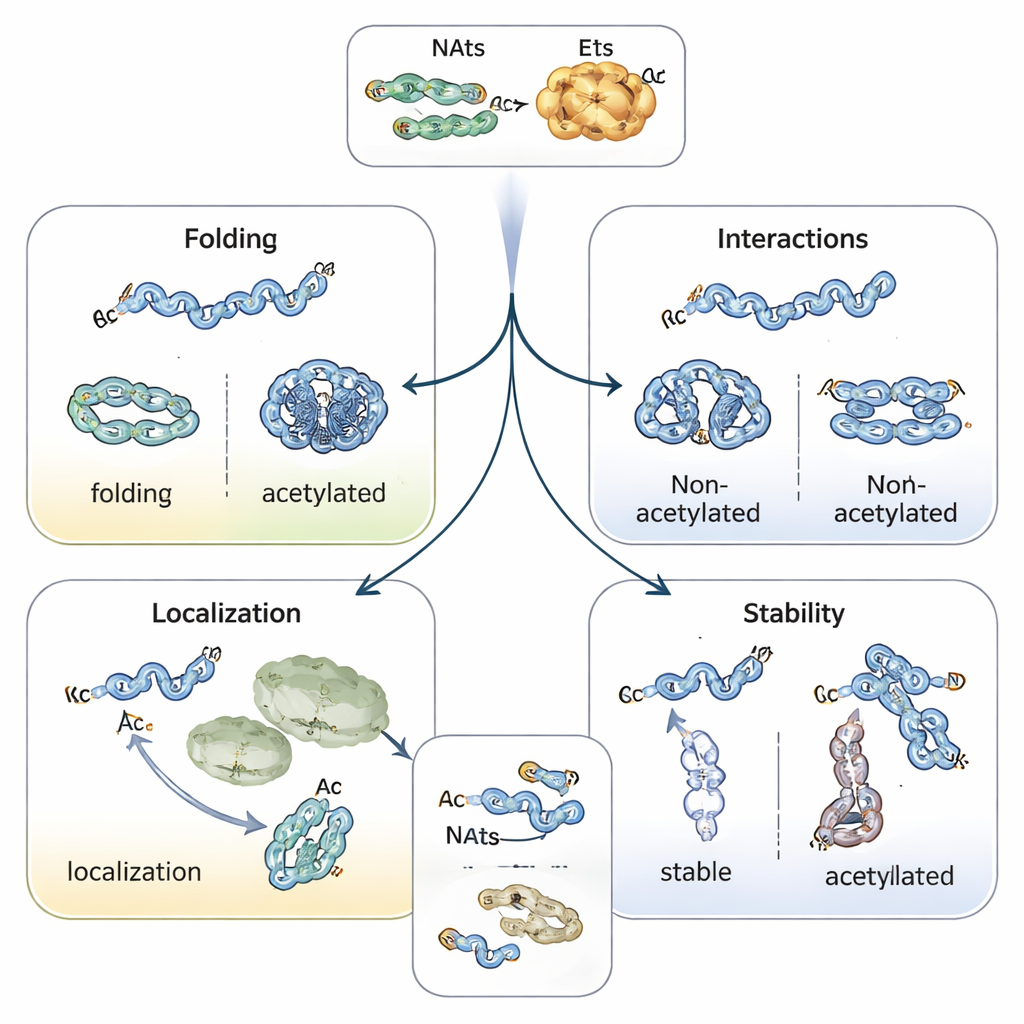
توجيه طي البروتين، موقعه وعمره
يغيّر إضافة غطاء أسيتيل الطبيعة الكيميائية لبداية البروتين، وغالبًا ما يستقرّ في تشكيلات حلزونية ويؤثر على كيفية طي البروتينات. على سبيل المثال، البروتين المرتبط بمرض باركنسون ألفا‑سينوكلين يميل إلى التجمّع أقلّ وتبني شكل أكثر أمانًا عندما يُأسّتل طرفه N. الترابوميوسين، شريك الأكتين، يرتبط وينظّم خيوط الأكتين بشكل أفضل عندما يكون مُؤسّتلًا بشكل صحيح. في النباتات والحيوانات، يمكن أن تعمل أسيتلة الطرف N كنوع من ملصق العنوان، مساعدًة البروتينات في الوصول إلى البلاستيدات، الليسوسومات أو جهاز جولجي. وربما الأبرز هو دورها في تحديد مدة بقاء البروتينات: فطرف N غير محمي يمكن أن يُقرأ كـ «إشارة تحلل» بواسطة إنزيمات وسم اليوبكويتين، بينما تُخفي الأسيتلة تلك الإشارة وتثبت البروتين — أو، في بعض الحالات، تخلق علامة شرطية يُعترف بها فقط عندما يكون البروتين مطويًا بشكل خاطئ أو ليس في المجمع الصحيح.
من فسيولوجيا الخلية إلى التطور والمرض
نظرًا لأن أسيتلة الطرف N تمس عددًا كبيرًا من البروتينات، فإن تعطيل NATs له عواقب واسعة على الكائن الحي بأكمله. يؤدي إزالة NatA أو NatB أو NatC في أنواع نموذجية غالبًا إلى عيوب تطورية شديدة، تغيُّر في استجابات الإجهاد، أو حتى موت، بينما تُحدث الإنزيمات الأكثر تخصصًا مثل NatF وNatH مشكلات أضيق مثل تكلسات الدماغ أو فقدان السمع. في البشر، تُسبِّب طفرات وراثية في عدة جينات NAT متلازمات نادرة في التطور العصبي مع تأخر ذهني، عيوب قلبية أو ضعف عضلي. تُظهر نفس الآلية نشاطًا زائدًا في كثير من الأحيان في السرطانات، حيث يرتبط ارتفاع مستويات NAT بتوقعات سيئة وقد يساهم في نمو الورم والانتشار ومقاومة العلاج. كما تؤثر التغيرات في أسيتلة الطرف N على بروتينات عرضة للتجميع مثل ألفا‑سينوكلين والهنغتين، رابطًة هذا التعديل بآليات الأمراض التنكسية العصبية.
اتجاهات مستقبلية ووعد طبي
يخلص المؤلفون إلى أنه بينما نعرف الآن معظم الإنزيمات الأساسية التي تضيف هذه الأغطية الطرفية N، لا نزال نفهم جزءًا صغيرًا فقط من الأهداف البروتينية المحددة وقواعد التنظيم. ثيمة رئيسية هي أن الأسيتلة في بداية البروتين غالبًا ما تحميه من الدمار المبكر، وفي الوقت نفسه تخلق إشارات معتمدة على السياق لمراقبة الجودة. تحديد أي لِجازات اليوبكويتين تقرأ أي أنماط طرفية N، واكتشاف ما إذا كان هناك أي إنزيم قادر على إزالة هذه الأغطية، هما أسئلتان مفتوحتان رئيسيتان. وبما أن NATs تقع عند مفترق استقرار البروتين وتنظيم الجين واستجابات الخلية للإجهاد، فإن مثبطات NAT الانتقائية — وربما أدوات مستقبلية تضبط أسيتلة الطرف N لبروتينات مرتبطة بالأمراض بعينها — تظهر كمسارات واعدة لتطوير علاجات جديدة للسرطان وأمراض القلب والتنكس العصبي.
الاستشهاد: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
الكلمات المفتاحية: تعديل البروتين, أسيتلة الطرف N, مراقبة جودة البروتين, أمراض تنكسية عصبية, بيولوجيا السرطان