Clear Sky Science · ar
متغير ZMYND11 p.Arg600Trp المرتبط بنمط مميز من الطيف النفسي العصبي النمائي
لماذا تهم هذه القصة الجينية النادرة
تواجه العديد من العائلات أطفالاً يتطورون أبطأ من المتوقع، ومع ذلك لا يحصلون على تفسير واضح. يركز هذا البحث على تغيير جيني نادر واحد، يُدعى p.Arg600Trp في جين ZMYND11، ويُظهر ارتباطه بنمط مميز من السمات النمائية والجسدية. من خلال توثيق حالة طفل متأثر بعناية ومقارنته بعشرات الحالات المبلغ عنها سابقاً عالمياً، يكشف الباحثون كيف أن تباينات طفيفة في نفس الجين يمكن أن تشكل أشكالاً مختلفة من الاضطرابات النمائية العصبية. يساعد عملهم الأطباء على التعرف على هذه الحالة مبكراً، ويوجه الإرشاد الوراثي للأسر، ويشير إلى مدى حساسية الآليات المسؤولة عن بناء الدماغ.
مريض واحد يحمل دلائل عديدة
جوهر التقرير هو صبي وُلد بحجم أقل قليلاً من المتوقع لعمر الحمل، برأس أصغر من المتوسط وضعف في توتر العضلات منذ الولادة. عانى من صعوبات في التنفس والأكل واحتاج إلى رعاية في وحدة العناية المركزة لحديثي الولادة. مع نموه، لاحظ الأطباء تأخراً نمائياً عاماً: تأخرت السيطرة على الرأس، واستغرق الجلوس المستقل أكثر من سنتين، وكان الكلام والفهم متأخرين بوضوح عن أقرانه. أظهر أيضاً ملامح وجسدية مميزة، بما في ذلك جسر أنفي عريض مع فتحات أنف واسعة، وآذان منخفضة، وحلمات غير عادية، إلى جانب قصر القامة، وخصية غير هابطة، وفتق إربي على الجانب الأيمن. أضاف سقوط المحاذاة في العين وطول النظر إلى الصورة السريرية، بينما بدت صور الدماغ من الناحية الهيكلية طبيعية.
اكتشاف التغيير الجيني
لم تفسر اختبارات الكروموسومات القياسية صعوبات الصبي. عبر المبادرة الوطنية اليابانية للأمراض النادرة وغير المشخّصة، أجرى الفريق تسلسل الإكسوم الكامل، الذي يقرأ مناطق ترميز البروتين في غالبية الجينات دفعة واحدة. كشف هذا عن تغيير حرف واحد في جين ZMYND11 يغير كتلة أمينية واحدة في الموقع 600 من البروتين. لم يُعثر على هذا التغيير في قواعد بيانات سكانية كبيرة، وكان غائباً عن كلا الوالدين، ما يعني أنه نشأ حديثاً في الطفل. أشارت أدوات الحوسبة المتخصصة في توقع تأثير هذه التغيرات إلى أنه مدمر بشكل قوي، وتُصنّف الإرشادات السريرية الدولية هذا المتغير كممرض مرضي—دليل على أنه على الأرجح سبب حالة الصبي.
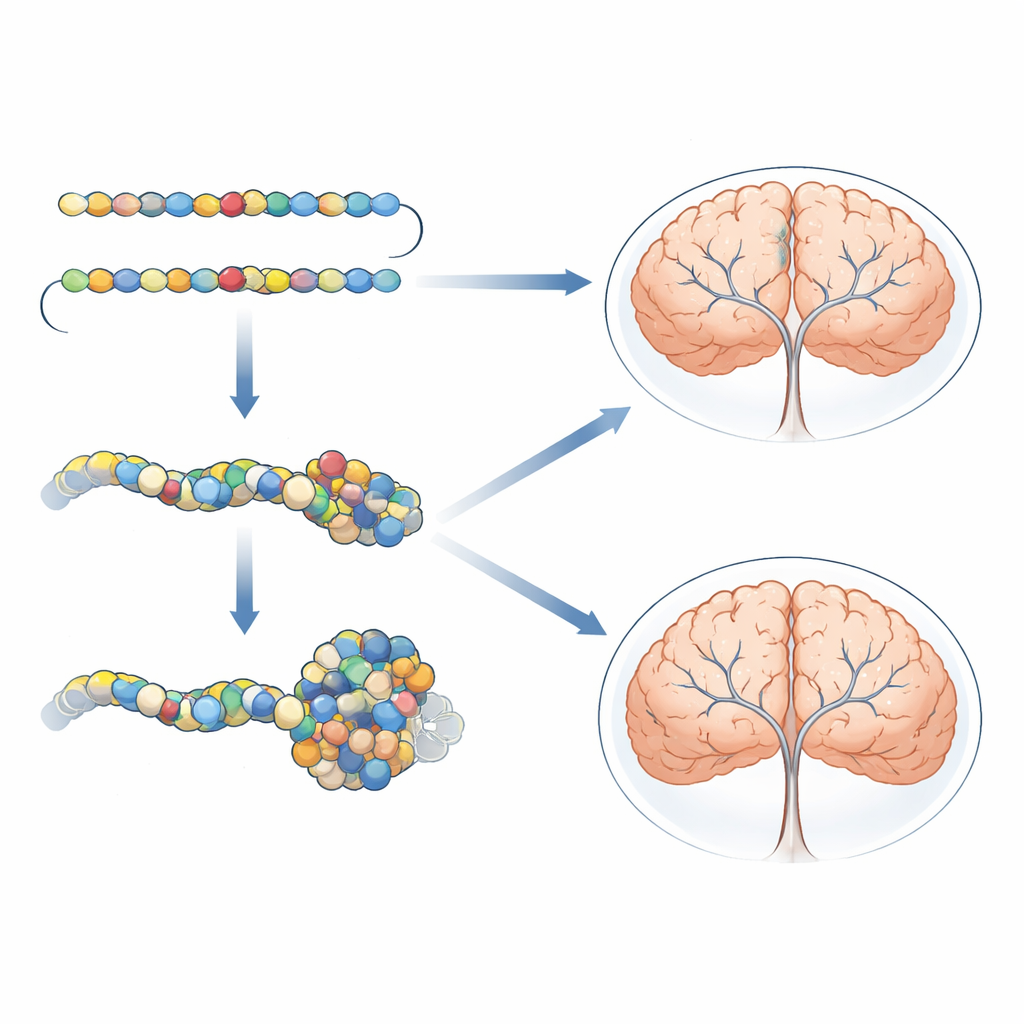
وضع طفل واحد في نمط أوسع
لفهم أهمية هذا الاكتشاف على نطاق أوسع، راجع المؤلفون الأدبيات الطبية وجمعوا بيانات من 50 شخصاً لديهم تغيرات في ZMYND11. تتضمن معظم الحالات المعروفة سابقاً متغيرات مفقودة الوظيفة، التي تعطل نسخة واحدة من الجين ويُعتقد أنها تعمل ببساطة عن طريق خفض كمية البروتين العامل. بالمقابل، حمل 13 فرداً فقط، بما في ذلك المريض الحالي، متغيرات تغيير حمض أميني (missense)، حيث يتغير البروتين دون أن يفقد تماماً. عند مقارنة السمات بين هذه المجموعات، وجدوا أن التأخر النمائي وتأخر النطق والتخلف العقلي كانت مشتركة لدى الجميع تقريباً، لكن برزت اختلافات مهمة. كان لدى الأشخاص ذوو المتغيرات من نوع missense، وخاصة الحاملين لـ p.Arg600Trp، غالباً اعتلال ذهني شديد، وانخفاض في توتر العضلات، وسقوط محاذاة العين، ورؤوس أصغر، وقصر قامة، وخصيتان غير هابطتين—وهي سمات أقل شيوعاً لدى من لديهم تغيرات تقطع البروتين.
ما التي يفعله البروتين عادة
لا يُعدّ ZMYND11 جين بنيوي للدماغ بالمعنى التقليدي؛ بل يعمل كـ«قارئ» جزيئي يربط علامات كيميائية محددة على بروتينات تغليف الحمض النووي ويساعد في ضبط نشاط الجينات بدقة. يحتوي على عدة مناطق مترابطة، بما في ذلك منطقة تُدعى مجال MYND، الذي يستخدم الزنك للحفاظ على شكله ولتجنيد بروتينات تنظيمية أخرى. أظهرت دراسات مخبرية في الفئران أن فقدان ZMYND11 يعرقل كيفية توليد ونضج الخلايا العصبية خلال التطور المبكر. يقع التغيير p.Arg600Trp في هذا المجال الحيوي MYND عند موضع معروف بأهميته في ربط جزيئات الشريك. يقترح المؤلفون أن هذا الاستبدال الأحادي للحمض الأميني قد يشوّه طريقة تجمع ZMYND11 مع فريقه الجزيئي، لا بمجرد خفض نشاطه وإنما ربما بتحريفه، مما يؤدي إلى نمط من الأعراض يختلف عن فقدان الجين البسيط.
ماذا يعني هذا للعائلات والبحث المستقبلي
بالنسبة للعائلات، يؤكد هذا البحث أن تشخيصاً جينياً محدداً يمكن أن يحول مجموعة محيرة من الأعراض إلى حالة مسمّاة ومفهومة، حتى عندما تكون الحالات المعروفة قليلة عالمياً. يُظهر العمل أن التغيير p.Arg600Trp في ZMYND11 يميّز مجموعة صغيرة لكن قابلة للتعرف من الاضطراب النمائي العصبي بسمات نمو ووجهية وتناسلية متسقة. بالنسبة للعلماء، يثير ذلك احتمال أن بعض متغيرات missense في جينات التنظيم قد تعمل عبر آليات أكثر تعقيداً من مجرد إيقاف الجين. سيستلزم تأكيد ذلك مزيداً من الحالات والتجارب المخبرية، لكن الرسالة لغير المتخصصين واضحة: التغيرات الطفيفة في آليات التحكم الجينومية يمكن أن تتسع لتطال الدماغ والجسم النامي، وتوثيق المرضى النادرين بعناية أمر أساسي لكشف هذه الروابط الخفية.
الاستشهاد: Yoshimatsu, H., Kido, J., Sawada, T. et al. ZMYND11 p.Arg600Trp variant associated with a distinctive neurodevelopmental phenotype. Hum Genome Var 13, 7 (2026). https://doi.org/10.1038/s41439-026-00339-1
الكلمات المفتاحية: اضطراب نمائي عصبي, ZMYND11, متغير جيني, تخلف عقلي, مرض نادر