Clear Sky Science · ar
مثيلة الرنا m6A تعدّل الاستجابة المضادة للفيروسات في داء الزُلاَر
عندما يتعاون فيروس والغلوتين
غالبًا ما يُنظر إلى داء الزُلاَر كمسألة غذائية بسيطة: تناول الغلوتين ويصيبه الضرر في الأمعاء. تُظهر هذه الدراسة قصة أعمق، حيث يعمل نوع شائع من فيروسات الأمعاء وعلامة كيميائية صغيرة على جزيئات الرنا معًا لدفع جهاز المناعة نحو تلف طويل الأمد. قد يساعد فهم هذه الطبقة الخفية من الضبط في تفسير لماذا يصاب بعض الناس فقط بداء الزُلاَر ويشير إلى علاجات جديدة تتجاوز النظام الغذائي الخالٍ من الغلوتين. 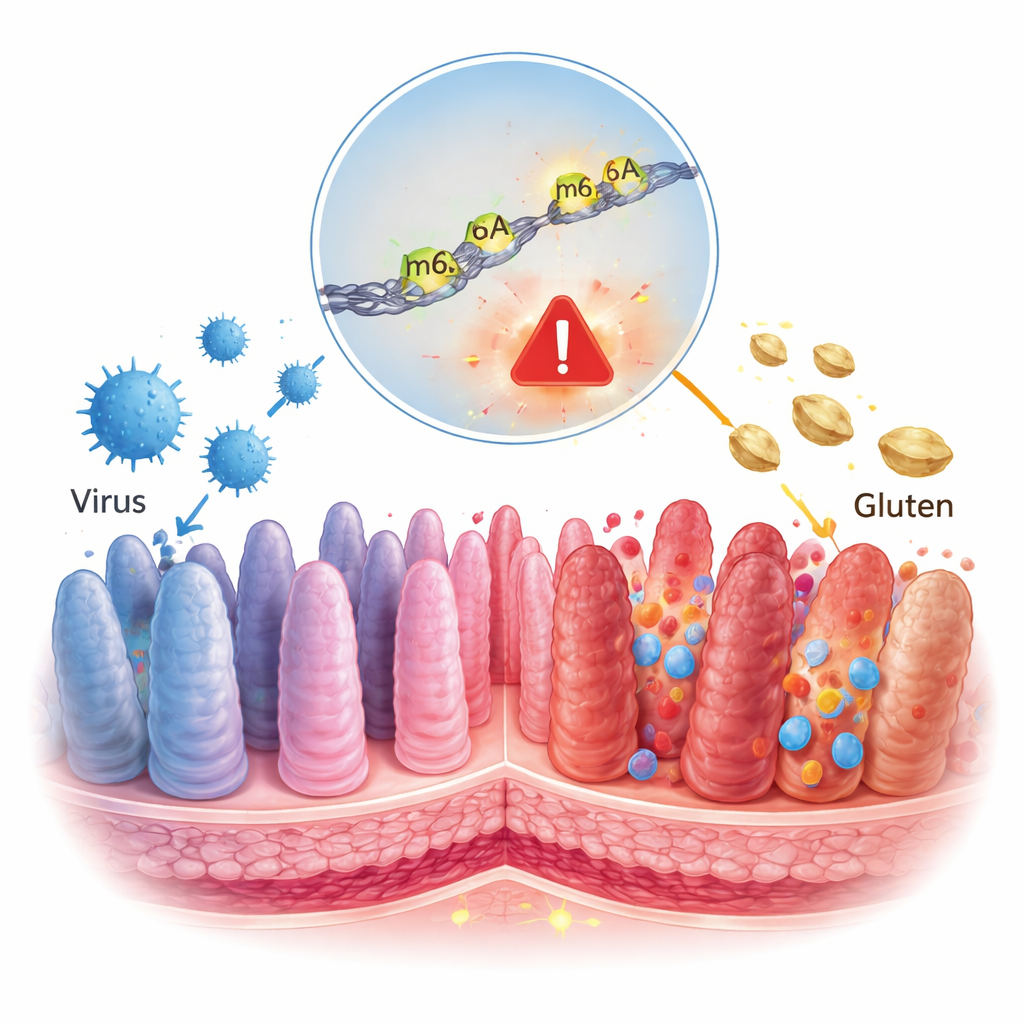
علامة خفية على رسائلنا الجينية
تقرأ خلايانا الجينات باستمرار وتنسخها إلى رنا، رسائل قصيرة تخبر الخلية ما البروتينات التي تصنعها. هذه الرسائل ليست ثابتة؛ يمكن تزيينها بعلامات كيميائية تعمل كأقلام تمييز، تغيّر مدى قراءة الرسالة. إحدى أكثر هذه العلامات شيوعًا تُسمى m6A، تغيير طفيف في أحرف الرنا. تُعرف الفيروسات بأنها تغير هذه العلامات على الرنا في الخلايا المصابة، وكان عمل سابق قد ربط بالفعل m6A بالطريقة التي يثير بها الغلوتين الالتهاب في أمعاء مرضى الزُلاَر. تساءل مؤلفو هذه الورقة عمّا إذا كان التغير الذي يُحدثه الفيروس في m6A يمكن أن يساعد في قلب جهاز المناعة من التسامح الغذائي إلى الهجوم.
دليل من مرضى داء الزُلاَر
نظر الباحثون أولاً إلى عينات دم وخزعات معوية من أشخاص يعانون من داء الزُلاَر النشط ومن ضوابط غير مصابين بالزُلاَر. وجدوا أن مرضى الزُلاَر لديهم مستويات أعلى من الأجسام المضادة ضد الفيروس العائد للريوفيروس (reovirus)، وهو فيروس رنا مزدوج الشريط يصيب الأمعاء، مما يشير إلى تعرض متكرر أو أقوى. في نسيج الأمعاء لهؤلاء المرضى، كانت جينات التحذير المضادة للفيروسات، وخصوصًا جين يسمى IRF7، مفعلة بمستويات أعلى، إلى جانب جزيئات التهابية مثل STAT1 وجاذب خلايا المناعة CXCL10. في الوقت نفسه، كانت الآلية التي تضيف وتقرأ علامات m6A أكثر نشاطًا، وكانت مستويات m6A الإجمالية على الرنا أعلى. ارتفعت وانخفضت تعابير الجينات المضادة للفيروسات مع جينات مرتبطة بـ m6A، مما يوحي أن نفس نظام الضبط قد يدير كلًّا من الدفاع ضد الفيروسات والضرر المناعي الذاتي.
كيف يضخم الغلوتين إنذار الفيروس
لاستكشاف السبب والنتيجة، بنى الفريق نموذجًا شبيهًا بداء الزُلاَر في خلايا معوية مزروعة في المختبر. حاكى الباحثون عدوى فيروسية باستخدام رنا مزدوج الشريط اصطناعي، ثم أضافوا شظايا غلوتين مهضومة شبيهة بتلك التي تظهر في الأمعاء بعد وجبة. وحده المحاكٍ الفيروسي عزّز كلًا من IRF3 وIRF7، مفتاحي التشغيل الرئيسيين للاستجابات المضادة للفيروسات. لكن عند إضافة الغلوتين بعد ذلك، أظهر IRF7 دفعة إضافية قوية، بينما لم يزد IRF3. اكتشف الباحثون أنه في هذه الظروف زادت علامات m6A على منطقة محددة داخل رنا IRF7، وأن هذا الرنا تفاعل فعليًا مع إنزيم كاتب m6A (METTL3) وإنزيم مَالِح (ALKBH5) يَحذف العلامات. رفع m6A، إما بإضافة مزيد من METTL3 أو بتقليل ALKBH5، أدى إلى ارتفاع مستويات IRF7 أكثر، رابطًا التآزر بين الغلوتين والفيروس مباشرةً بتعديل الرنا هذا. 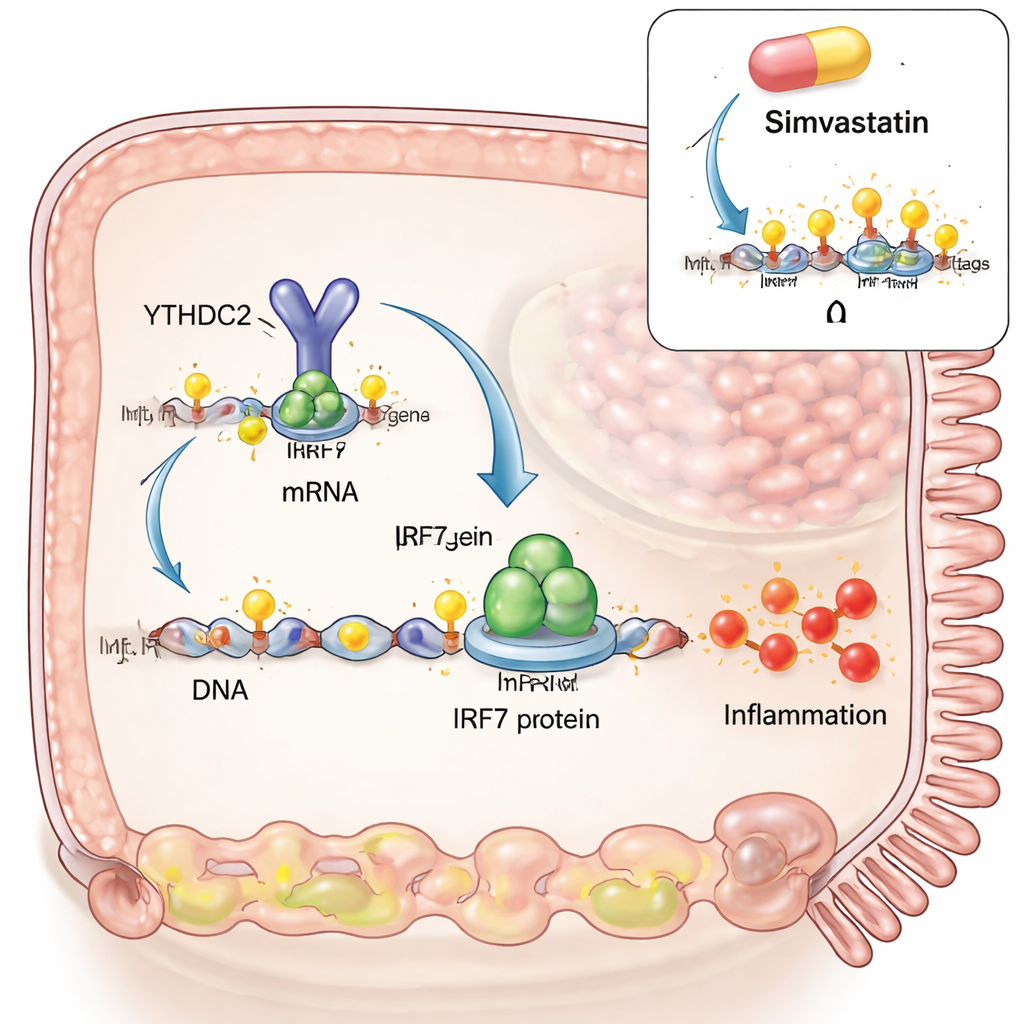
الوسيط الجزيئي ودواء مُفاجِئ
بعد ذلك، سأل المؤلفون كيف تغيّر علامات m6A على رنا IRF7 سلوك الخلية فعليًا. هندسوا نسخة من رنا IRF7 لها نفس شفرة البروتين لكن بدون مواقع m6A. أنتج هذا الرنا كميات مماثلة من النسخ، لكن بروتين IRF7 كان أقل بكثير، وفشل في تحفيز الجينات الالتهابية اللاحقة مثل STAT1 وCXCL10. كانت الحلقة المفقودة بروتين قارئ يدعى YTHDC2، الذي يرتبط عادةً بـ m6A داخل منطقة ترميز البروتين ويساعد على دفع الترجمة الفعّالة إلى بروتين. بدون مواقع m6A، لم يعد بإمكان YTHDC2 الالتحام برنا IRF7. أدى حجب كاتب m6A METTL3 في نموذج الخلية إلى خفض بروتين IRF7 وCXCL10، مما قلل المخرجات الالتهابية. كما أن دواءً لتخفيض الكوليسترول، سيمفاستاتين، الذي أُظهر مؤخرًا أنه يقلّل m6A في أنسجة أخرى، خفّض أيضًا m6A على رنا IRF7، وخفّض بروتين IRF7 في الخلايا، وكبح جينات مرتبطة بـ IRF7 في خزعات أمعاء مرضى الزُلاَر المأخوذة حديثًا وزرعت خارج الجسم. أشارت مقارنات واسعة النطاق لتعبير الجينات إلى أن السيمفاستاتين يدفع نسيج مرضى الزُلاَر نحو نمط أقرب إلى نمط المرضى المتبعين نظامًا غذائيًا خاليًا من الغلوتين.
ماذا يعني هذا لمرضى داء الزُلاَر
تصور هذه الورقة مشهدًا تتعاون فيه عدوى معوية والغلوتين على طبقة دقيقة من ضبط الرنا. في الأشخاص المعرّضين، يبدو أن العدوى الفيروسية تعزز وسم m6A لرنا IRF7 في الخلايا المعوية. ثم يضاعف التعرض للغلوتين هذه الإشارة الموسومة، مما يؤدي إلى مزيد من بروتين IRF7، وإنذارات مضادة للفيروسات أقوى، ومستويات أعلى من الرسائل الالتهابية التي تساعد في دفع الهجوم المناعي الذاتي على بطانة الأمعاء. عبر تقليل علامات m6A—إما وراثيًا أو بدواء مثل السيمفاستاتين—يمكن تليين سلسلة التفاعلات هذه، على الأقل في نماذج المختبر والخزعات خارج الجسم. للقراء العامين، الرسالة الأساسية هي أن داء الزُلاَر ليس مجرد ما تأكله، بل أيضًا كيف تشكّل العدوى والعلامات الكيميائية الدقيقة على الرنا قرار جهاز المناعة بالتسامح أو الهجوم. قد يكمل استهداف هذه العلامات الرنوية يومًا ما النظام الغذائي الخالي من الغلوتين ويستنسخ علاجات جديدة لطيف أوسع من أمراض المناعة الذاتية.
الاستشهاد: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
الكلمات المفتاحية: داء الزُلاَر, مثيلة الرنا, المناعة المضادة للفيروسات, IRF7, سيمفاستاتين