Clear Sky Science · ar
CRISPR-AuNP: التحسين الفيزيائي-الكيميائي لمنصة جسيمات ذهبية نانوية للحرَف الجيني غير الفيروسي منخفض التكلفة وقابل للتعديل في الخلايا الجذعية المكونة للدم
توسيع إمكانات التحرير الجيني ليصل إلى مزيد من المرضى
أدوات التحرير الجيني مثل CRISPR قد غيّرت بالفعل حياة أشخاص مصابين بأمراض وراثية دموية، لكن العلاجات لا تزال مكلفة وتتطلب مهارة تقنية عالية ومحصورة إلى حد كبير في عدد قليل من المراكز المتخصصة. يصف هذا البحث طريقة جديدة لإيصال CRISPR إلى الخلايا الجذعية المكونة للدم باستخدام جزيئات صغيرة قائمة على الذهب يمكن خلطها على طاولة المختبر خلال بضع ساعات فقط. الهدف هو جعل تقنيات التحرير الجيني القوية أبسط وأرخص وأسهل التطبيق في مزيد من الأماكن حول العالم.
لماذا تهم الخلايا الجذعية الدموية
تعيش الخلايا الجذعية والمناشئة المكونة للدم في نخاع العظم وتُجدّد باستمرار كل أنواع خلايا الدم المختلفة في الجسم. إذا تمكن الأطباء من تصحيح الطفرات المسببة للأمراض في هذه الخلايا بشكل آمن، فقد يوفر علاج لمرة واحدة شفاءً مادياً لحالات مثل فقر الدم المنجلي وبعض عيوب الجهاز المناعي. اليوم، تعتمد الطريقة الأكثر شيوعًا لإدخال CRISPR إلى هذه الخلايا على التحريض الكهربي (electroporation)، وهو إجراء يستخدم نبضات كهربائية لفتح ثقوب مؤقتة في أغشية الخلايا. ورغم قوته، فإن التحريض الكهربي قاسٍ على الخلايا ويتطلب معدات مكلفة ومواد كيميائية متخصصة، وليس من السهل توسيعه أو نقله إلى بيئات محدودة الموارد. الناقلات الفيروسية الأكثر أمانًا ممتازة لكثير من علاجات الجينات، لكنها أقل ملاءمة لتوصيل CRISPR لأنها تستمر في إنتاج أدوات التحرير لفترة طويلة، مما يزيد من خطر التغييرات غير المستهدفة.
بناء ناقل توصيل ذهبي صغير
سعى الباحثون إلى تحسين نظام الجسيمات النانوية الذهبية المبلغ عنه سابقًا والذي حمل مكونات CRISPR على سطحه. في التصاميم السابقة، كانت الرنا الموجهة التي تقود بروتين القص المرتبط بـCRISPR مرساة مباشرة على اللب الذهبي ثم تُقرن مع بروتين Cas9. أدى هذا إلى عمل معقول لنوع واحد من إنزيمات CRISPR لكنه أدنى أداءً مع Cas9، الذي يعد محورياً في العديد من الاستراتيجيات العلاجية. من خلال فحص دقيق لسلوك Cas9 ورناته الإرشادية في الظروف الحمضية المستخدمة أثناء تجميع الجسيمات، اكتشف الفريق أن ثنائي الرنا الإرشادي أصبح غير مستقر على السطح الذهبي، مما أدى إلى وجود قليل أو لا وجود لبروتين Cas9 النشط المرتبط بالجسيمات. كما أشارت الميكروسكوبية الكونفوكالية إلى أن الطلاء البوليمري المصمم لمساعدة الجسيمات على الهروب من الحويصلات الخلوية تقشر قبل أن يؤدي وظيفته.
إعادة تصميم تدريجية للمنصة
لتجاوز هذه المشكلات، أعاد العلماء بناء النظام من الأساس على ثلاث مراحل. أولاً، بدلاً من تثبيت رنا عاري على الذهب ثم إضافة البروتين، شكّلوا مجمعات ريبونوبروتينية CRISPR كاملة (البروتين مع الرنا الإرشادي) قبل تقريبها من السطح الذهبي. حددوا حالة حمضية طفيفة سمحت لهذه المجمعات بالارتباط بالجسيمات مع الحفاظ على نشاط بروتين القص. بعد ذلك، قاموا بتغليف الجسيمات المحملة ببوليمرات مصممة خصيصًا تجمع بين سلاسل موجبة الشحنة—اللازمة للهروب من الحويصلات—ومقاطع بولي إيثيلين جليكول مرنة محبة للماء تمنع التكتل. من خلال قياس الحجم والشحنة السطحية ومحتوى البروتين، أظهروا أنهم قادرون على تحميل عشرات مجمعات CRISPR لكل جسيم بشكل متكرر مع الحفاظ على الثبات في المحلول.
اختراق دفاعات الخلية
حتى مع تحميل أفضل، ظل الجيل الثاني من الجسيمات يواجه عقبة رئيسية: إخراج CRISPR من الحويصلات الداخلية للخلية إلى الجزء الذي يعيش فيه الحمض النووي. لذلك قام الفريق بضبط كيمياء الطبقة البوليمرية ونسبة المجموعات الموجبة على البوليمر إلى المجموعات السالبة على مجمع CRISPR بشكل منهجي. اكتشفوا أن إضافة المزيد من سلاسل البولي إيثيلين جليكول القصيرة وعدد مضبوط من المراسي المحتوية على الكبريت حسّنت كلًا من ثبات الجسيمات والقدرة على تعطيل أغشية الإندوزوم دون إلحاق ضرر بالخلايا. في التصميم النهائي للجيل الثالث، أنشأوا أولاً مجمعات مدمجة من CRISPR والبوليمر، ثم ربطوها بنوى ذهبية مركزة. أظهرت الميكروسكوبية الإلكترونية غلافًا رقيقًا من CRISPR والبوليمر حول كل كرة ذهبية، وأكد التصوير في خلايا جذعية حية أن الحمولة قادرة على الهروب إلى داخل الخلية والوصول إلى النواة.
نتائج التحرير عبر أدوات CRISPR متعددة
لاختبار مدى فعالية الجسيمات المحسنة، استهدف الباحثون جينًا يسمى بيتا-2-ميكروغلوبولين، الذي ينتج بروتينًا يوجد على سطح ما يقرب من جميع خلايا الدم ويمكن قياسه بسهولة بواسطة التدفق الخلوي (flow cytometry). باستخدام منصتهم الذهبية من الجيل الثالث، حققوا أكثر من 10% تعطيلات دقيقة لهذا الجين في الخلايا الجذعية والمناشئة الدموية البشرية الأولية—نِسَب تُعتبر ذات معنى للعديد من التطبيقات العلاجية—مع الاحتفاظ ببقاء خلايا عالٍ. على الرغم من أن هذه الكفاءة أقل مما يمكن تحقيقه بالتحريض الكهربي، فإن النظام الذهبي لم يتطلب معدات متخصصة وتسبب إجهادًا ضئيلًا للخلايا. والأهم أن نفس المنصة يمكن استخدامها مع بروتينات CRISPR مختلفة، بما في ذلك Cas9 وCas12a وإنزيم أحدث يسمى Cas12a-M29-1، مع مستويات تحرير مماثلة ولا سُمية قابلة للكشف، مما يبرز الطابع الوحدوي للتصميم.
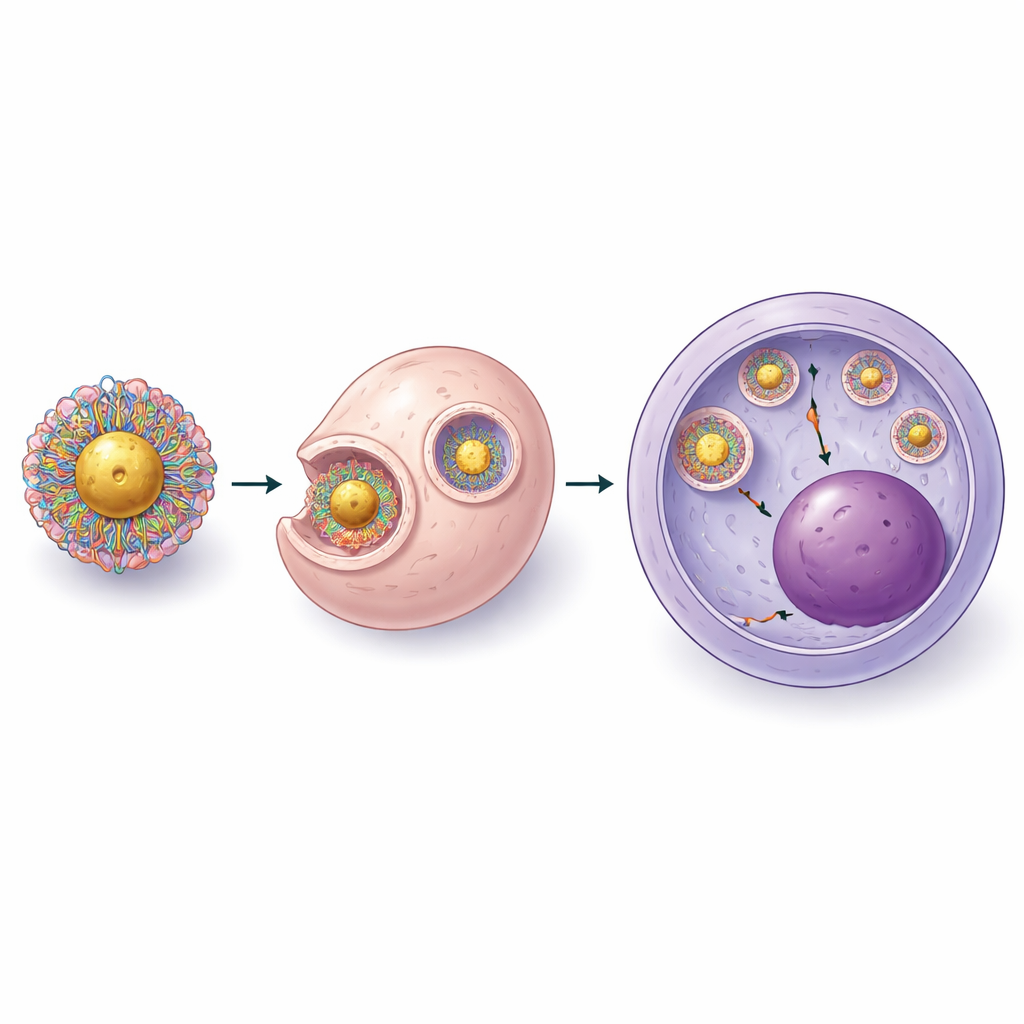
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه العملة أنه من الممكن بناء ناقل صغير ومدروس بعناية قائم على الذهب يمكنه إدخال أدوات CRISPR إلى خلايا جذعية دموية حساسة دون كهرباء أو فيروسات، باستخدام مواد جاهزة من السوق بتكلفة تقل عن سبعين دولارًا لكل مليون خلية. وبينما ما يزال ثمة حاجة إلى تحسينات إضافية لمضاهاة كفاءة أفضل الأساليب السريرية الحالية، خاصة للأمراض التي تتطلب مستويات عالية جدًا من الخلايا المصححة، تخفّض هذه المنصة المركبة على الطاولة الحواجز العملية أمام إجراء تحرير جيني متقدم. مع مزيد من الصقل واختبارات السلامة، قد تساعد مثل هذه الجسيمات النانوية في نشر فوائد العلاجات القائمة على CRISPR إلى ما بعد المراكز المتخصصة، مما يجعل العلاجات الشافية أكثر إمكانية للمرضى حول العالم.
الاستشهاد: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
الكلمات المفتاحية: التحرير الجيني بواسطة CRISPR, الجسيمات النانوية الذهبية, الخلايا الجذعية المكونة للدم, نقل غير فيروسي, الطب النانوي