Clear Sky Science · ar
المرافِقون الاصطناعيون: من التصاميم التقليدية إلى الأنظمة الذكية
مساعدة الجزيئات على الطي بشكل صحيح
داخل كل خلية حية، يجب أن تنحني وتلتف سلاسل طويلة من البروتينات والمواد الوراثية لتتخذ الأشكال المناسبة لتعمل بشكل صحيح. عندما يحدث طي خاطئ، يمكن أن تتجمع هذه السلاسل مع بعضها وتفقد وظائفها، وحتى تحفز أمراضًا مثل التنكس العصبي. تعتمد الطبيعة على جزيئات «مرافِق» لتنظيم هذا الفوضى المجهرية، لكن هذه المساعدات الطبيعية مكلفة وهشة ويصعب استخدامها خارج الخلايا. يعرض هذا المقال كيف يبني العلماء اليوم مرافِقين اصطناعيين—مساعدين مهندسين يمكنهم إقناع الجزيئات الضالة بالعودة إلى شكلها الصحيح ويمكن تشغيلهم وإيقافهم مثل أدوات ذكية.
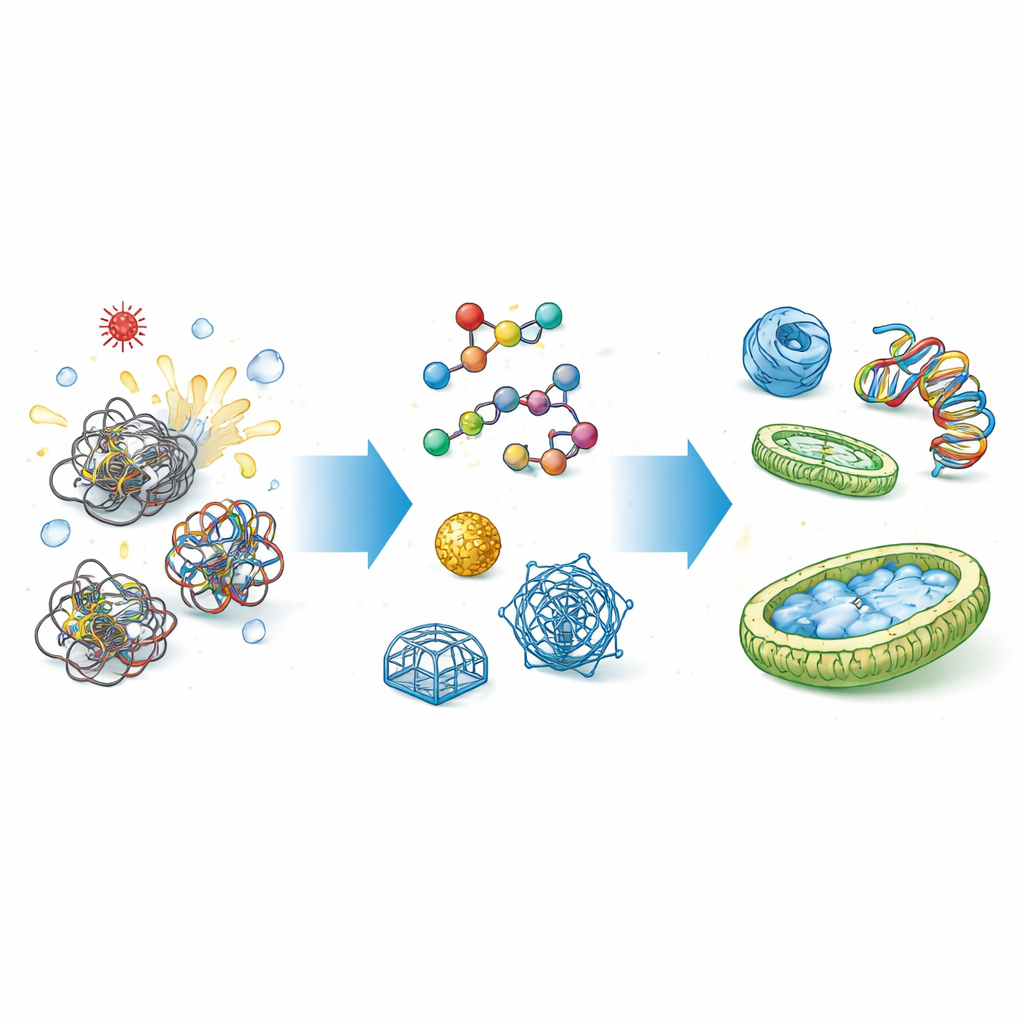
لماذا تحتاج الخلايا إلى مساعدي الطي
البروتينات والأحماض النووية (مثل DNA وRNA) لا تولد جاهزة؛ بل يجب أن تطوى إلى أشكال ثلاثية الأبعاد معقدة. الطريق إلى تلك الأشكال مليء بالمطبات، حيث قد تعلق السلاسل أو تلتصق ببعضها. تقوم المرافِقات الطبيعية، مثل بروتينات الصدمة الحرارية، بالإمساك بهذه السلاسل الرخوة، وتغطية مناطقها اللاصقة، ومنحها مساحة محمية لتطوى بشكل صحيح. وتلعب المرافِقات أدوارًا موجهة مماثلة للأحماض النووية، حيث تساعد على فك العقد وإعادة ترتيب أزواج القواعد. عندما يفشل هذا التحكم، تكون النتيجة فقدان الوظيفة، وتكوين رواسب سامة، وأمراض، وإخفاقات مكلفة في الإنتاج الصناعي للبروتينات.
من المواد الكيميائية البسيطة إلى البوليمرات المصممة
كانت المرافِقات الاصطناعية الأولى عبارة عن مواد كيميائية بسيطة تغير كيفية شعور الجزيئات ببيئتها. بعض المذيبات والمواد الخافضة للتوتر السطحي يمكن أن تخفي المناطق اللاصقة على البروتينات، وتمنع التكتل، وتمنحها فرصة ثانية لإعادة الطي. تساعد بعض الأحماض الدهنية الصغيرة، على سبيل المثال، اشتقاقات الكولاجين على الطي بشكل أكثر صحة وتخفف الإجهاد داخل الخلايا المتأثرة بأمراض وراثية. لكن هذه المساعدات الكيميائية عادةً ما تحتاج إلى جرعات عالية، ويصعب ضبطها لاستهداف محدد، وقد تزعج مكونات أخرى في خليط معقد. للحصول على مزيد من التحكم، اتجه الباحثون إلى بوليمرات أكبر مصممة خصيصًا—سلاسل مرنة يمكن تزيينها بفروع مشحونة أو محبة للماء لاحتضان DNA وRNA والبروتينات بشكل أكثر انتقائية.
طقم أدوات البوليمرات والنانوجل
يمكن للبوليمرات المصممة أن تلتصق بالهياكل الخلفية المشحونة للـDNA أو بالبقع المكشوفة على البروتينات، ملسّيةً مشهد الطاقة بحيث تجد هذه الجزيئات أشكالها المفضلة بشكل أسرع وأكثر موثوقية. بالنسبة للأحماض النووية، يمكن للبوليمرات الكاتيونية (الموجبة الشحنة) أن تلغي تنافر الشحن بين الشُرَيطين، مسرعةً اقتران القواعد، وتبادل الشرائط، وتشكيل الهياكل الغريبة المستخدمة في الحوسبة القائمة على DNA وأجهزة الاستشعار الحيوية. بالنسبة للبروتينات، يمكن لِبوليمرات مثل حلقات البولي إيثيلين غليكول المصممة بشكل خاص أو البوليانونات الاصطناعية أن تتفوق على بعض المرافِقات الطبيعية في منع التراكم الناجم عن الحرارة. تربط أنظمة أخرى بوليمرات مرافِق مرنة بببتيدات قصيرة لإعادة تشكيل أغشية شبيهة بالخلايا إلى صفائح نانوية مسطحة أو حويصلات، مكونة منصات ثنائية الأبعاد قابلة للعكس لنقل الحمولات وهندسة الأنسجة.

بناء مرافِقين ذكيين وقابلين للتبديل
بالتجاوز عن مجرد الإمساك بالإِكلاء وإطلاقهم، فإن المرافِقين الاصطناعيين الحديثين يمكنهم الآن الاستجابة لبيئتهم. بنى الباحثون نانوجلز، وجسيمات نانوية، وشبكات بوليمرية يتغير فيها قبضتها على البروتينات بتبدلات الحموضة أو الحرارة أو الضوء أو مواد كيميائية محددة مثل الجلوكوز. على سبيل المثال، تصبح بعض الميسيلات أكثر محبة للماء عند درجة حموضة حمضية طفيفة، مقلدةً المرافِقات الطبيعية من خلال التقاط البروتينات المهددة ثم إطلاقها عندما يعود الـpH إلى حالته. تنهار أو تتمدد البوليمرات الحساسة للحرارة عند عبورها عتبة حرارية، مما يسمح لها بحجز البروتينات التالفة عند درجة حرارة وإطلاق البروتينات المعاد طيها عند أخرى. يمكن استخدام مجموعات حساسة للضوء كمفاتيح جزيئية، تشغيل أو إيقاف مسارات تجميع الـDNA بومضة، بينما يمكن للجسيمات المستجيبة للسكر حماية هرمون علاجي ثم إطلاقه تفضيليًا عندما يرتفع مستوى السكر في الدم.
ما يعنيه هذا للطب والتكنولوجيا
يخلص المقال إلى أن المرافِقين الاصطناعيين يتطورون من مثبتات كيميائية بسيطة إلى «أدوات جزيئية» قابلة للبرمجة بدرجة عالية يمكنها التعرف على هياكل بيولوجية متنوعة وحمايتها وإعادة تشكيلها عند الطلب. من خلال موازنة القوى الجاذبة والطاردة بعناية، وبدمج الحساسية لإشارات مثل الحموضة والحرارة والضوء أو الإجهاد الميكانيكي، يمكن لهذه الأنظمة أن تطوي الجزيئات المستهدفة في المكان والوقت المناسبين. على المدى البعيد، قد تجعل هذه المساعدات الذكية إنتاج البروتينات الصناعي أكثر كفاءة، وتحسن حساسية أجهزة الاستشعار الحيوية، وتدعم حواسيب جزيئية، وتقدّم طرقًا جديدة لمعالجة الأمراض المرتبطة بالبروتينات غير المطوية—مما قد يشمل حالات مثل مرض ألزهايمر—في حين تقلد بدقة التحكم الدقيق الذي تحققه الخلايا الحية بالفعل.
الاستشهاد: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
الكلمات المفتاحية: المرافِقون الاصطناعيون, طي البروتين, البوليمرات الذكية, النانوطب, المواد المستجيبة للمحفزات