Clear Sky Science · ar
التعامل مع الموت بالنحاس: من إعادة برمجة الأيض إلى الاستغلال العلاجي في السرطان
عندما يتحول معدن مفيد إلى سلاح ضد السرطان
يشتهر النحاس كعنصر في الأسلاك الكهربائية والسباكة، لكنه يجري أيضاً بهدوء داخل خلايانا، مساعداً الإنزيمات على إنتاج الطاقة وحمايتنا من الضرر. تستعرض هذه المقالة مراجعة مفاجأة: في ظل ظروف معينة، يؤدي فائض النحاس إلى دفع خلايا السرطان إلى نوع خاص من الموت. قد يفتح فهم هذه العملية — المسماة «الموت بالنحاس» أو cuproptosis — سبل علاجية جديدة للأورام التي تهربت من العلاجات القياسية.
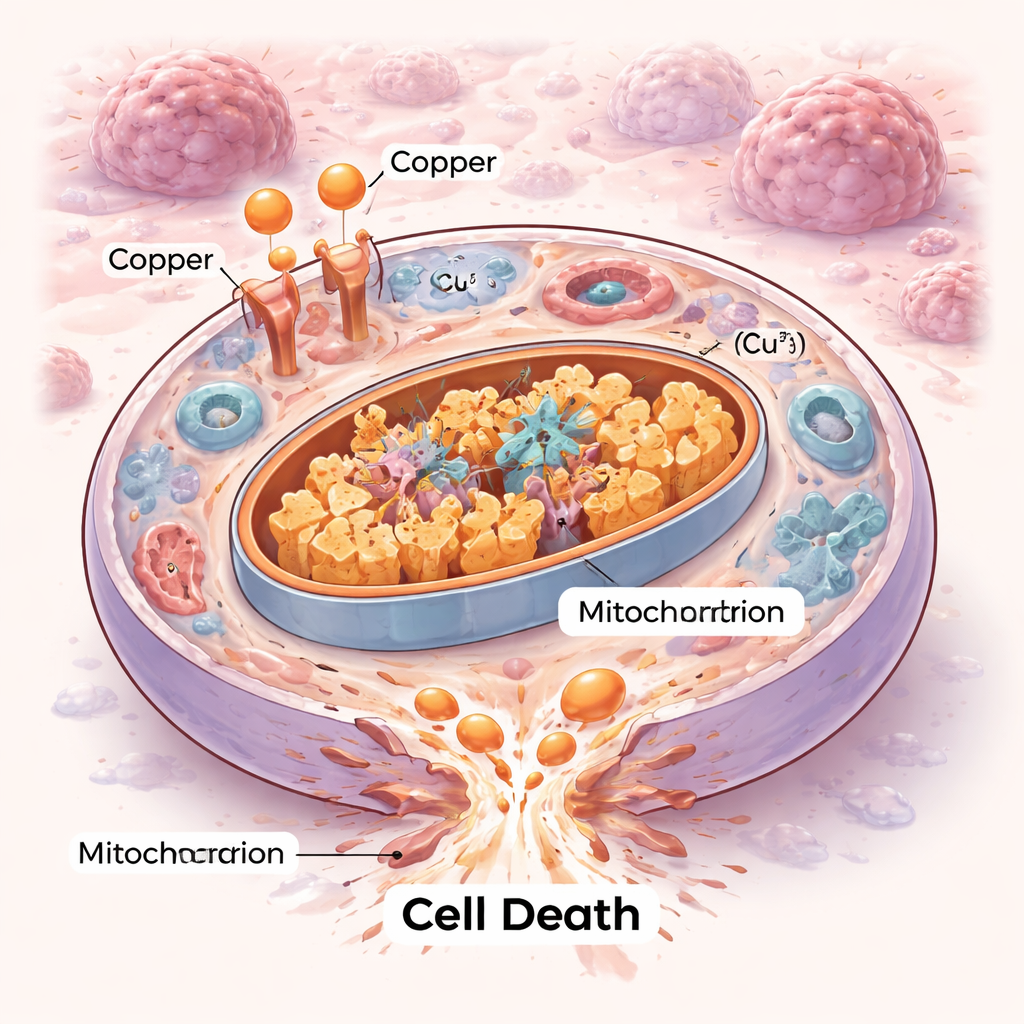
طريقة جديدة يمكن للخلايا أن تموت بها
الخلايا لا تموت جميعها بنفس الطريقة. لعقود، رسم العلماء برامج الانتحار الخلوي المنظمة مثل الاستماتة (apoptosis) وأشكال أحدث مثل الفيروبتوزيس. يضيف الموت بالنحاس فصلاً جديداً. هنا، يفيض النحاس الزائد محطات طاقة الخلية — الميتوكوندريا — ويرتبط بأنزيمات أيضية محددة تساعد عادة على احتراق الوقود. يسبب هذا الالتحام تجمّع هذه الإنزيمات ويزعزع استقرار مكونات الحديد–كبريت الصغيرة التي تحتاجها الميتوكوندريا لتعمل. النتيجة تشبه ازدحاماً داخلياً وانهياراً ميكانيكياً لا تستطيع الخلية إصلاحه، فينتهي بها المطاف بالموت نتيجة ضغط بروتيني سام بدلاً من مسارات الانتحار الكلاسيكية.
كيف تسيطر خلايا السرطان على النحاس والطاقة
بما أن النحاس ضروري وخطير في الوقت نفسه، تحافظ الخلايا على شبكة لوجستية معقدة لنقله بأمان. تجلب ناقلات مخصصة النحاس إلى داخل الخلية، وترافقه بروتينات مرافقه إلى الميتوكوندريا ووجهات أخرى، وتلتقط جزيئات التخزين مثل الميتالوثيونين والغلوتاثيون أي فائض. غالباً ما تعيد الأورام برمجة هذا النظام. يعزّز بعضها الناقلات أو البروتينات المرافقة لتلبية حاجتها العالية للطاقة؛ بينما يزيد البعض الآخر ناقلات التصدير أو بروتينات التخزين لتجنب فائض النحاس. في الوقت نفسه، يغيّر العديد من السرطانات أيضها — متبدلة بين حرق السكر قرب سطح الخلية والتنفس الميتوكوندري الأعمق. توضح المراجعة أن الموت بالنحاس يضرب بشدة الخلايا التي تعتمد بشكل كبير على الميتوكوندريا، مما يجعل الأورام ذات هذا الملف الأيضي عرضة بشكل خاص.
مفاتيح تحكم تضبط حساسية النحاس
تؤثر «صنّاعات القرار» الخلوية الرئيسية على ما إذا كان الموت بالنحاس سيقع أم لا. على سبيل المثال، يدفع مكبح الأورام p53 الخلايا بعيداً عن التخمّر السريع للسكر نحو استخدام الوقود الميتوكوندري بشكل أكثر انتظاماً. وبذلك، ومن خلال تغيير تعامل الإنزيمات الرابطة للنحاس، يمكن أن يجعل p53 السرطانات أكثر عرضة للموت الناتج عن النحاس — بينما تشيع الأشكال المطافرة من p53 العكس. في المقابل، يساعد عامل نقص الأكسجين HIF‑1α، النشط في نوى الأورام منخفضة الأكسجين، الخلايا على الهروب من الموت بالنحاس عبر خفض إنزيمات ميتوكوندريّة رئيسية وتعزيز دروع رابطة للنحاس. مسارات أخرى، مثل Wnt/β‑catenin وAKT، تعزز المقاومة عبر دفع تصدير النحاس أو تعديل بروتينات حاسمة كيميائياً بحيث لا تعود تستجيب لفائض النحاس. تعمل هذه الشبكات معاً كمنظمات حرارة، ترفع أو تخفض حساسية الورم للعلاج القائم على النحاس.
النحاس وجهاز المناعة وتوصيل الأدوية الأذكى
لا يقتصر دور النحاس على قتل خلايا السرطان مباشرة؛ بل يشكّل أيضاً المشهد المناعي حول الأورام. يمكن للإجهاد النحاسي المضبوط أن يجعل الخلايا السرطانية المحتضرة أكثر «وضوحاً»، مطلقة إشارات خطر تجذب وتفعّل الخلايا التائية والخلايا المتغصنة والبلعميات. كما يمكن للنحاس أن يؤثر في مستويات نقاط التفتيش المناعي مثل PD‑L1، التي تستخدمها الأورام لإيقاف الخلايا التائية المضادة للسرطان، مما يشير إلى إمكانيات الجمع بين أدوية استهداف النحاس والعلاجات المناعية الحديثة. وبما أن النحاس الحر يمكن أن يضر الأنسجة السليمة، يبني الباحثون أدوات دقيقة — أيونوفورات صغيرة تجلب النحاس انتقائياً إلى خلايا السرطان، ومنصات نانوتكنولوجية تحشُو النحاس أو أدوية مدفوعة بالنحاس داخل جسيمات مستهدفة أو مواد هلامية. تهدف هذه التقنيات إلى رفع النحاس إلى مستويات قاتلة داخل الأورام مع إبقاء باقي الجسم في نطاق آمن.
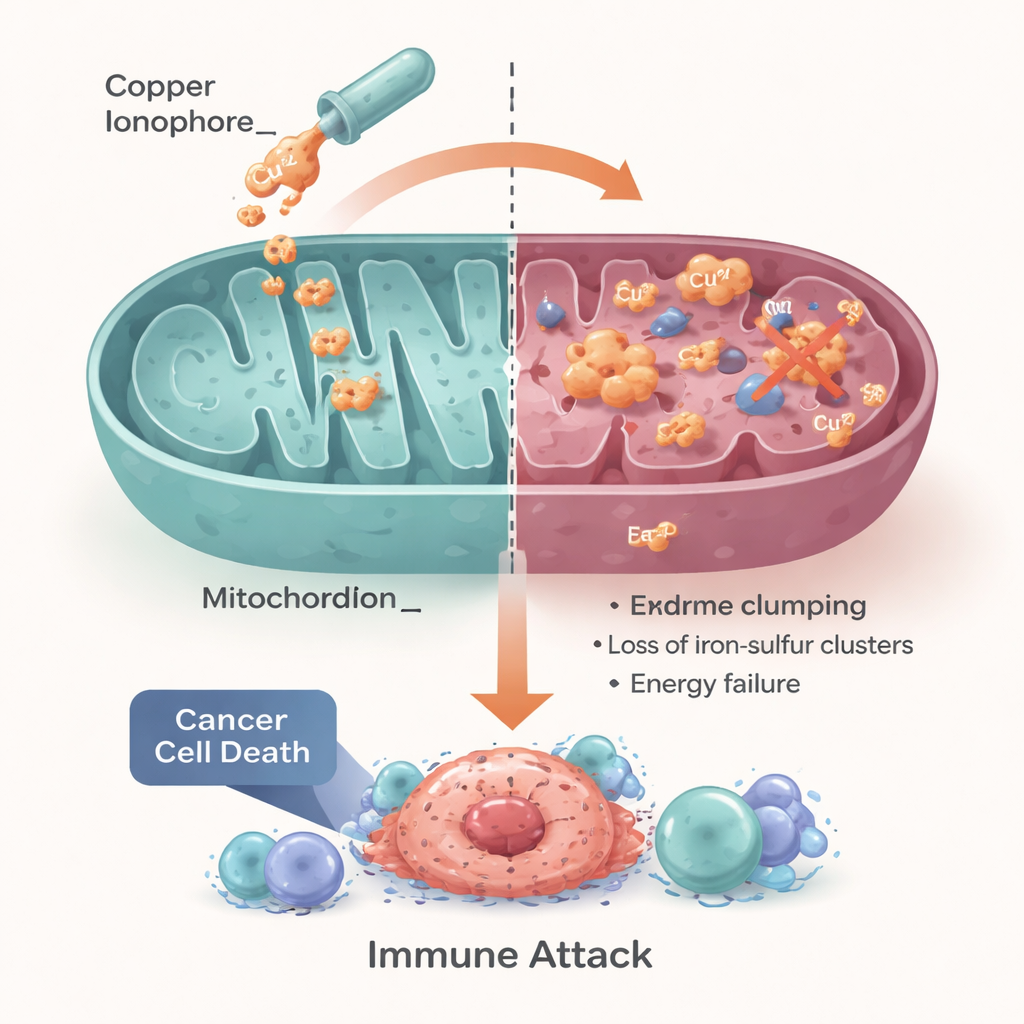
تحويل ضعف خلوي إلى علاج
يخلص المؤلفون إلى أن الموت بالنحاس يحوّل حاجة خلوية أساسية — إدارة دقيقة للنحاس والطاقة — إلى نقطة ضعف محتملة للسرطان. قد تكون السرطانات التي تعاني اضطراباً في التعامل مع النحاس أو اعتماداً مفرطاً على الأيض الميتوكوندري أكثر حساسية لاستراتيجيات قائمة على النحاس، بما في ذلك أدوية معاد توظيفها مثل ديسلفيرام وإليسكلومول، وكذلك الجيل التالي من الجزيئات النانوية. ومع ذلك، يؤكدون أن النجاح سيعتمد على مطابقة المرضى المناسبين مع النهج المناسب، باستخدام مؤشرات حيوية تُبلغ عن ناقلات النحاس، ونشاط الميتوكوندريا، وحالة المناعة والأكسجين في الورم. إذا أمكن تجاوز هذه العقبات، قد يمنح تسخير الموت بالنحاس أطباء الأورام رافعة جديدة مدفوعة بالمعدن لعلاج أورام تفتقر حالياً إلى خيارات جيدة.
الاستشهاد: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
الكلمات المفتاحية: الموت بالنحاس, أيض النحاس, علاج السرطان, أيض الورم, المناعة ضد السرطان