Clear Sky Science · ar
قوة مغناطيسية‑ميكانيكية ديناميكية في الليسوسومات تُحدث إعادة استقطاب طويلة الأمد للبلعميات من أجل مناعة مضادة للأورام
استخدام قوى لطيفة لإيقاظ الجهاز المناعي
غالبًا ما ينجح السرطان في البقاء عبر جعل دفاعات الجسم في حالة خمول. يستقصي هذا البحث طريقة غير متوقعة لإيقاظها مجددًا: من خلال سحب أجزاء صغيرة داخل الخلايا المناعية باستخدام جسيمات نانوية مدفوعة مغناطيسيًا. بدلاً من الاعتماد فقط على الأدوية، يستخدم الباحثون قوى ميكانيكية مضبوطة داخل الخلايا لإعادة برمجة خلايا مناعية تسمى البلعميات إلى مقاتلين ضد الورم تدوم خصائصهم لفترة طويلة.
لماذا يصعب علاج الأورام الصلبة
غيرت العلاجات المناعية الحديثة للسرطان، مثل الأجسام المضادة المانعة لنقاط التفتيش والخلايا المناعية المهندسة، مسار العلاج لبعض سرطانات الدم. ومع ذلك، فإن هذه الطرق تساعد إلا نسبة صغيرة فقط من المصابين بالأورام الصلبة مثل سرطان الرئة. أحد الأسباب الرئيسية هو البيئة المجهرية للورم. تحاط الأورام بموئل واقٍ مملوء بالخلايا والإشارات التي تخمد المناعة. غالبًا ما تُدفع البلعميات، التي تستطيع إما مهاجمة الأورام (حالة شبيهة بـM1) أو دعمها (حالة شبيهة بـM2)، إلى وضعية M2 المساندة للورم. وقد كان من الصعب قلب هذه «البرمجة السيئة» بطريقة دائمة باستخدام الأدوية الكيميائية الحيوية التقليدية وحدها.
تحويل الجسيمات النانوية إلى محركات ميكانيكية دقيقة
صمم الفريق محركات نانوية مغناطيسية—جسيمات نانوية من أكسيد الحديد مخدوم بالزنك ومغلفة ببوليمر ذي شحنة موجبة—تبتلعها البلعميات بسهولة وتتركز داخل الليسوسومات، وهي مراكز إعادة التدوير والإشارات داخل الخلية. بمجرد دخولها، تجعل حقل مغناطيسي دوار خارجي هذه الجسيمات تصطف في سلاسل شبيهة بالقصبات وتدور، مما يحرك السائل الكثيف داخل الليسوسومات ويخلق دوامات دقيقة. أظهرت محاكيات الحاسوب وتجارب على أغشية نموذجية أنه من خلال ضبط تردد الدوران بدقة يمكن ضبط إجهاد القص على غشاء الليسوسوم إلى نقطة «مناسبة»: قوية بما يكفي لجعل الغشاء يتسرب لفترة وجيزة، لكن ليست مدمرة بشكل دائم.
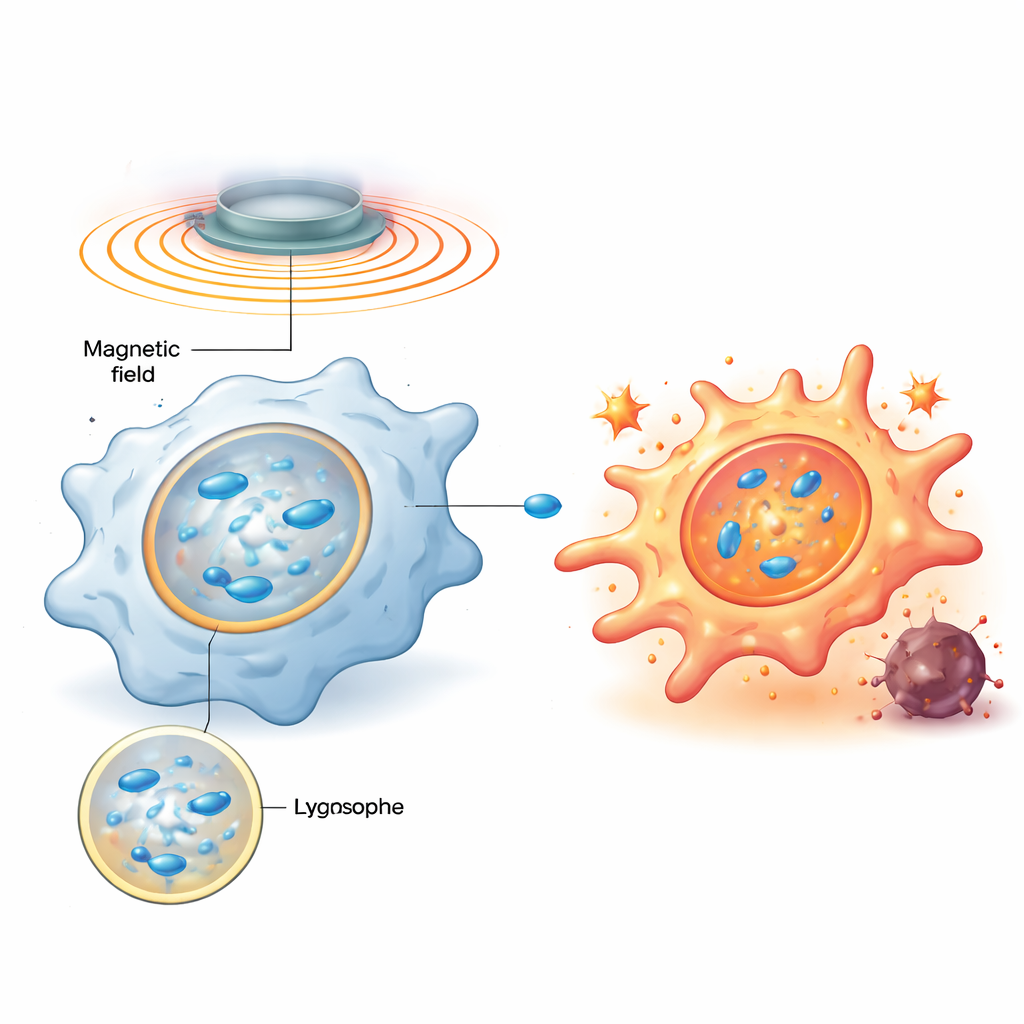
دفعة ميكانيكية تُطلق إنذارًا كيميائيًا حيويًا
عندما يتعرض غشاء الليسوسوم لاضطراب مؤقت، يتجه بروتين رابط للسكريات يُدعى جاليكتين‑9 بسرعة إلى بقع الضرر، ليعمل كمستشعر لهذا الضغط الميكانيكي. تظهر الدراسة أن هذا يؤدي بدوره إلى تنشيط إنزيم حساس للطاقة، AMPK، الذي يعزز بدوره مسار الإشارة NF‑κB—المعروف بدوره في دفع الاستجابات الالتهابية والمضادة للميكروبات. معًا تعيد هذه الإشارات توصيل أيض البلعميات بعيدًا عن حالة هادئة وموفرة للوقود ونحو التحلل السكر السريع (الجليكوليسيس)، وهو نمط مرتبط بسلوك عدائي شبيه بـM1. والأهم أن الليسوسوم يصلح نفسه ويخفّ النشاط الإشارِيّ عند إيقاف الحقل المغناطيسي؛ وعند إعادة تشغيل الحقل لاحقًا يُعاد تنشيط نفس المسار. تتيح هذه الدورات البرمجية الممكنة تشغيل وإيقاف المفتاح الميكانيكي نفسه مرارًا دون قتل الخلايا.
إعادة تعليم البلعميات لمحاربة الأورام
في مزروعات الخلايا، حولت النفاذية الليسوسومية المحرضة مغناطيسيًا—التي سُمِّيت MagLMP—البلعميات المدفوعة نحو حالة داعمة للورم شبيهة بـM2 إلى حالة مؤيدة للالتهاب شبيهة بـM1. أنتجت هذه الخلايا المعاد برمجتها المزيد من السيتوكينات الالتهابية واحتفظت بملف M1‑شبيه لعدة أيام، حتى في وسط مستمد من الأورام الذي يدفعها عادة نحو M2. في نماذج أورام الفئران، أدى تضمين المحركات النانوية المغناطيسية داخل الأورام وتطبيق دورات يومية من الحقل الدوار إلى إبطاء نمو عدة أنواع من السرطان. عندما أُزيلت البلعميات تجريبيًا، اختفى الفائدة إلى حد كبير، ما يبيّن أن هذه الخلايا مركزية لتأثير العلاج. وكشف التسلسل الجيني لخلايا مفردة في نسيج الورم أن MagLMP زاد نسبة البلعميات الشبيهة بـM1، وعزز العدلات والـCD8 التائية المُنفذة المضادة للأورام، ورفَّع تعابير جينية متعلقة بـNF‑κB والجليكوليسيس داخل البلعميات.
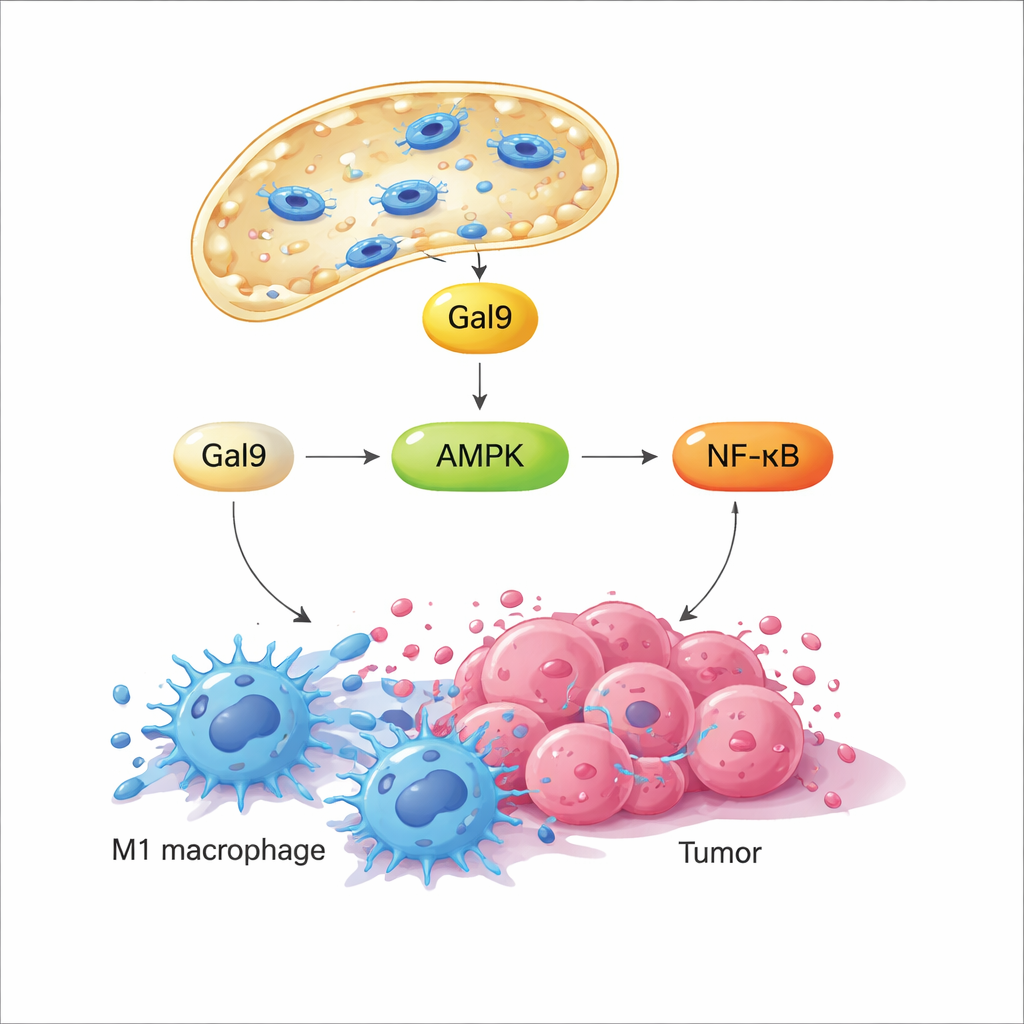
من التحكم المحلي إلى العلاج الجهازي
سأل الباحثون فيما بعد ما إذا كان يمكن أن يعمل هذا النهج بشكل أقرب إلى العلاج في العالم الحقيقي، يُعطى عبر مجرى الدم. حقنوا المحركات النانوية وريديًا واستخدموا مغناطيسًا خارجيًا بسيطًا لتركيزها داخل الأورام، مظهرين التقاطًا فعالًا من قبل البلعميات في فراش الورم. وعند تطبيق علاج MagLMP بعد ذلك تحولَت البلعميات مجددًا نحو حالة شبيهة بـM1 وكبح نمو الورم. في نموذج فأري لسرطان الرئة المبكر المتنامي داخل الرئة نفسها، أدى الجمع بين التوجيه المغناطيسي وMagLMP الدوري إلى إطالة ملحوظة في البقاء: عاش نحو ثلث الفئران المعالجة أكثر من 300 يوم، مقارنة بأسابيع فقط لدى الحيوانات الضابطة. وعند الجمع بين MagLMP ومثبط نقطة تفتيش PD‑1 تعزز التحكم في الورم في نماذج يصعب علاجها.
طريقة جديدة للتحكم في المناعة من الداخل إلى الخارج
تُظهر هذه الدراسة أن قوى ميكانيكية صغيرة ومتحكمًا فيها داخل عضية خلوية محددة يمكن استثمارها لتوجيه سلوك الجهاز المناعي في حيوانات حية. من خلال «نخز» الليسوسومات بشكل متكرر وقابل للعكس، ينشط MagLMP محور جاليكتين‑9–AMPK–NF‑κB الذي يعيد برمجة البلعميات إلى مقاتلين ضد الورم يدومون دون إلحاق ضرر واسع بالخلايا. للقراء غير المتخصصين، الفكرة الأساسية هي أن الإشارات الفيزيائية—التي تُقدم بواسطة محركات نانوية مغناطيسية—يمكن أن تعمل كقرص تحكم على الجهاز المناعي، مقدمة فئة جديدة من الأدوات لتكاملة مع الأدوية في مستقبل علاجات السرطان المناعية.
الاستشهاد: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
الكلمات المفتاحية: العلاج المناعي للسرطان, إعادة برمجة البالعات (البلعميات), جسيمات مغناطيسية نانوية, التحويل الميكانيكي‑الخلوي, إشارات الليسوسوم