Clear Sky Science · ar
الإينوزين يعزز إعادة برمجة أيض كريات الدم الحمراء ويستعيد تحرير الأكسجين للتجديد عبر محور 2,3‑BPG‑PNP
لماذا يهم هذا لشيخوخة صحية
مع تقدم الناس في العمر، غالبًا ما لا تحصل أعضاؤهم على كمية كافية من الأكسجين، وهو ضغط صامت يساهم في أمراض القلب وفقدان الذاكرة وضعف العضلات ومشكلات مرتبطة بالعمر الأخرى. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قويًا: ماذا لو أن جزءًا من المشكلة يبدأ داخل كريات الدم الحمراء التي تنقل الأكسجين، وماذا لو أن جزيئًا طبيعيًا شائعًا يسمى الإينوزين يمكنه أن يساعد في استعادة حيويتها؟
كيف تتغير كريات الدم الحمراء مع العمر
تابع الباحثون أكثر من 300 بالغ تتراوح أعمارهم بين 20 و85 سنة وقاسوا بعناية مدى كفاءة كريات دمهم الحمراء في تحرير الأكسجين. وجدوا تراجعًا ثابتًا عبر العمر: كريات دم المسنين احتفظت بالأكسجين بإحكام أكبر وأطلقت كمية أقل منه إلى الأنسجة. جاء هذا التغير مصحوبًا بعلامات تحذيرية في أعضاء أخرى، بما في ذلك ارتفاع ضغط الدم وتراجع طفيف في وظائف الكلى والكبد. في الفئران ظهر نفس النمط: الحيوانات الأكبر سنًا كانت كريات دمها الحمراء تطلق كمية أقل من الأكسجين وأظهرت إجهادًا تأكسديًا أكبر، وهو تآكل كيميائي مرتبط بالشيخوخة.
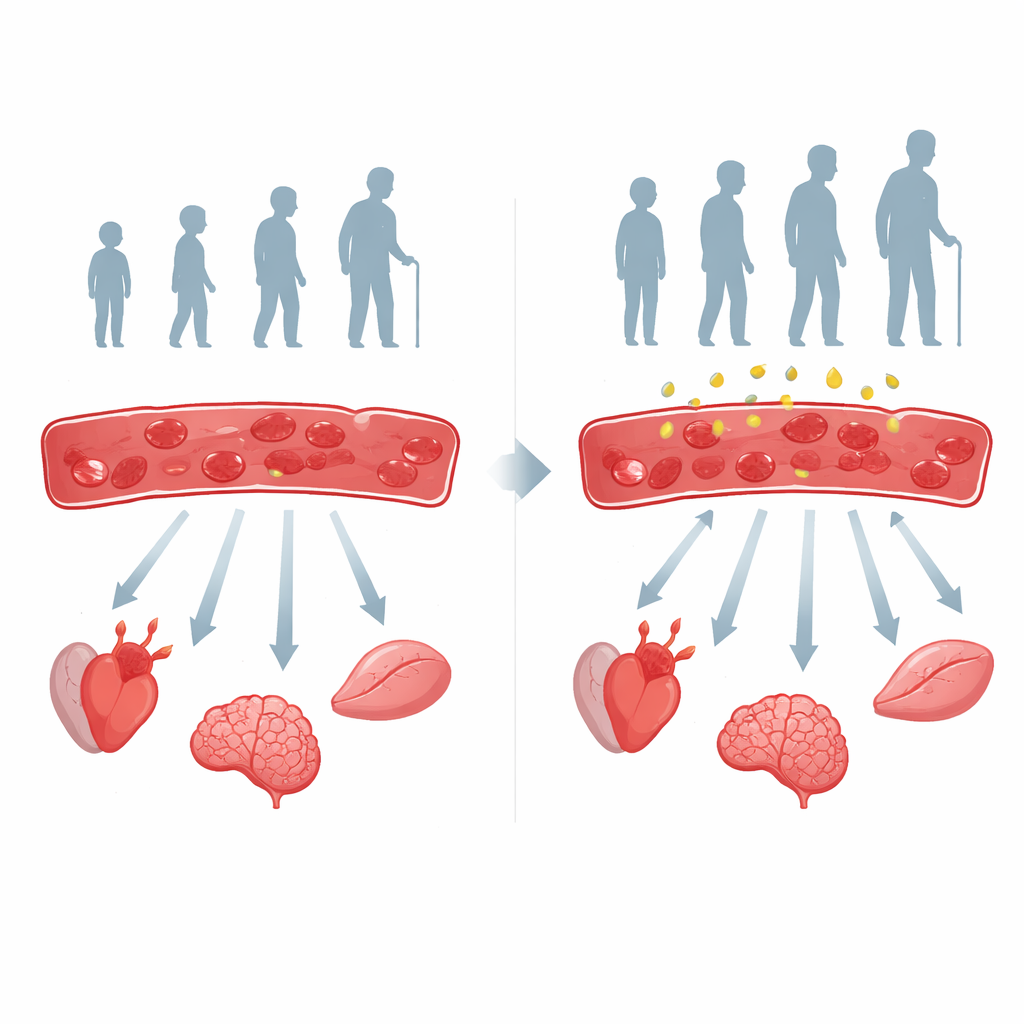
مفتاح الوقود الخفي داخل خلايا الدم
تفتقد كريات الدم الحمراء للنوى والميتوكوندريا، لذا تعتمد على كيمياء داخلية مبسطة لصنع الطاقة وضبط تحرير الأكسجين بدقة. جزيء صغير يسمى 2,3‑BPG يساعد عادةً الهيموغلوبين على تحرير الأكسجين حيثما يلزم. وجد الفريق أن مستويات 2,3‑BPG تنخفض مع العمر لأن إنزيمًا يصنعه، BPGM، يصبح أقل نشاطًا. في كل من البشر والفئران، ارتبط انخفاض 2,3‑BPG ارتباطًا وثيقًا بتراجع تحرير الأكسجين. عندما هندس العلماء فئرانًا لم تستطع كريات دمها الحمراء صنع 2,3‑BPG، طورت تلك الحيوانات قصورًا مبكرًا في الأنسجة لأسباب نقص الأكسجة، وإجهادًا تأكسديًا أكبر، وضعفًا في العضلات، وتدهورًا في الذاكرة، وتنظيمًا أسوأ للسكر في الدم — باختصار صورة تسارع الشيخوخة ناتجة فقط عن تغييرات في كريات الدم الحمراء.
الإينوزين كمصدر طاقة احتياطي
كشف التحليل الأيضي أن كريات الدم الحمراء المتقدمة في السن لا تبطئ فحسب؛ بل تعيد توصيل مساراتها. مع تعثر معالجة الجلوكوز، تبدأ في الاعتماد بشكل متزايد على حرق الإينوزين، وهو مركب طبيعي مشتق من النيوكليوتيدات. في المسنين والفئران، أصبح إنزيم PNP، الذي يكسر الإينوزين إلى جزء سكري يسمى ريبوز‑1‑فوسفات، أكثر نشاطًا. باستخدام إينوزين موسوم، أظهر الباحثون أن هذا الجزء السكري يتدفق إلى مسارات داخلية رئيسية تدعم إنتاج الطاقة، والأهم من ذلك، تساعد في إعادة بناء 2,3‑BPG. في تجارب أنبوبية، أدى نقع كريات الدم الحمراء البشرية أو الفأرية في الإينوزين إلى تعزيز سريع لقدرتها على إطلاق الأكسجين وخفض الجزيئات المؤكسدة الضارة — بشرط أن تتمكن الخلايا من إدخال الإينوزين عبر ناقل يسمى ENT1 وهضمه بواسطة PNP.
اختبارات جينية وتجارب حيوانية
لتأكيد أهمية نظام الوقود الاحتياطي هذا، أنشأ الفريق فئرانًا تفتقر كريات دمها الحمراء إلى ENT1، بوابة دخول الإينوزين. هذه الحيوانات لم تستفد من الإينوزين، وكان لديها تحرير أكسجين أسوأ، وإجهاد تأكسدي أعلى، وأظهرت تدهورًا أسرع في الإدراك وقوة العضلات وتنظيم السكر مع تقدمها في العمر. ثم انتقل العلماء إلى اختبار قبل سريري: أعطوا فئرانًا في منتصف العمر حقن إينوزين يومية لمدة شهر. أظهرت الحيوانات المعالجة كريات دم حمراء تطلق مزيدًا من الأكسجين وتنتج مؤكسدات ضارة أقل. ركضت الفئران أداءً أفضل على قضيب دوار، وأمسكت بقوة أكبر، وأدت أفضل في اختبارات الذاكرة، وكان لديها دليل أقل على تلف ناتج عن نقص الأكسجة في القلب والكلى والعضلات ومناطق دماغية رئيسية تشارك في التعلم والذاكرة.
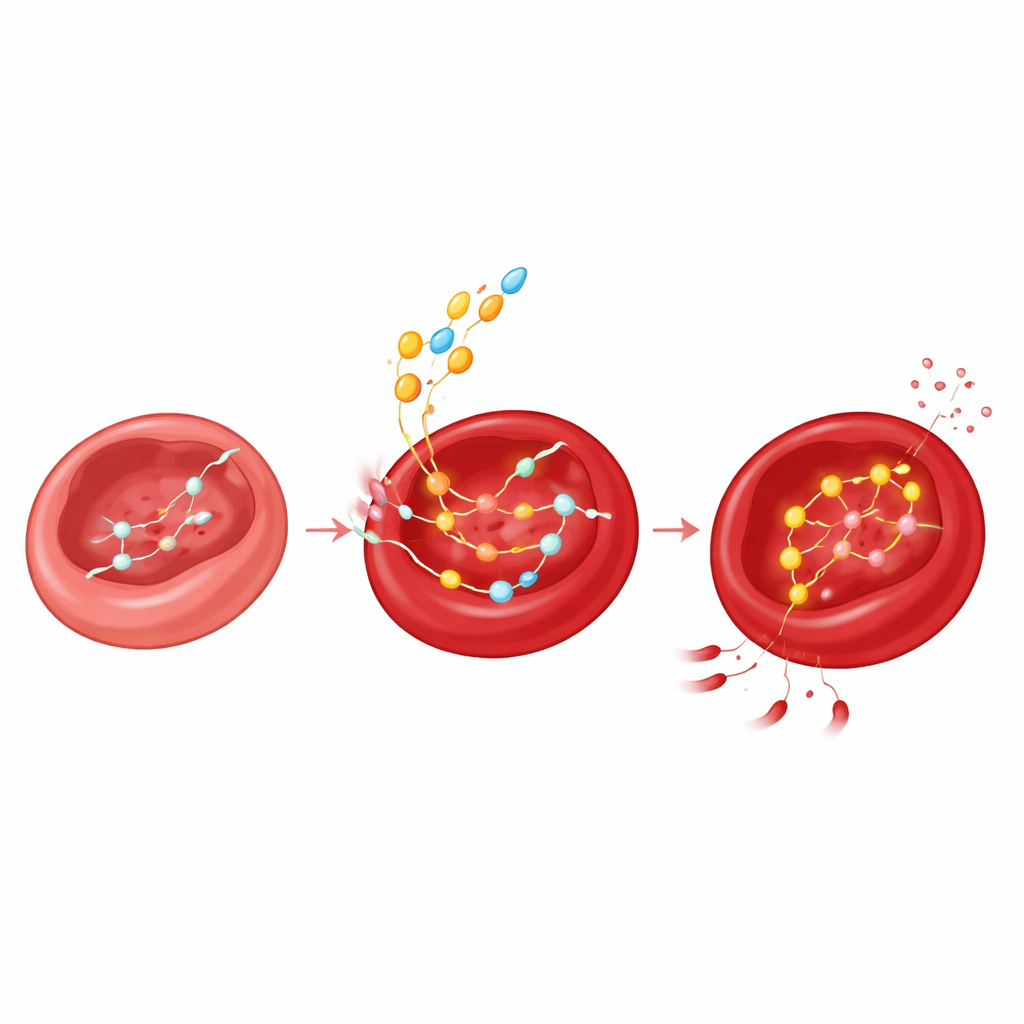
فرملة جزيئية ترتخي مع التقدم في العمر
تكشف الدراسة أيضًا عن حلقة تغذية راجعة أنيقة. باستخدام النمذجة الجزيئية وقياسات نشاط الإنزيم والتحويرات المستهدفة، يظهر المؤلفون أن 2,3‑BPG نفسه يرتبط بـ PNP ويمنع نشاطه عن طريق التنافس مع الفوسفات عند نقاط تلامس محددة على الإنزيم. في الشباب، تحافظ وفرة 2,3‑BPG إذن على كبح تفكيك الإينوزين. ومع انخفاض مستويات 2,3‑BPG مع العمر، تُفلت هذه الفرملة: يصبح PNP أكثر نشاطًا، يُستهلك الإينوزين بشكل أسرع، ويتم تحويل جزء الرِيبوز إلى مسارات منتجة للطاقة لتعويض تباطؤ أيض الجلوكوز. بعبارة أخرى، نفس الجزيء الذي يساعد الهيموغلوبين على تحرير الأكسجين يتحكم أيضًا بهدوء في كيفية استغلال كريات الدم الحمراء لمخزون وقود طارئ.
ماذا يعني هذا للشيخوخة والتجديد
مجموع هذه النتائج يقترح أن الشيخوخة ليست فقط عن فشل الأعضاء بل أيضًا عن كريات دم حمراء مسنة توصل أقل من الأكسجين. يشكل انخفاض نشاط BPGM ومستويات 2,3‑BPG علامة جديدة لـ «الشيخوخة»، بينما يعمل محور الإينوزين–PNP–ENT1 كنظام إنقاذ مدمج يعيد جزئيًا تدفق الطاقة وتحسين تحرير الأكسجين. بتوفير إينوزين إضافي من الخارج، على الأقل في الفئران، استطاع الباحثون تقوية هذا النظام الإنقاذي، وتحسين أداء كريات الدم الحمراء، وتخفيف نقص الأكسجة في الأنسجة، وإبطاء تراجع القوة والذاكرة. وعلى الرغم من بقاء الكثير للاختبار في البشر، تثير الدراسة إمكانية مثيرة: أن ضبط أيض كريات الدم الحمراء — ربما بالإينوزين أو استراتيجيات ذات صلة — قد يصبح طريقًا جديدًا لشيخوخة أكثر صحة.
الاستشهاد: Liu, W., Yang, Z., Chen, C. et al. Inosine promotes erythrocyte metabolic reprogramming and restores oxygen release for rejuvenation via 2,3-BPG-PNP axis. Cell Discov 12, 19 (2026). https://doi.org/10.1038/s41421-026-00877-6
الكلمات المفتاحية: كريات الدم الحمراء, الشيخوخة, توصيل الأكسجين, الإينوزين, الأيض