Clear Sky Science · ar
التغيرات الديناميكية للبيئة المناعية الدقيقة في سرطان المبيض بعد العلاج الكيميائي النيوأديوفانت
لماذا تهم هذه الدراسة النساء المصابات بسرطان المبيض
يُعالَج سرطان المبيض المتقدّم غالبًا بعلاجات كيميائية قوية قبل أو بعد الجراحة، ومع ذلك يعود المرض لدى كثير من النساء ويتوقف عن الاستجابة للأدوية. تطرح هذه الدراسة سؤالًا ملحًا: كيف يعيد العلاج الكيميائي تشكيل دفاعات الجسم حول الورم بصمت، وهل يمكننا تعديل تلك الاستجابة لإطالة مدة فاعلية العلاج؟ من خلال فحص الخلايا الفردية وتجربة تراكيبات دوائية جديدة في الفئران، يكشف الباحثون دورًا مخفيًا لجزيئات دهنية شبيهة بالهرمونات تُسمى البروستاجلاندينات في مساعدة الأورام على التهرب من الجهاز المناعي بعد العلاج الكيميائي.
ساحة معركة متغيرة حول الورم
لا تنمو أورام المبيض بمعزل: فهي تقع في "حي" مكتظ بالخلايا المناعية والنسيج الضام والسائل في البطن. قبل العلاج، يكون هذا الحي مائلًا بالفعل لصالح السرطان، مع ندرة خلايا T القاتلة النشطة وكثرة الخلايا التي تخفف الهجوم المناعي. حلّل الفريق بيانات تسلسل RNA للخلايا الفردية المنشورة سابقًا من نساء مصابات بسرطان المبيض المصفوحي عالي الدرجة، وقارنوا عينات مأخوذة قبل وبعد العلاج الكيميائي النيوأديوفانت (العلاج الكيميائي المعطى قبل الجراحة). وجدوا أن العلاج الكيميائي لم يقضِ على خلايا الورم فحسب؛ بل أطلق أيضًا نشاطًا مناعيًا مؤقتًا، زيَّد إشارات مرتبطة بتحفيز خلايا T والالتهاب مع تقليل بعض الخلايا التُّظيمية التي عادةً ما تكبح الهجوم.
عندما تتحول التغييرات المفيدة إلى ضارة
رغم هذا الدفع المؤقت، يعود المرض لدى معظم المرضى ويصبح مقاومًا لعقاقير البلاتين مثل السيسبلاتين. لفهم السبب، غاص الباحثون أعمق في كيفية تواصل أنواع الخلايا المختلفة بعد العلاج. اكتشفوا أن العلاج الكيميائي زاد بقوة من تعبير الجينات المشاركة في صنع البروستاجلاندينات في البلاعم المرتبطة بالأورام والخلايا الليفية، وعزَّز التواصل بين هذه الخلايا وخلايا T. باستخدام أدوات رياضية متقدمة، أظهروا أن البيئة العامة تحوّلت نحو حالة مُلْهِبة ولكنها في النهاية قمعية، مع ارتفاع مستويات الكيموكينات التي تجذب الخلايا النخاعية وتعزيز مسارات يمكن أن تُنهك خلايا T مع مرور الوقت. يشير هذا إلى أن البروستاجلاندينات قد تعمل كمفتاح جزيئي، يحول دفعة مناعية مفيدة في البداية إلى مكبح طويل الأمد للمناعة المضادة للورم.
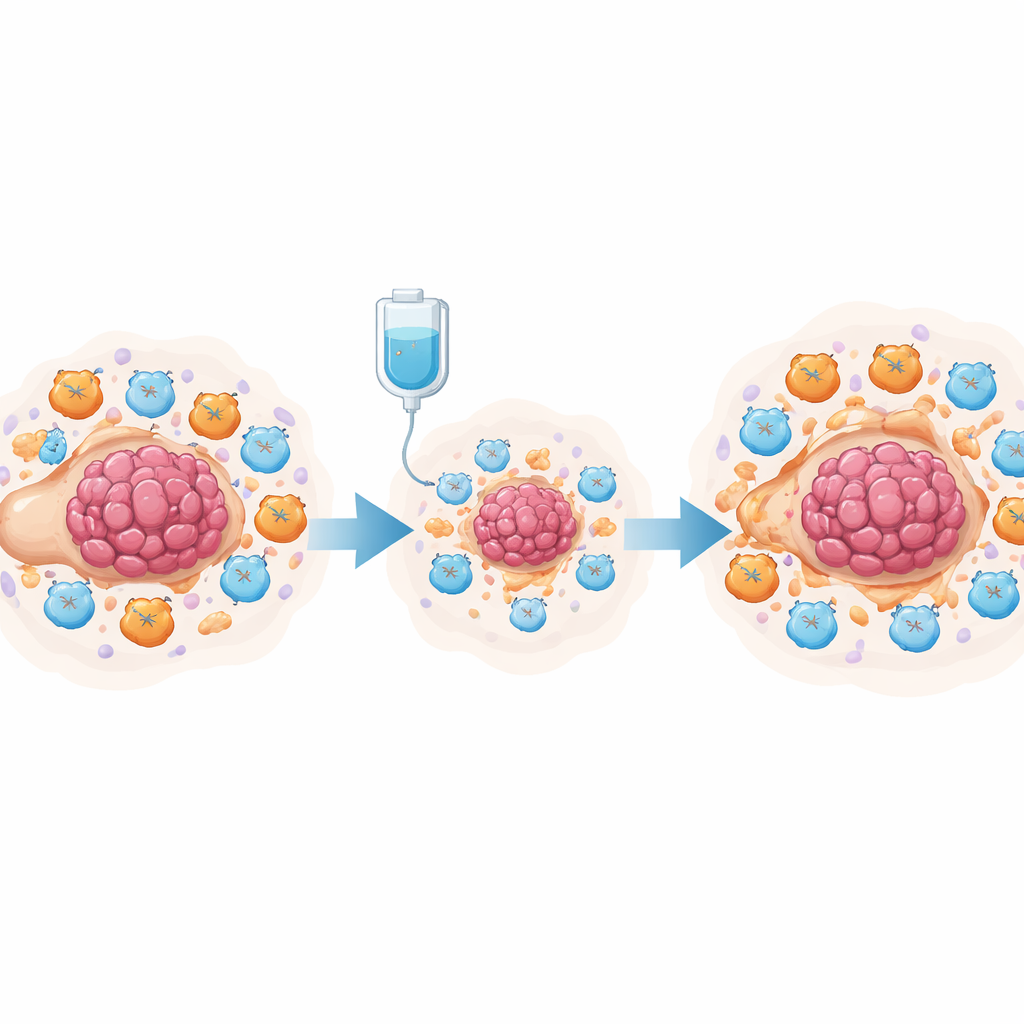
العلاج الكيميائي، البروستاجلاندينات وخمول خلايا T
لاختبار هذه الفكرة تجريبيًا، استخدم الفريق نموذجًا فأريًا لسرطان المبيض عُولج بالسيسبلاتين. أظهر التحليل الخلوي الفردي لعشرات الآلاف من الخلايا من تجويف البطن أن السيسبلاتين قلّل خلايا الورم وزاد إجمالي خلايا T، لكنه وسّع أيضًا بشكل ملحوظ الخلايا المكبتة المنشأ من النخاع (MDSCs) وخلايا T القاتلة المتعبة. أنتجت كل من خلايا الورم وهذه الخلايا المكبة مستويات عالية من إنزيمات صنع البروستاجلاندين. في أطباق التعايش الخلوي، دفعت خلايا الورم المعالجة بالسيسبلاتين خلايا نخاع العظم إلى تبنّي حالة شبيهة بـ MDSC وضعفت نشاط ونمو خلايا CD8+ القاتلة. تتبّع الباحثون هذا الأثر إلى مسار الإشارات NF-κB في خلايا الورم، الذي شغّل جين PTGES، خطوة رئيسية في إنتاج البروستاجلاندين E2. أدى حجب هذا المسار إلى خفض مستويات PTGES ومخرجات البروستاجلاندين.
قلب المعادلة بالعلاج المركب
كان السؤال الأكثر عملية: هل يمكن أن يجعل حجب البروستاجلاندينات العلاج الكيميائي أكثر فعالية؟ في الفئران، استخدم العلماء حذفًا جينيًا لـ Ptges في خلايا الورم، أو أجسامًا مضادة تعادل البروستاجلاندين E2، أو أدوية جزيئية صغيرة تثبط سينثاز البروستاجلاندين E. خفّضت كل هذه الطرق مستويات البروستاجلاندينات، وقللت تراكم MDSCs، وأعادت قدرة خلايا CD8+ على القتل ومتانتها الشبيهة بالجذور. عند الجمع بين ذلك وبين السيسبلاتين، أو مع نظام السيسبلاتين-باكليتاكسيل القياسي، بطّأت مثبطات البروستاجلاندينات نمو الورم وانتشاره أكثر من العلاج الكيميائي وحده. تشير البيانات إلى أن القمع المناعي المدفوع بالبروستاجلاندينات ليس هامشًا بل سبب مركزي لهروب الأورام بعد استجابة أولية.
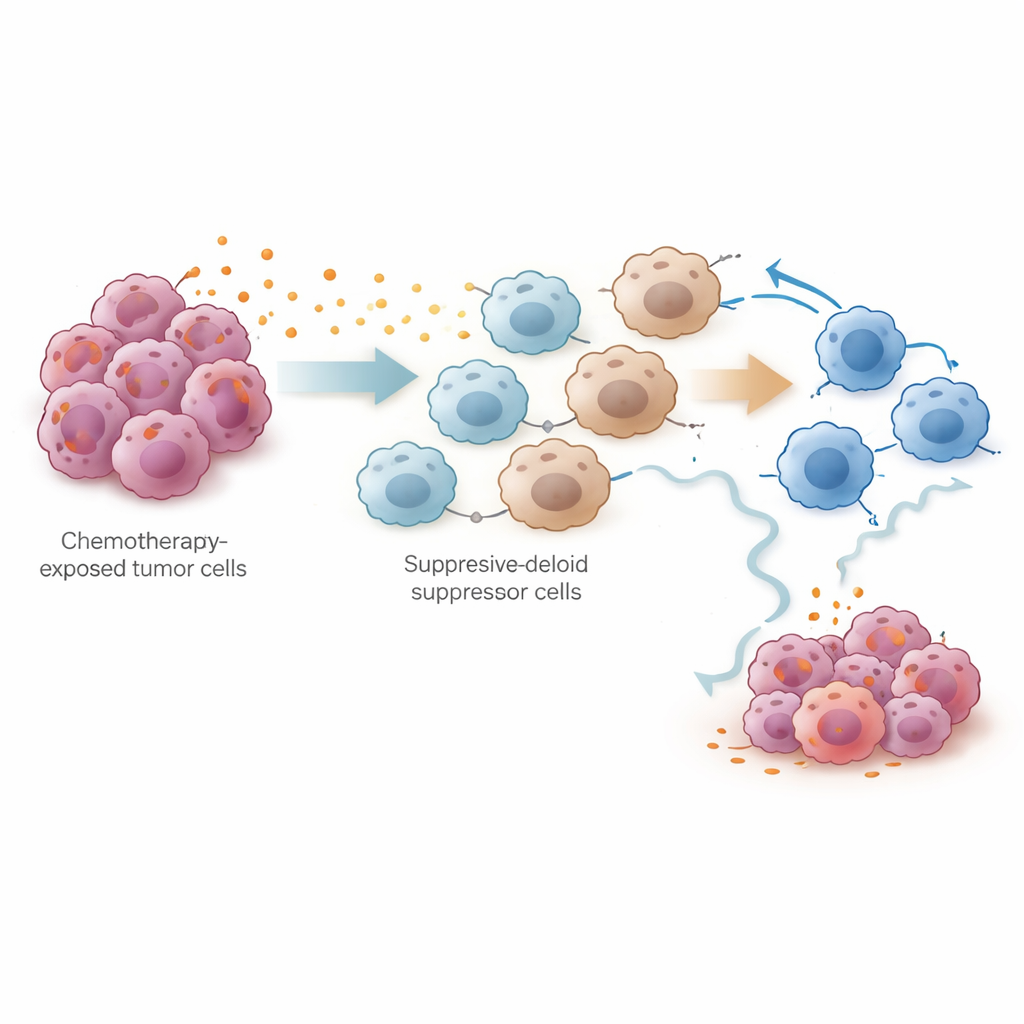
منظور جديد للحفاظ على فعالية العلاج
بعبارة بسيطة، توضح هذه الدراسة أن العلاج الكيميائي يغيّر محيط الورم على مرحلتين: أولًا يضعف السرطان ويحرّك الجهاز المناعي مؤقتًا، ثم يطلق موجة من البروستاجلاندينات التي تستدعي خلايا مكبطة وتجهد قوى الجسم الطبيعية لقتل الورم. من خلال تحديد إنتاج البروستاجلاندينات المدفوع بـ PTGES كسبب رئيسي، تشير الدراسة إلى استراتيجية ملموسة: إقران العلاج الكيميائي البلاتيني القياسي بأدوية تحجب مسارات البروستاجلاندين قد يساعد في الحفاظ على هجوم مناعي قوي وتأخير أو منع الانتكاس في سرطان المبيض. وبينما لا تزال التجارب السريرية مطلوبة، يقدم هذا النهج المركب اتجاهًا واعدًا لتمديد فائدة العلاجات الحالية.
الاستشهاد: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
الكلمات المفتاحية: سرطان المبيض, بيئة الورم الدقيقة, مقاومة العلاج الكيميائي, البروستاجلاندينات, العلاج المناعي