Clear Sky Science · ar
إنزيم غلوتاميت ديكربوكسيلاز 1 (GAD1) يثبط تقدم الورم الأرومي الدبقي من خلال مسار GSK3β/β‑catenin
لماذا تهم هذه الدراسة عن سرطان الدماغ
الورم الأرومي الدبقي هو من أخطر أنواع سرطان الدماغ، حيث يعيش معظم المرضى سنة تقريبًا أو أقل بعد التشخيص. العلاجات الحالية—الجراحة والإشعاع والعلاج الكيميائي—نادراً ما تمنع عودة المرض. تستكشف هذه الدراسة حليفاً مفاجئاً موجوداً بالفعل داخل خلايا الدماغ، وهو إنزيم يُدعى GAD1، وتشير إلى أن تعزيز نشاطه قد يبطئ نمو الورم وانتشاره.
مدافع هادئ داخل خلايا الدماغ
يشتهر GAD1 بدوره في الخلايا العصبية السليمة، حيث يساعد على إنتاج المادة المهدئة في الدماغ، غابا (GABA). تساءل الباحثون عما إذا كان هذا الإنزيم قد يؤثر أيضاً على أورام الدماغ. بمقارنة خلايا الورم الأرومي الدبقي مع خلايا الدعم الدماغي الطبيعية، وجدوا أن مستويات GAD1 كانت أقل باستمرار في الخلايا السرطانية. وأكدت قواعد بيانات المرضى الكبيرة أن الأورام التي تحتوي على كمية أقل من GAD1 ارتبطت بفترات بقاء أقصر، ما يشير إلى أن GAD1 يتصرف كفرامل أكثر منه كمسرع في هذا المرض.
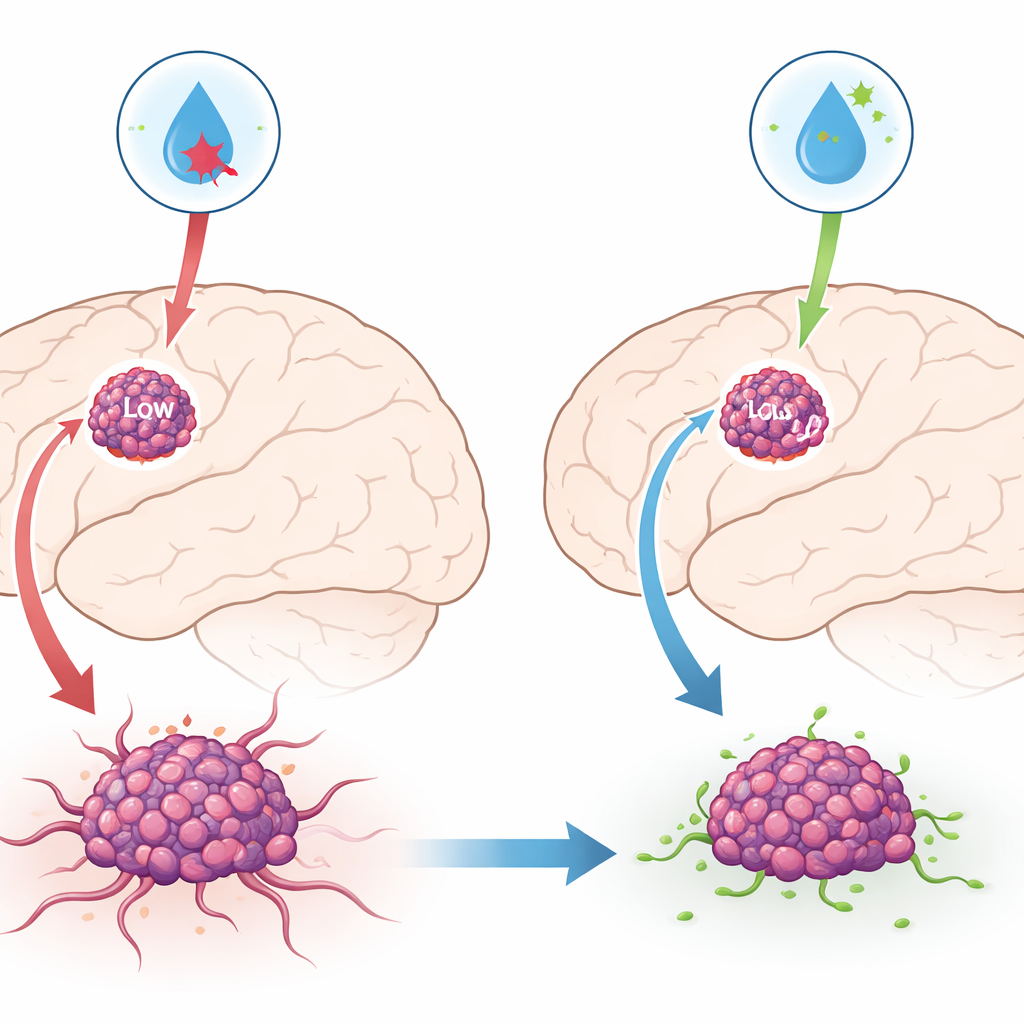
تشغيل الفرامل أو إطفاؤها
لاختبار هذه الفكرة، رفع الفريق أو خفض مستويات GAD1 اصطناعياً في عدة سلالات بشرية من خلايا الورم الأرومي الدبقي نمت في المختبر. عندما عزّزوا GAD1، انقسمت خلايا الورم بوتيرة أبطأ، شكلت مستعمرات أقل، تحركت أقل عبر خدش في طبق الزرع، واجهت صعوبة في الغزو عبر هلام يحاكي النسيج المحيط. وعند تقليل GAD1 حصل العكس: دارت الخلايا بسرعة أكبر، انتشرت بسهولة أكبر، وغزت بعمق أكبر. تُظهر هذه التجارب أن GAD1 يؤثر بقوة في سلوك خلايا الورم الأرومي الدبقي العدواني.
دائرة تحكم خفية داخل الورم
سأل العلماء بعد ذلك كيف يمارس GAD1 هذا التأثير. ركزوا على مسار إشارة داخلي مبني حول بروتين يسمى GSK3β ومنظم نمو معروف، β‑catenin. في العديد من السرطانات، عندما يكون هذا المسار نشطاً جداً، تتكاثر الخلايا وتغزو بسهولة أكبر. وجد الباحثون أن مستويات GAD1 الأعلى خفّضت خطوات رئيسية في هذا المسار، ونتيجة لذلك قللت من كميات بروتينين مهمين يدفعان تقدم دورة الخلية وغزو النسيج. أما خفض GAD1 فشغّل هذا المسار، مستعيداً إشارات النمو والغزو تلك. ومن المثير للاهتمام أن إضافة غابا إضافية، المادة التي يساعد GAD1 عادة على صنعها، لم تُلغي آثار فقدان GAD1، مما يوحي بأن للإنزيم أدواراً إضافية وغير كلاسيكية تؤثر في سلوك الورم.
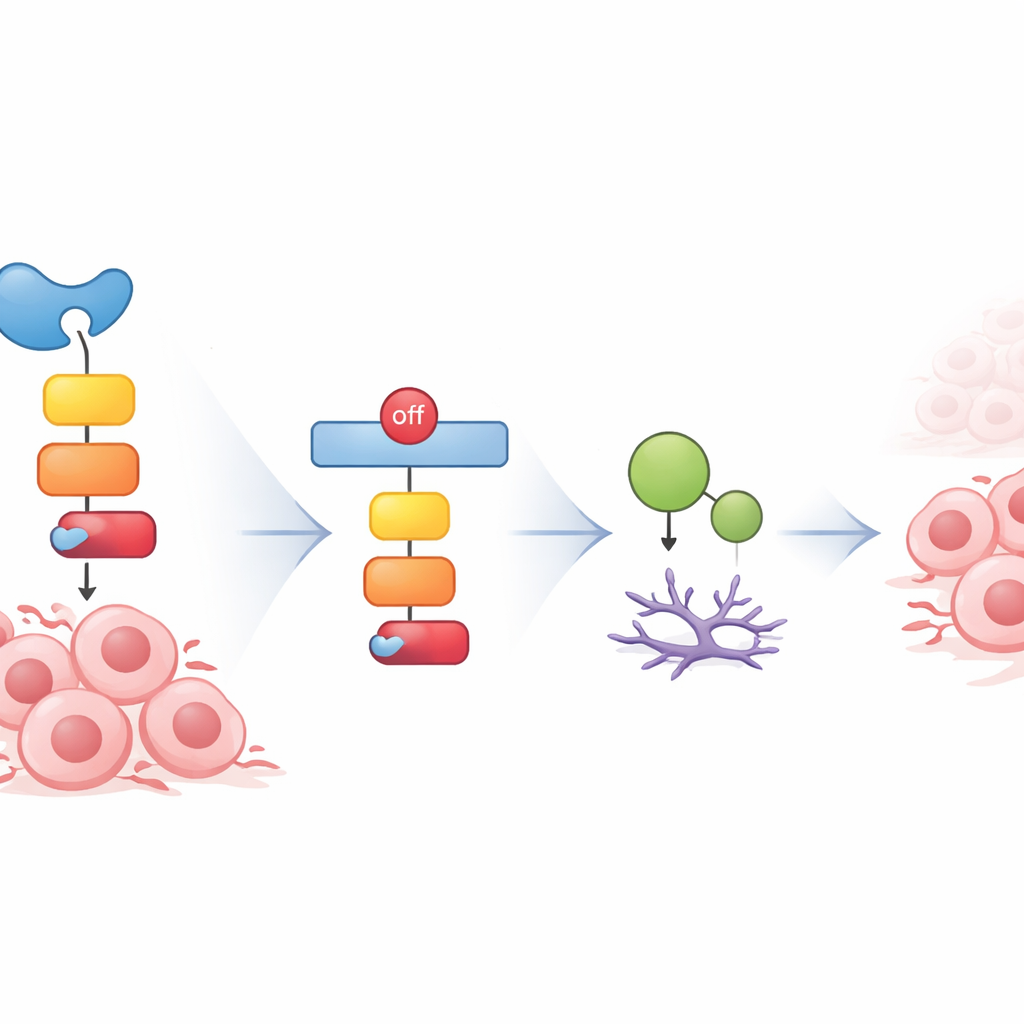
اختبارات دوائية وسمك صغير تكشف التأثير في أنظمة حية
بما أن آثار GAD1 تمتد عبر GSK3β، استخدم الفريق دواءً جزيئياً صغيراً يثبط هذه الكيناز ليروا ما إذا كانوا يستطيعون تحييد أثر فقدان GAD1. في خلايا الورم الأرومي الدبقي التي انخفض فيها GAD1، قلل المثبط التكاثر، وأبطأ تقدم دورة الخلية، وخفض الغزو، مع تخفيض نفس البروتينات التالية للمسار المرتبطة بالنمو والانتشار. وللتقدم إلى ما بعد طبق الزرع، زرع الباحثون خلايا ورمية بشرية معنّمة بالفلوئرسانس في يرقيات زِبْرافِيش شفافة، مكوّنين نموذجاً حياً يمكن فيه مراقبة نمو الورم في الزمن الحقيقي. بقيت الأورام المهيّأة لإنتاج كميات زائدة من GAD1 أصغر وبقِيَت الأسماك على قيد الحياة لفترة أطول، بينما نمت الأورام التي تفتقر إلى GAD1 أكبر وقصّرت من مدة البقاء.
ماذا يمكن أن يعني هذا لعلاجات مستقبلية
تجمع النتائج معاً لتصوّر GAD1 كدرع داخلي يقيّد الورم الأرومي الدبقي عن طريق إضعاف دائرة قوية للنمو والغزو داخل خلايا الورم. عندما يكون GAD1 منخفضاً، تعمل هذه الدائرة بلا رقيب، مما يساعد على تفسير سبب تفاقم سير المرض لدى المرضى ذوي مثل هذه الأورام. وبينما تبقى كثير من الأسئلة—مثل الكيفية الدقيقة لارتباط GAD1 بمفتاح GSK3β—تُبرز هذه الدراسة GAD1 ومساره التالي كبدايات واعدة لعلاجات جديدة. على المدى الطويل، قد توفر أدوية تعزز نشاط GAD1 أو تحاكي تأثيره المهدئ على شبكة الإشارات هذه وسيلة جديدة لإبطاء أحد أكثر سرطانات الدماغ عدوانية.
الاستشهاد: Zheng, Y., Zhong, Z., Zhang, C. et al. Glutamate decarboxylase 1 (GAD1) suppresses the progression of glioblastoma through GSK3β/β-catenin pathway. Cell Death Discov. 12, 132 (2026). https://doi.org/10.1038/s41420-026-02997-0
الكلمات المفتاحية: الورم الأرومي الدبقي, سرطان الدماغ, GAD1, إشارات الورم, نموذج سمك الحبّار الشفاف (زِبْرافِيش)