Clear Sky Science · ar
تسخير البيروباتوزيس في علاج سرطان الثدي: الآليات المناعية واستراتيجيات المواد الحيوية الناشئة
تحويل موت الخلايا إلى سلاح جديد ضد سرطان الثدي
يبقى سرطان الثدي واحداً من أكثر السرطانات شيوعاً وإصراراً على مستوى العالم. العديد من الأورام يتفلت في النهاية من الجراحة والعلاج الكيميائي وحتى العلاجات المناعية الحديثة. تستعرض هذه المقالة فكرة ناشئة: إثارة شكل «ناري» من موت الخلايا يُسمى البيروباتوزيس داخل أورام الثدي بشكل متعمد. من خلال إحداث انفجار الخلايا السرطانية بطريقة متحكم بها ومصحوبة بالالتهاب، يأمل العلماء في قتل الورم مباشرةً وإيقاظ الجهاز المناعي للمشاركة في الهجوم.
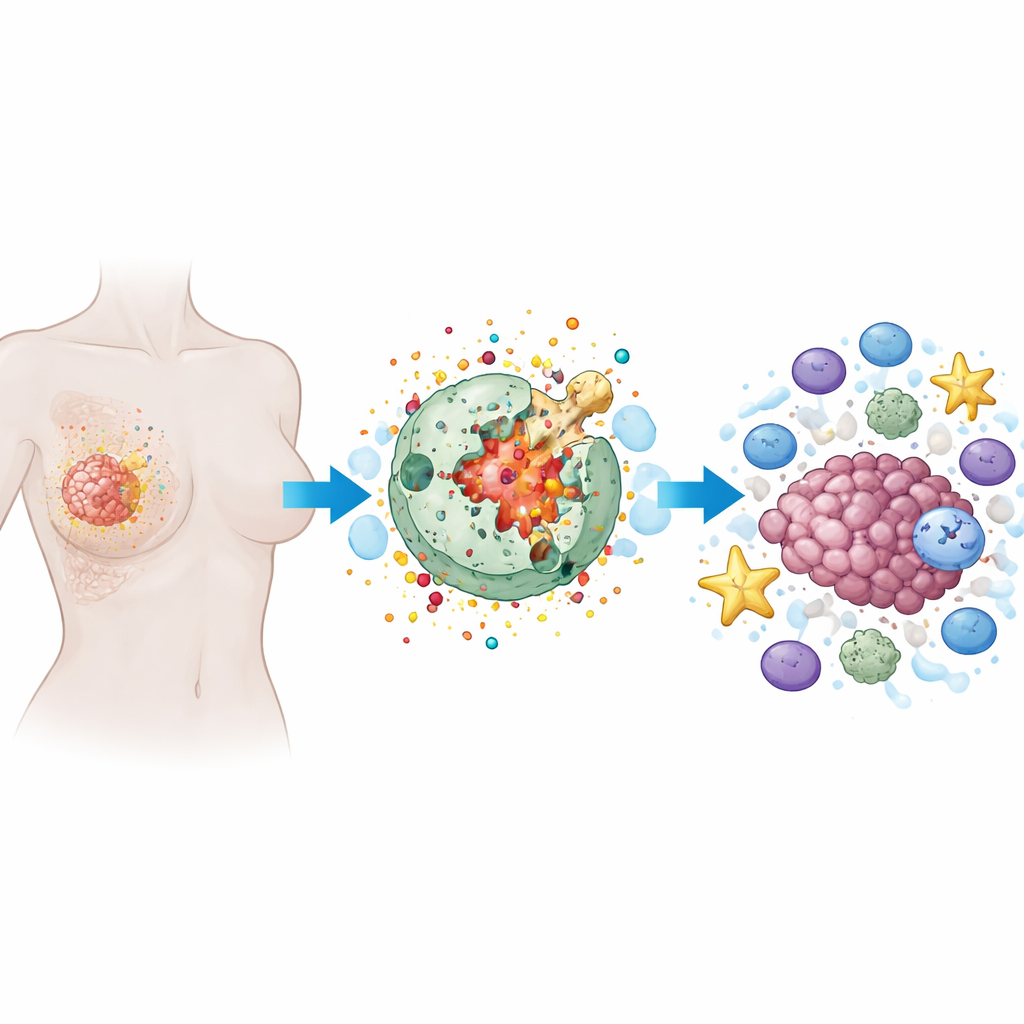
كيف يعمل شكلٌ ناري من موت الخلايا
البيروباتوزيس هو شكل مبرمج من موت الخلايا تتورم فيه الخلية، وتصاب غشاؤها الخارجي بفتحات، وفي النهاية تنفجر وتفرغ محتوياتها. خلافاً لموت الخلايا الهادئ والمرتب الذي يحدث في العديد من العلاجات، فإن البيروباتوزيس صاخب ومُحدث للالتهاب. تلعب بروتينات متخصصة، لا سيما عائلة تُدعى غاسدرمين، دور شبيهة بشحنات تفجيرية صغيرة. عندما تُقطع بواسطة إنزيمات داخلية، تُحدث الغاسدرمين ثقوباً في غشاء الخلية. هذا لا يدمر الخلية السرطانية فحسب، بل يطلق أيضاً إشارات إنذار وجزيئات التهابية يمكنها استدعاء الخلايا المناعية وتنشيطها.
لماذا تُشكّل أورام الثدي تحدياً خاصاً
سرطان الثدي ليس مرضاً واحداً بل مجموعة فرعية ذات سلوكيات مختلفة. بعضها، مثل سرطان الثدي ثلاثي الارتباط السلبي، يفتقر إلى أهداف دوائية شائعة وغالباً ما يقاوم العلاج. تُعتبر العديد من أورام الثدي «باردة مناعياً»، بمعنى أنها تحتوي على عدد قليل من الخلايا المناعية النشطة داخلها. تشرح المراجعة كيف أن ميزات بيئة الورم في الثدي — بما في ذلك الخلايا الداعمة، والخلايا كابحة للمناعة، ونقص الأكسجين الموضعي — يمكن أن تُمهِّد الطريق للبيروباتوزيس، ولكن إذا لم تُتحكم بها جيداً فقد تُحوّل التهابها إلى وقود لنمو الورم وانتشاره. هذه الطبيعة ذات الحافتين تجعل الدقة أمراً بالغ الأهمية.
مفاتيح الغاسدرمين داخل خلايا الورم
ثيمة مركزية في المقال هي كيف تعمل بروتينات الغاسدرمين المختلفة كمفاتيح جزيئية داخل خلايا سرطان الثدي. نسخ مثل GSDMD وGSDME يمكنها تحويل إشارات العلاجات الكيميائية أو الإشعاعية أو هجومات الخلايا المناعية إلى بيروباتوزيس كامل. أخرى، مثل GSDMC وبعض أشكال GSDMB، تكون غالباً مرتفعة في الأورام العدوانية ويمكن أن تُسهِم أو تقيد المرض اعتماداً على كيفية تنشيطها. كثير من سرطانات الثدي تكبت GSDME كيميائياً، مما يُضعف البيروباتوزيس وتفعيل المناعة. قد يُحدّد استعادة أو تحفيز الغاسدرمين المناسب ما إذا كانت المعالجة تقتل عددًا قليلاً من الخلايا فحسب أو تحول الورم بأكمله إلى لقاح موضعي يُنبه الجهاز المناعي.
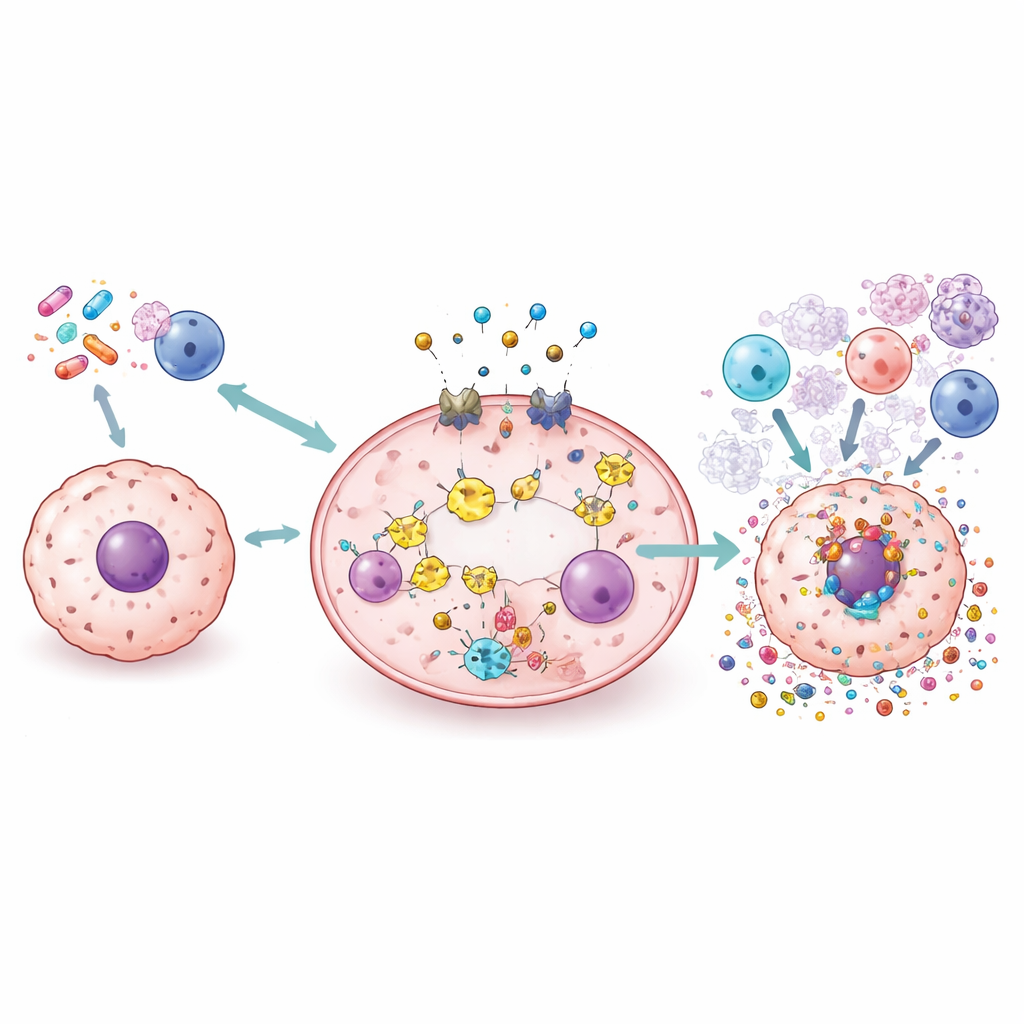
أدوات جديدة: أدوية، جزيئات نانوية، فيروسات وإشعاع
تستعرض المراجعة نطاقاً واسعاً من الاستراتيجيات المدروسة لتسخير البيروباتوزيس بأمان. يمكن إعادة توظيف أدوية قياسية مثل سيسبلاتين ودوكسوروبيسين أو إعادة صياغتها لدفع الخلايا السرطانية نحو انفجار مدفوع بالغاسدرمين بدلاً من الموت الهادئ. يمكن للجزيئات الصغيرة إما تضخيم أو حجب أجزاء من المسار لضبط الالتهاب بدقة. تُصمم الجسيمات النانوية والناقلات المحاكاة للأنسجة لتوصيل العلاج الكيميائي أو أيونات النحاس أو جزيئات مفعلة بالضوء مباشرة إلى الأورام، حيث تُثير البيروباتوزيس مع حماية الأنسجة السليمة. يمكن أيضاً هندسة الفيروسات المحللة للورم والإشعاع أو دمجهما مع عوامل أخرى لاستفزاز البيروباتوزيس وإعادة تشكيل المشهد المناعي للورم، مما قد يجعل أدوية نقاط التفتيش المناعية أكثر فعالية.
موازنة الفائدة القوية مع المخاطر الحقيقية
بما أن البيروباتوزيس مُحدث للالتهاب بشدة، قد تتسبب التفاعلات نفسها التي تُعين الجهاز المناعي على مكافحة السرطان أيضاً في إتلاف الأنسجة الطبيعية أو حتى تعزيز نمو الورم إذا أصبحت مزمنة. يبرز المؤلفون مؤشرات حيوية مبكرة — مثل توقيعات جينية، وأنماط مثيلة، وقطع من بروتينات الغاسدرمين في الدم، وملامح السيتوكينات — التي قد تُساعد في تحديد المرضى الأكثر احتمالاً للاستفادة والذين هم أكثر عرضة لخطر «عواصف السيتوكين» الخطيرة. تُستكشف تصاميم متقدمة في الطب النانوي، وتركيبات أدوية مختارة بعناية، والمراقبة اللحظية لمؤشرات الالتهاب للحفاظ على استجابة حادة لكن مضبوطة.
ماذا قد يعني هذا للمرضى في المستقبل
بعبارات بسيطة، تجادل هذه المراجعة بأن جعل الخلايا السرطانية «تموت بصوت عالٍ» قد يُحوّل رعاية سرطان الثدي. من خلال إثارة البيروباتوزيس في مجموعة محددة بدقة من خلايا الورم، قد ينجح الأطباء في تقليص الورم وإيقاظ استجابة مناعية قوية ودائمة، مما يحول الأورام الباردة إلى أورام ساخنة وأكثر استجابة للعلاجات المناعية الحديثة. ومع ذلك، فإن البيروباتوزيس حليف متقلب: إذا أُطلق بشكل واسع أو لفترة طويلة جداً، فقد يفاقم الالتهاب أو يشجع الخلايا المقاومة على الازدهار. ستركز الأبحاث المستقبلية على رسم خريطة من سيستفيد، وإتقان أنظمة التوصيل المستهدفة، وإجراء تجارب سريرية تزاوجُ بين نهج إثارة البيروباتوزيس والأدوية المناعية. إذا أمكن حل هذه التحديات، فقد يضيف تسخير البيروباتوزيس بعداً قوياً جديداً لعلاج سرطان الثدي.
الاستشهاد: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
الكلمات المفتاحية: البيروباتوزيس, سرطان الثدي, غاسدرمين, البيئة الميكروية للورم, الطب النانوي