Clear Sky Science · ar
ديناميكية مطلقة وسكون نسبي: علاقة التحلل السكري والتنفس التأكسدي في تطور السرطان
لماذا تهم خيارات الطاقة لدى السرطان
تُشبه الخلايا السرطانية الرياضيين ذوي التحمل الشديد: فهي بحاجة دائمة إلى الوقود لتنمو وتنتشر وتتفادى العلاج. تشرح هذه المراجعة كيف تستغل خلايا الورم نظامي طاقة رئيسيين — واحد سريع وآخر عالي الكفاءة — والأهم من ذلك كيف تمزج بينهما وتنتقل من أحدهما إلى الآخر. فهم استراتيجيات الطاقة المتغيرة هذه يوفر منظورًا جديدًا لتشخيص السرطان ومعالجته على امتداد مسار المرض.
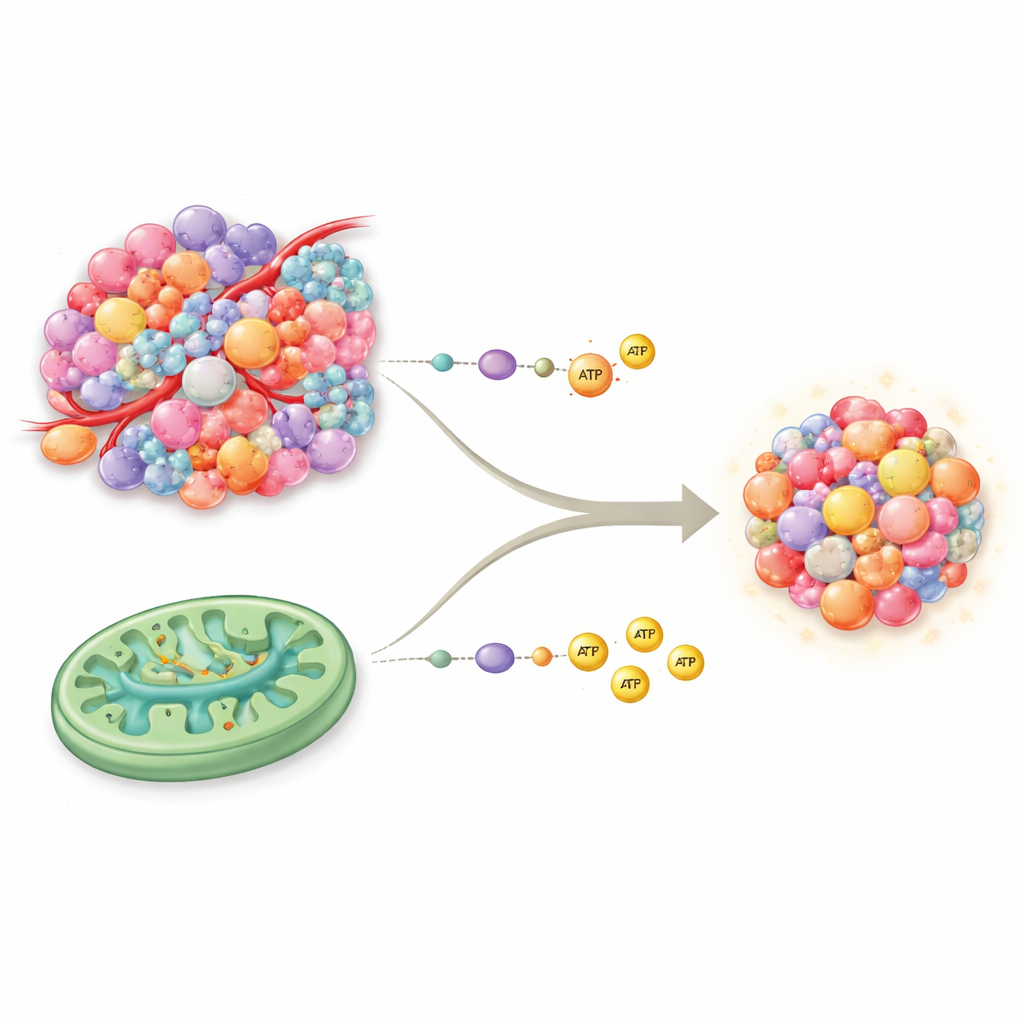
طريقتان رئيسيتان لصناعة الوقود في الخلايا
تنتج خلايانا الطاقة عادةً عبر مسارين أساسيين. التحلل السكري هو النظام السريع، «النقدي الفوري»، الذي يكسر السكر بسرعة لكنه ينتج طاقة قليلة لكل وحدة. أما الفسفرة التأكسدية (OXPHOS) فتجري داخل الميتوكوندريا وتعمل كأنها محطة طاقة عالية الكفاءة، تنتج طاقة بكميات أكبر لكنها تتطلب تزويدًا جيدًا بالأكسجين والمواد المغذية. لعقود، كان يُعتقد أن السرطان يعتمد تقريبًا حصريًا على التحلل السكري حتى في وجود الأكسجين — نمط يُعرف بتأثير واربورغ. تقلبت الأدلة الحديثة هذا التصور المبسط: فالكثير من الأورام لديها ميتوكوندريا تعمل بشكل كامل ويمكنها استخدام الفسفرة التأكسدية ودورة حمض الستريك (TCA) جنبًا إلى جنب مع التحلل السكري، مما يمنحها مجموعة طاقة أغنى وأكثر مرونة مما كان يُعتقد سابقًا.
أنواع خلوية متعددة، اختيارات وقود متعددة
الورم ليس كتلة متجانسة. إنه نظام بيئي صغير يحتوي على خلايا سرطانية، وخلايا داعمة، وأوعية دموية، وخلايا مناعية، لكل منها احتياجات وقود مختلفة. تعيش بعض الخلايا السرطانية بالقرب من الأوعية الدموية وتتمتع بكميات وافرة من الأكسجين والمواد المغذية؛ بينما تُدفن أخرى في مناطق محرومة. نتيجة لذلك، قد تفضل خلايا ضمن نفس الورم التحلل السكري أو تعتمد أساسًا على الفسفرة التأكسدية أو تستخدم الاثنتين معًا. تنشأ هذه التنوعات الأيضية — المسماة التغايرية — من اختلافات في تدفق الدم ومستويات المواد الغذائية ونوع الخلايا والإشارات من البيئة المحيطة. بالإضافة إلى ذلك، غالبًا ما تُظهر الأورام تبادلًا أيضيًا متناغمًا: تصدر الخلايا المعتمدة على التحلل السكري اللاكتات كمنتج شبيه بالفضلات، فتستورده الخلايا المجاورة المعتمدة على الفسفرة التأكسدية وتحرقها كوقود ثمين. يحدث تبادل اللاكتات المماثل بين الخلايا السرطانية والخلايا الداعمة مثل الليفيات وخلايا الأوعية الدموية والخلايا المثبطة للمناعة، ما يساعد الورم جماعيًا على الازدهار ومقاومة العلاج.
تغير دائم: كيف تتحول طاقة الورم عبر الزمن
لا يقتصر استقلاب الأورام على كونه متنوعًا في لحظة معينة فحسب؛ بل هو أيضًا ديناميكي للغاية. مع نمو الأورام، تواجه ظروفًا متغيرة مثل نقص الأكسجين، تراكم الحموضة، نقص المواد المغذية، وتفاوت في صلابة الأنسجة. تحت ظروف قاسية ومنخفضة الأكسجين، يتحول العديد من الخلايا السرطانية نحو التحلل السكري. أما عند تراكم الحموضة أو نفاد السكر، فقد تميل إلى زيادة استخدام الفسفرة التأكسدية. تظهر نفس المرونة خلال مراحل بيولوجية رئيسية: الخلايا المنقسمة بسرعة تعتمد على التحلل السكري لتوفير اللبنات الأساسية للحمض النووي الجديد والدهون والأغشية. بينما الخلايا الساكنة أو الدائرة في الدم غالبًا ما تعتمد أكثر على الفسفرة التأكسدية. أثناء الغزو والانتقال النقيلي، تعدل الخلايا السرطانية اختياراتها من الوقود مرارًا: تفضل بعض المراحل التحلل السكري، بينما تفضل أخرى الفسفرة التأكسدية، والخلايا النقيليَّة التي تستعمر أعضاء جديدة تضبط أيضها ليتوافق مع «تربة» نسيج الوجهة.
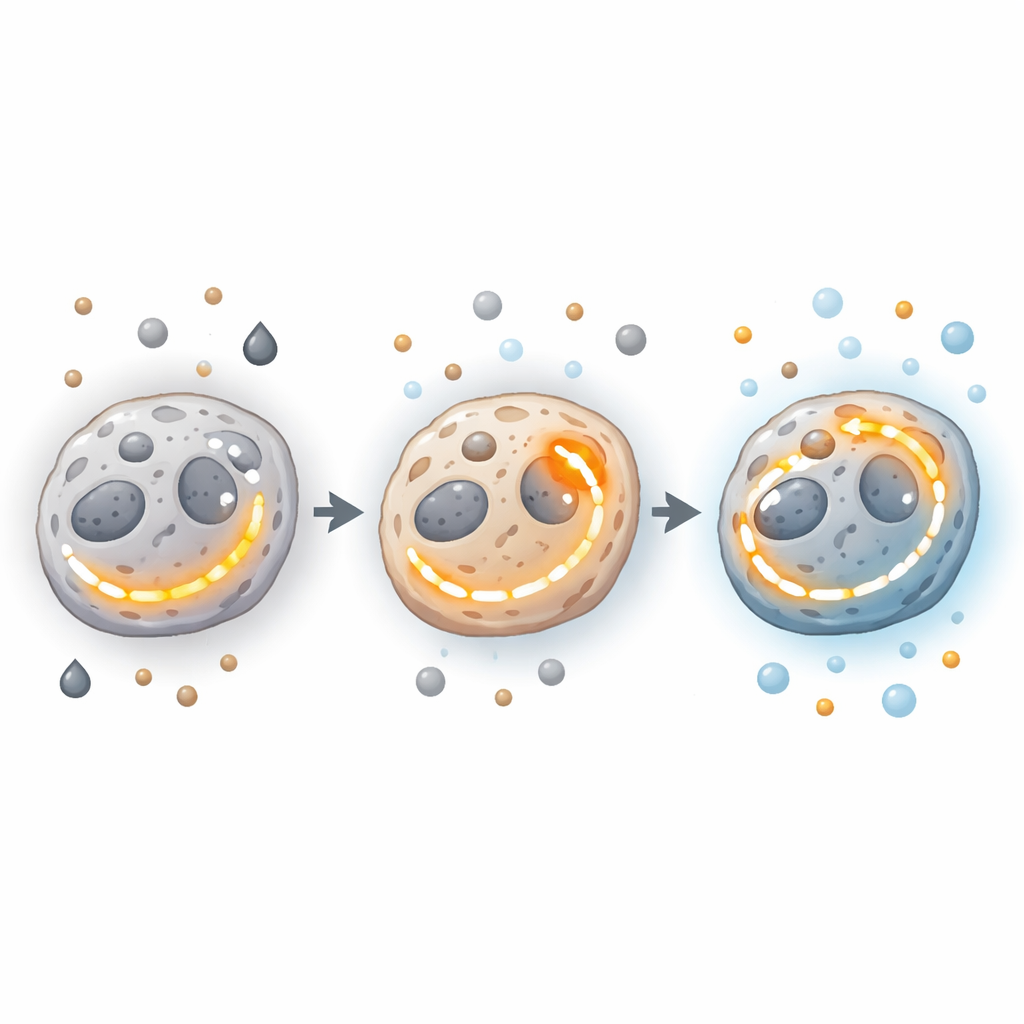
الجينات والإنزيمات ومحطات الطاقة خلف التحول
في عمق آليات الخلية، توجه الجينات والإنزيمات هذه القرارات المتعلقة بالطاقة. يمكن للمولدات المسرطنة ومثبطات الأورم دفع الخلايا نحو التحلل السكري أو الفسفرة التأكسدية، أو تمكينها من زيادة كلا المسارين. قد تتسبب الطفرات أو التغيرات في إنزيمات مفتاحية في دورة TCA، مثل تلك المسؤولة عن السيتريت أو السكسينات أو الإيزوسيتريت، في ميل التوازن، أحيانًا محفزة إشارات تعزز السرطان مثل نمو الأوعية الدموية والغزو. تربط الإنزيمات الموجودة عند مفترقات حاسمة — مثل بيروفات كيناز M2، الذي يساهم في تقرير ما إذا كان الكربون المستمد من السكر سيُستخدم لإنتاج الطاقة أو لبناء مكونات خلوية — بين التحلل السكري ووظيفة الميتوكوندريا. في المقابل، تساهم الاختلافات في عدد الميتوكوندريا وبنيتها وأدائها عبر مناطق الورم في توسيع طيف حالات الطاقة الممكنة.
إعادة التفكير في العلاج عبر هدف طاقة متحرك
نظرًا لأن خلايا الورم قادرة على التنقل بين التحلل السكري والفسفرة التأكسدية، فإن حظر أحد المسارين وحده غالبًا لا يكفي؛ فقد يعيد السرطان توجيه استخدامه للوقود وينجو. يجادل المؤلفون بأن استقلاب الطاقة في السرطان يستقر لفترات قصيرة فقط وأنه متغير وأساسيًا بصورة مستمرة. يقترحون رؤية الأورام عبر «طيف استقلاب الطاقة» الذي ينبغي قياسه مع مرور الوقت، لا مرة واحدة فقط. عمليًا، قد يعني هذا تتبع تفضيلات وقود الورم خلال مراحل المرض المختلفة ومزج مثبطات للتحلل السكري والفسفرة التأكسدية بتراكيب مخصصة. قد تفي مثل هذه الاستراتيجيات العلاجية الديناميكية الموجهة نحو الأيض بغرض قطع مصدر طاقة الورم، وتقليل قدرته على التكيف، وتحسين السيطرة طويلة الأمد على المرض.
الاستشهاد: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
الكلمات المفتاحية: استقلاب السرطان, التحلل السكري, الفسفرة التأكسدية, البيئة الميكروية للورم, المرونة الأيضية