Clear Sky Science · ar
بروتين S100A9 داخل الإكسوسومات يعزز نقائل الرئة لسرطان الغدة المخاطية الكيّفية عن طريق تنشيط الخلايا الليفية المرتبطة بالسرطان
كيف يجد سرطان الغدد اللعابية الصامت طريقه إلى الرئتين
سرطان الغدة المخاطية الكيّفية هو سرطان بطيء النمو لكنه عنيد، غالبًا ما يبدأ في الغدد اللعابية ويظهر لاحقًا في الرئتين، أحيانًا بعد سنوات من استئصال الورم الأولي. بالنسبة للمرضى وعائلاتهم، هذا الانتشار المتأخر مثير للقلق ويصعب التنبؤ به أو منعه. تكشف هذه الدراسة كيف تُعدّ خلايا هذه الأورام نسيج الرئة البعيد بصورة سرية لغزو السرطان، كاشفة عن حوار خفي بين خلايا الورم والخلايا الداعمة المحيطة بها قد يوفر أخيرًا نقاط تدخل علاجية جديدة.
السرطان الذي يبقى ويعاود الظهور
سرطان الغدة المخاطية الكيّفية (ACC) هو سرطان يصيب غدد الرأس والعنق، وخصوصًا الغدد اللعابية. يمكن للجراحة والإشعاع أن يسيطرا على الورم الأساسي في كثير من الأحيان، ومع ذلك يطوّر العديد من المرضى في النهاية نقائل رئوية، وهي السبب الرئيسي للوفاة. الأدوية الحالية للحالات المنتشرة من ACC محدودة، جزئيًا لأن العلماء لا يفهمون بالكامل كيف تتمكن خلايا الورم الأصلية من الاستقرار والنمو في الرئتين. سعى مؤلفو هذه الورقة إلى تحديد الإشارات الأساسية التي تسمح لخلايا ACC بإعادة تشكيل محيطها وتهيئة «تربة» مرحبة للأورام الرئوية المستقبلية.
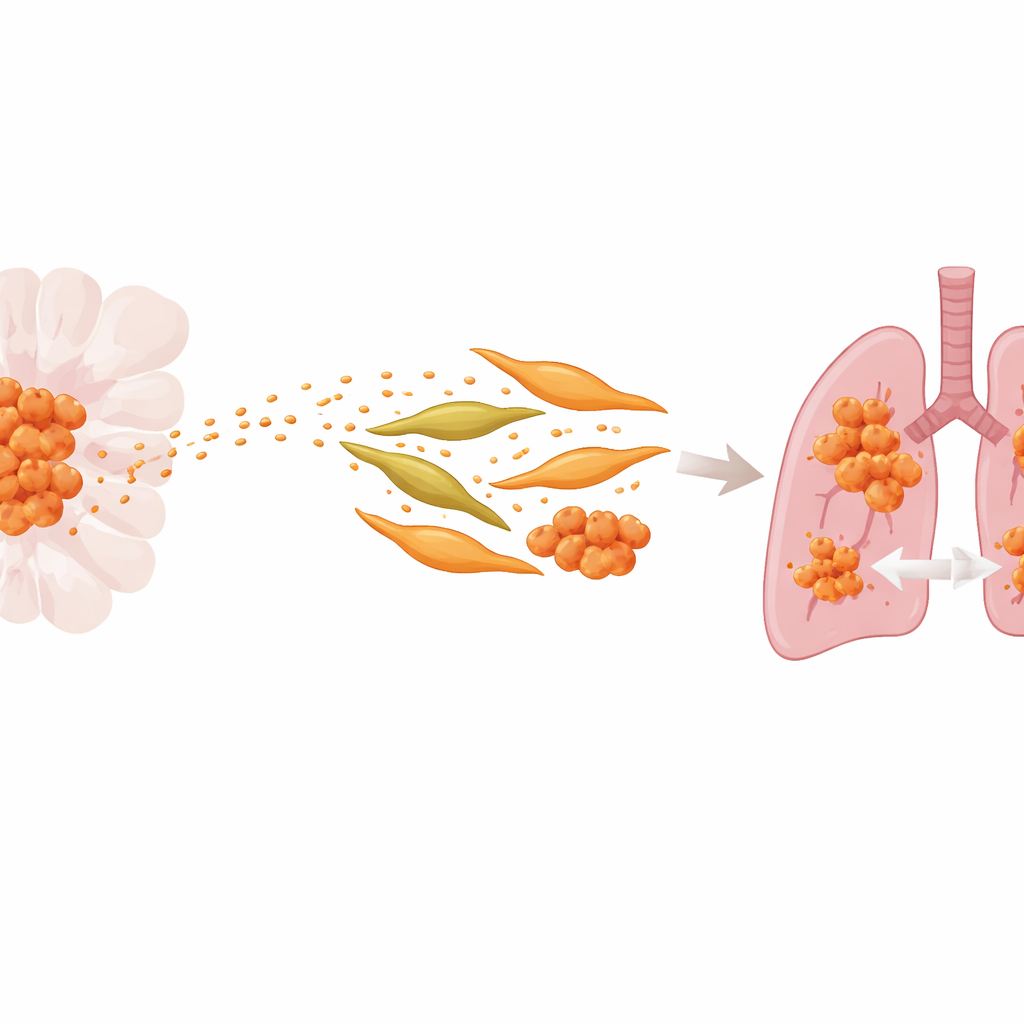
حزم صغيرة ذات تأثير كبير
ركّز الباحثون على الإكسوسومات، فقاعات دقيقة محاطة بغشاء تطلقها خلايا السرطان إلى مجرى الدم. تحمل هذه الحويصلات بروتينات ومادة وراثية يمكنها إعادة برمجة خلايا بعيدة. بمقارنة خط خلوي قياسي لسرطان ACC مع نسخة تم انتقاؤها خصيصًا لقدرتها القوية على الانتشار إلى الرئة، وجد الفريق أن كلًا من الخلايا العدوانية وإكسوسوماتها كانت غنية ببروتين يُدعى S100A9، المرتبط بالالتهاب. كان المرضى الذين احتوت أورامهم وإكسوسومات دَمِهم على S100A9 بكميات أعلى أكثر عرضة لنقائل رئوية وفترات خالية من المرض أقصر، مما يشير إلى أن هذا البروتين يساهم في دفع انتشار السرطان.
إعادة برمجة طاقم الدعم في الورم
باستخدام تحليل تسلسل RNA لخلية مفردة، بنى المؤلفون خريطة مفصّلة لجميع أنواع الخلايا داخل أورام ACC والغدد السليمة المجاورة. اكتشفوا تواصلًا مكثفًا بين خلايا الظهارة الورمية والخلايا الليفية المجاورة، وهي الخلايا البنيوية التي تنتج النسيج الضام. في السرطان، يمكن «تجنيد» هذه الخلايا الليفية وتحويلها إلى خلايا ليفية مرتبطة بالسرطان (CAFs)، التي تزيد من صلابة الأنسجة، وتغذي الالتهاب، وتساعد خلايا السرطان على الحركة. أظهرت الدراسة أن إكسوسومات غنية بـS100A9 من خلايا ACC العدوانية يمكنها تحويل الخلايا الليفية الطبيعية إلى خلايا CAFs منشطة: أصبحت أكثر تقلصًا وأكثر حركة، وبدأت تنتج إنزيمات وجزيئات التهابية تعيد تشكيل النسيج وتعزز نمو الورم.
من إشارات محلية إلى مستعمرات رئوية
تساءل الفريق بعد ذلك عما إذا كانت هذه الخلايا الليفية المنشّطة بواسطة الإكسوسومات تسهل بالفعل استعمار ACC للرئتين. في نماذج الفئران، أدى حقن إكسوسومات محمّلة بـS100A9 في مجرى الدم إلى تمهيد الرئتين: حيث أظهرت الخلايا الليفية هناك مؤشرات تنشيط، وبدأ نسيج الرئة في التعبير عن عوامل مرتبطة بتكوين أوعية دموية جديدة وتحلل المصفوفة. عندما أُدخلت خلايا ACC لاحقًا، طورت الفئران المعالجة مسبقًا بإكسوسومات S100A9 نقائل رئوية أكثر وحجمًا أكبر. أظهرت تحليلات إضافية أن هذه العملية اعتمدت على سلسلة من الإشارات الالتهابية التي تتركز حول الرسول IL-17، جنبًا إلى جنب مع TNF وNF-κB، والتي معًا ضاعفت تنشيط الخلايا الليفية وأعادت تشكيل الميكروبيئة الرئوية.
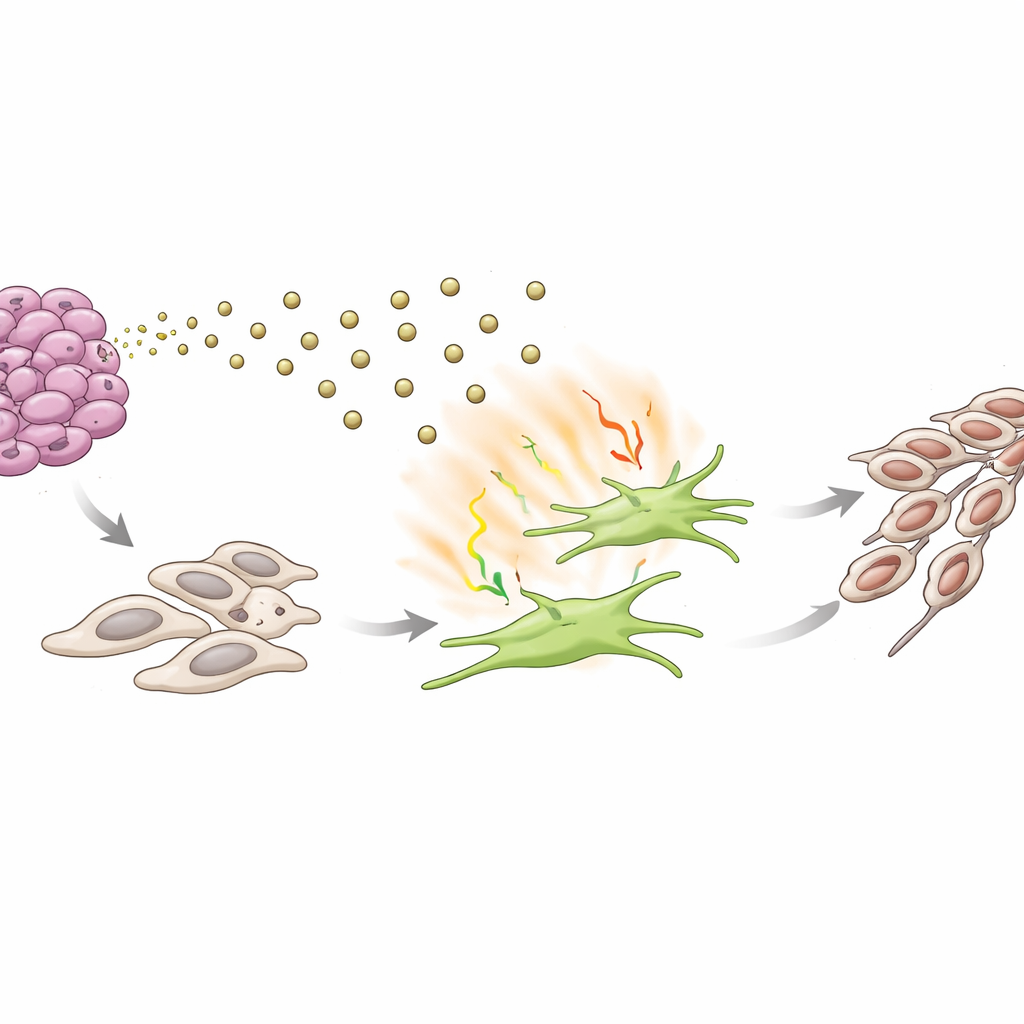
دورة شريرة تدفع تحول شكل السرطان
في أنظمة الثقافة المشتركة المخبرية، جعلت الخلايا الليفية التي «تعلّمت» من إكسوسومات غنية بـS100A9، أو من طريق إشارة محوره IL-17، خلايا ACC المجاورة أكثر عدوانية. أصبحت خلايا السرطان أفضل في الحركة، والغزو عبر الحواجز، والتكوّن إلى مستعمرات، وتبنّت هيئة أكثر حركة وشبيهة بالمغزل المرتبطة بالتحول الطفاري الظهاري اللحائي، وهي خطوة أساسية نحو النقائل. أدت ممانعة IL-17 بواسطة جسم مضاد معادل إلى عكس العديد من هذه التغيرات، بينما دفعت إضافة IL-17 المنقى بمفرده خلايا ACC نحو هذه الحالة الأكثر غزوًا. معًا، ترسم هذه النتائج حلقة تعزيز ذاتي: ترسل خلايا الورم S100A9 في الإكسوسومات لتنشيط الخلايا الليفية؛ وتُطلق الخلايا الليفية المنشّطة IL-17 وإشارات أخرى تجعل خلايا الورم أكثر ميلاً للانتشار.
كسر حلقة الاتصال الخفية
لغير المتخصص، الفكرة الأساسية أن ACC لا ينتشر إلى الرئتين بالمصادفة. بدلاً من ذلك، يدرب الورم الأصلي سرًا الخلايا الداعمة والأنسجة البعيدة لمساعدته على النمو في مكان آخر، مستخدمًا طرودًا دقيقة مملوءة بالبروتين كرسائل. تحدد هذه الدراسة S100A9 ومسار إشارة IL-17 اللاحق كمراكز أساسية في تلك العملية. عبر استهداف هذا المحور الاتصالي — إما عن طريق حجب S100A9، أو كبح إشارات IL-17، أو تعطيل تنشيط الخلايا الليفية — قد تتمكن العلاجات المستقبلية من مقاطعة «مرحلة الإعداد» لنقائل الرئة، مما يمنح الأطباء طرقًا جديدة لمنع عودة هذا السرطان الهادئ لكنه الخطر بعيدًا عن موطنه الأصلي.
الاستشهاد: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
الكلمات المفتاحية: سرطان الغدة المخاطية الكيّفية, الإكسوسومات, الخلايا الليفية المرتبطة بالسرطان, نقائل الرئة, محور S100A9 IL-17