Clear Sky Science · ar
الانتقال البطاني اللحمي المحفز عبر APOA2 وإعادة برمجة استقلاب الشحوم في السرطان تمنح مقاومة للأدوية المضادة لتكوّن الأوعية عبر TGF-β
لماذا يهم هذا الاكتشاف المرضى
يتجه الأطباء بشكل متزايد إلى استخدام أدوية تجوع أورام الكبد عن طريق قطع إمدادها بالدم، ومع ذلك يتوقف استجابة العديد من المرضى لهذه الأدوية بعد فائدة أولية. تطرح هذه الدراسة سؤالاً ملحاً: لماذا تصبح بعض سرطانات الكبد مقاومة لهذه العلاجات التي تمنع الأوعية الدموية، وكيف يمكننا التغلب عليها؟ يكشف الباحثون عن شراكة مخفية بين بروتين دهنوي في الدم وإشارة نمو قوية تسمح للأورام بإعادة توصيل أوعيتها الدموية وإعادة برمجة استخدام الطاقة لديها، مما يشير إلى نهج علاجي مختلف لسرطان يصعب علاجه.
ورم يتعلم العيش بدون شريان حياتيه المعتاد
يعتمد سرطان الكبدة البدئي، الشكل الأكثر شيوعاً من سرطان الكبد، اعتماداً كبيراً على الأوعية الدموية الجديدة للنمو. تُصمم الأدوية القياسية للحالة المتقدمة لحجب مسار رئيسي لنمو الأوعية يركّز على VEGF ومستقبله VEGFR2. ومع ذلك، تستمر الأورام في الانتعاش لدى الكثير من المرضى رغم هذه الأدوية. من خلال مقارنة عينات أورام من مرضى استجابوا أو لم يستجيبوا للعقار المضاد لتكوّن الأوعية apatinib، وجد المؤلفون أن جيناً واحداً، APOA2، تميز بشكل واضح. كانت مستويات APOA2 أعلى بكثير في أورام المرضى المقاومين؛ وهو بروتين معروف بدوره في نقل الدهون في الدم. أثار ذلك احتمال أن APOA2 قد يساعد الأورام على التحايل على الأدوية التي تستهدف الأوعية.
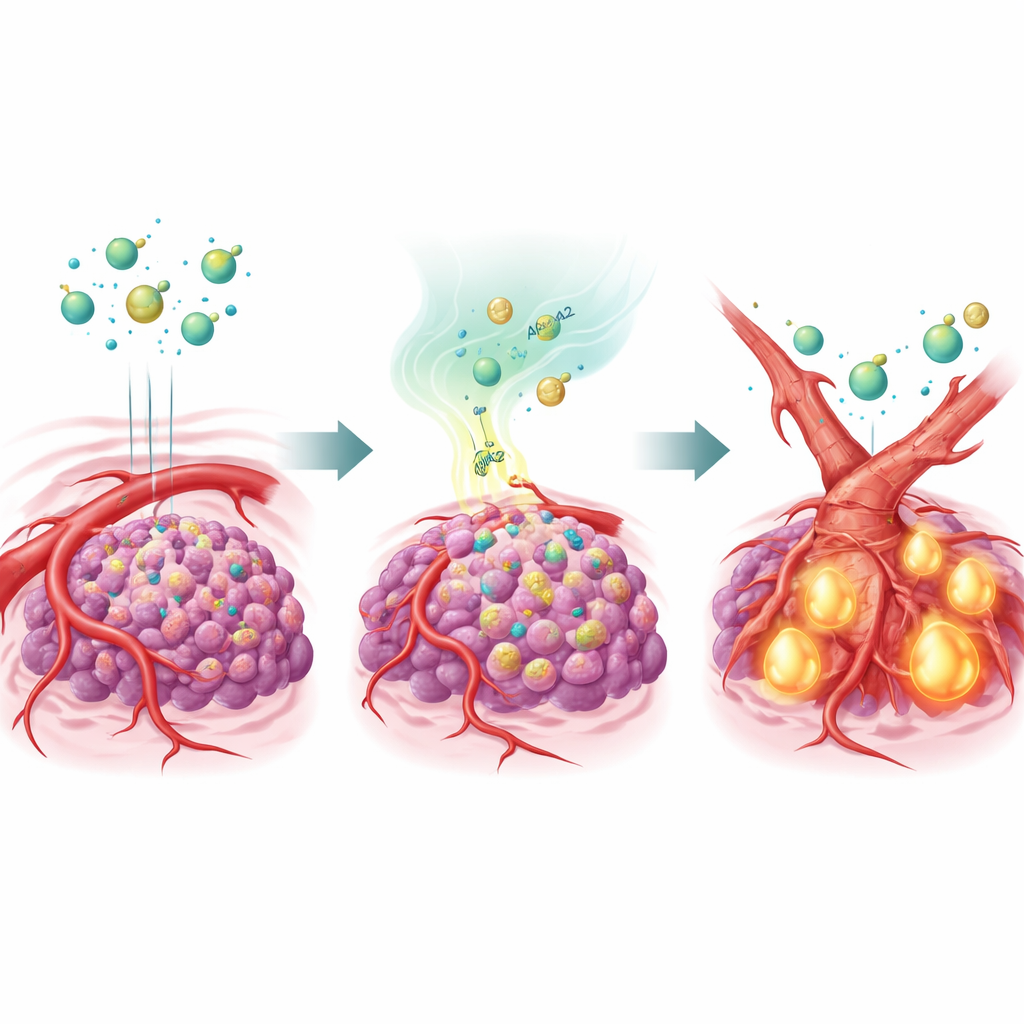
بروتين ناقل للدهون يعيد تشكيل الأوعية الدموية
لاختبار هذه الفكرة، مهندَس الفريق خلايا سرطان الكبد لزيادة إنتاج APOA2 وزرعوها في فئران. عندما عولجت هذه الأورام الغنية بـAPOA2 بعدة أدوية مضادة لتكوّن الأوعية، تجاهلت العلاج إلى حد كبير: بقيت أوعيتها الدموية قائمة واستمرت الأورام في النمو. أظهر التحليل التفصيلي أن إشارة رئيسية تسمى TGF-β كانت مفعلة بشدة في هذه الأورام، وكانت مستوياتها مرتفعة في كل من بيئة الورم ودم الحيوانات. أثرت TGF-β على الخلايا المُبطِنة للأوعية الدموية، ودَفَعَتْها إلى تغيير هويتها في عملية تُعرف بالانتقال البطاني إلى اللحمي (endothelial-to-mesenchymal transition). ومع تحولها نحو حالة أكثر شبيهة بالنسيج الندبي واللحمي، فقدت هذه الخلايا جزءاً كبيراً من مستقبل VEGFR2، وهو الهدف الذي تصمم له الأدوية المضادة لتكوّن الأوعية. عملياً، أعادت الأوعية تشكيل نفسها إلى شكل لم تعد الأدوية قادرة على استهدافه.
تحويل استقلابي يحافظ على تغذية الخلايا السرطانية
لم تنتهِ القصة عند جدار الوعاء. أعادت نفس إشارة TGF-β المدفوعة بواسطة APOA2 أيضاً برمجة كيفية حصول الخلايا السرطانية على طاقتها. بدلاً من الاعتماد أساساً على تحلل السكر، بدأت الخلايا ذات مستويات APOA2 العالية في سحب مزيد من الأحماض الدهنية الحرة من محيطها واحتراقها في المتقدرات عبر أكسدة الأحماض الدهنية. أظهرت تجارب قياس استخدام المغذيات واستهلاك الأوكسجين أن هذه الخلايا أصبحت أكثر اعتماداً على الدهون كمصدر للطاقة وأنتجت مزيداً من ناقلات الطاقة الخلوية (ATP). سمح هذا التحول لخلايا الورم بالانقسام بسرعة وتجنب موت الخلايا، حتى عندما كان إمداد الدم مضغوطاً بفعل العلاج المضاد لتكوّن الأوعية.
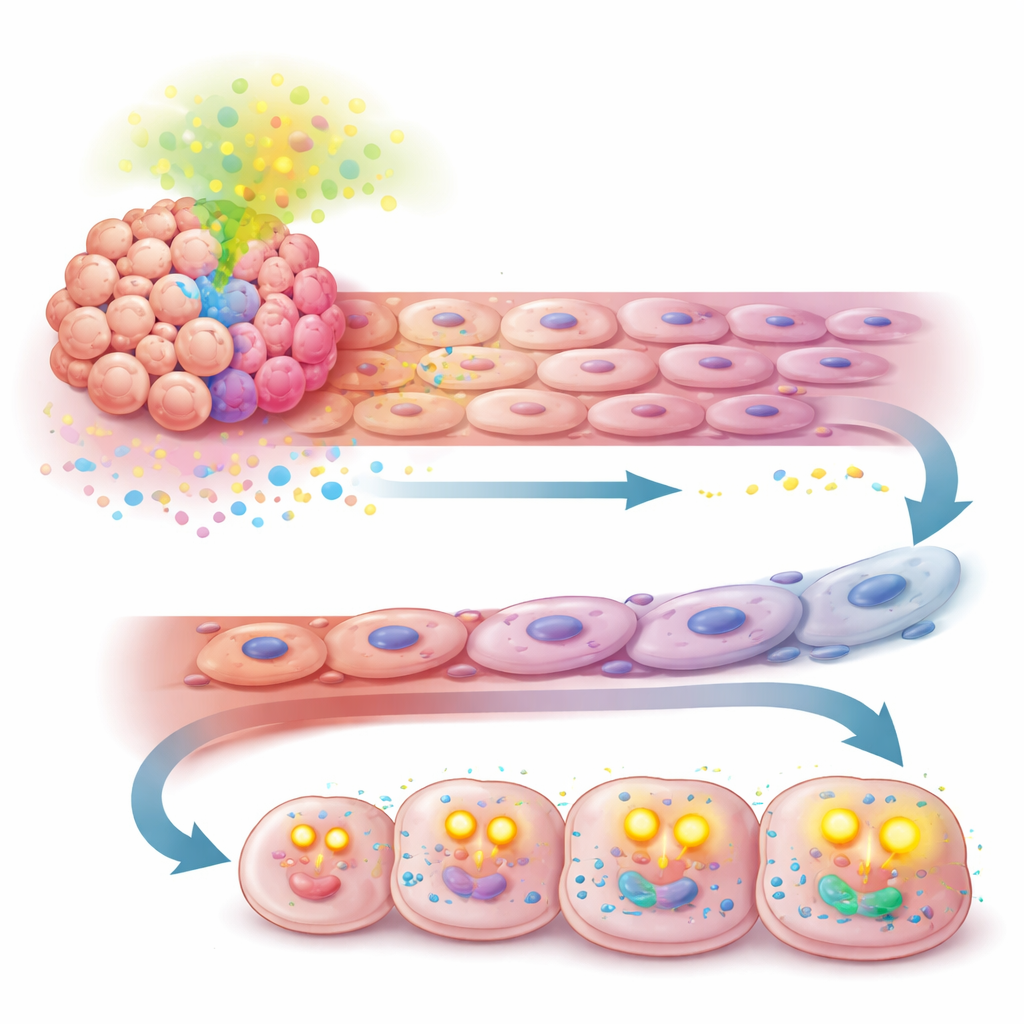
تحويل نقطة ضعف إلى هدف علاجي جديد
بشكل حاسم، عندما قام الباحثون بحجب TGF-β، تفككت المزايا التي يمنحها APOA2. أدى تثبيط هذه الإشارة في نماذج الفئران إلى تقليل تغيرات الأوعية غير الطبيعية، واستعادة الحساسية للعلاج، وإبطاء نمو الورم. وما هو أكثر تشجيعاً أن جسم مضاد مزدوج يحجب TGF-β ونقطة المراقبة المناعية PD-1 في آن واحد عمل بشكل أفضل من أي نهج منفرد في الأورام ذات مستوى APOA2 العالي. تشير هذه النتائج إلى أنه في شريحة من سرطانات الكبد المميزة بمستويات APOA2 المرتفعة، يكون المرض قد غير بهدوء اعتماده من مسار VEGF المعتاد إلى مسار متمركز حول TGF-β يدعم كل من الأوعية الدموية واستقلاب الورم.
ماذا يعني هذا لرعاية سرطان الكبد في المستقبل
للشخص العادي، الرسالة الأساسية هي أن بعض أورام الكبد تهرب من أدوية الأوعية الحالية عبر إعادة توصيل كل من شبكاتها وأنظمة الطاقة فيها. يقوم بروتين مرتبط بالدهون، APOA2، بتعزيز إشارة TGF-β، والتي بدورها تخفي الأوعية الدموية بحيث لا تستطيع الأدوية الحالية رؤيتها وتعلّم الخلايا السرطانية الاعتماد على الدهون بدلاً من السكر. تقترح الدراسة أن فحص الأورام بحثاً عن APOA2 قد يميّز المرضى الذين من غير المرجح أن يستفيدوا من الأدوية المضادة لتكوّن الأوعية التقليدية لكن قد يستجيبون لأدوية تُثبّط TGF-β، خصوصاً عند الجمع بينها وبين العلاجات المناعية الحديثة. باختصار، عبر الكشف عن كيفية تكيف الأورام، يشير هذا العمل إلى استراتيجية أكثر تخصيصاً تهاجم كلاً من الأوعية ومصدر الطاقة التي تعتمد عليه هذه السرطانات المقاومة.
الاستشهاد: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
الكلمات المفتاحية: سرطان الكبدة البدئيّ (هبدات), مقاومة مضادات الأوعية, APOA2, إشارة TGF-beta, استقلاب الشحوم في السرطان