Clear Sky Science · ar
KCTD1 يثبّت c-Myc لزيادة تنظير PD-L1 وكبت المناعة المضادة للأورام في سرطان الكبد الكبدي
لماذا هذا مهم لرعاية السرطان في المستقبل
العديد من الأشخاص المصابين بسرطان الكبد لا يستفيدون من أكثر العلاجات المناعية إثارة اليوم، المصممة لتحرير خلايا T الخاصة بالجسم ضد الأورام. تستكشف هذه الدراسة سبب تمكن شكل شائع من سرطان الكبد، سرطان الكبد الكبدي، من الاختباء من الهجوم المناعي حتى أثناء العلاج—وتحدد مفتاحًا جزيئيًا جديدًا، يُسمى KCTD1، يمكن أن يجعل أدوية المناعة الحالية تعمل بشكل أفضل.
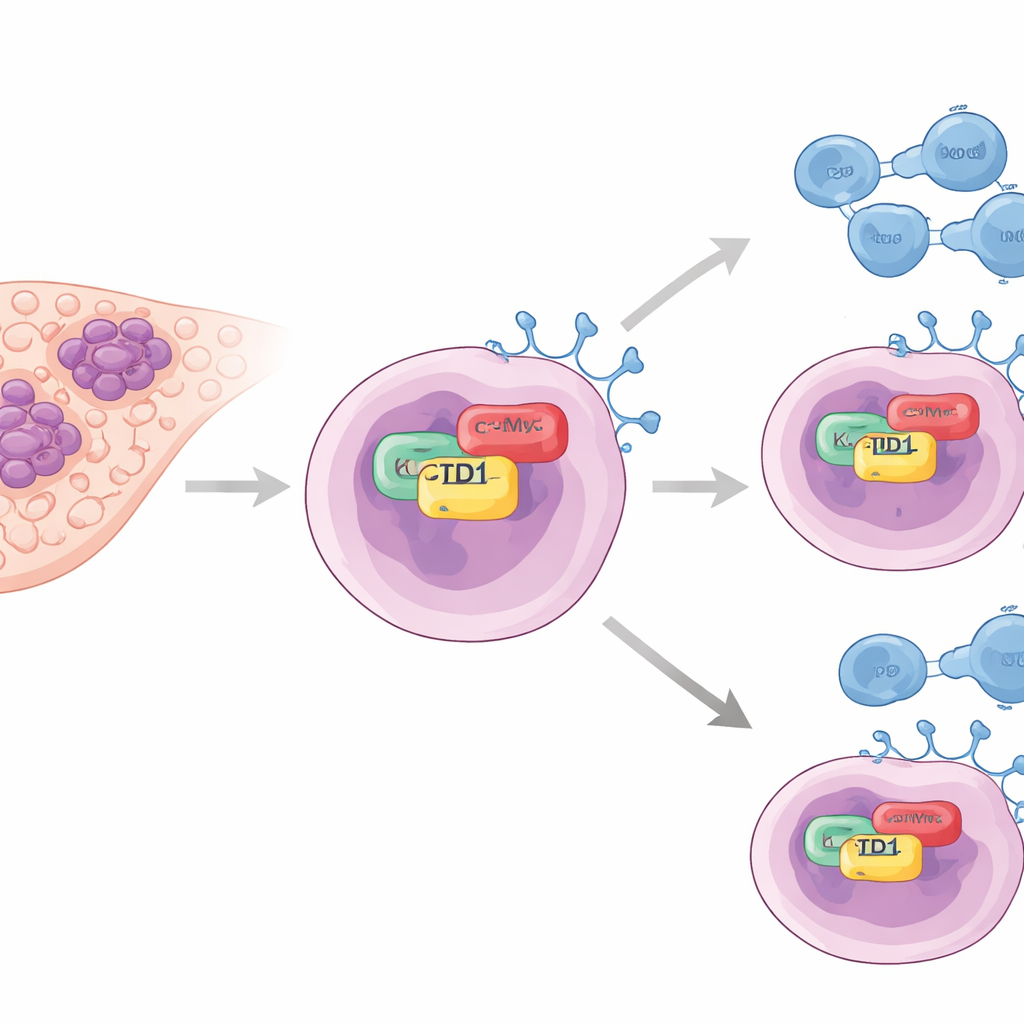
مساعد خفي لمفاتيح الإيقاف في الورم
ركّز المؤلفون على بروتين يُدعى KCTD1، المرتبط سابقًا بنمو أورام الكبد ولكنه لم يُدرس جيدًا في هروب الجهاز المناعي. في عينات الأورام من المرضى، وجدوا أن مستويات KCTD1 كانت أعلى بشكل ملحوظ في الأنسجة الكبدية السرطانية مقارنة بالكبد الطبيعي. والأهم من ذلك، أن الأورام الغنية بـ KCTD1 كانت أيضًا ذات مستويات عالية من PD-L1، وهو بروتين سطحي على خلايا السرطان يرتبط بـ PD-1 على خلايا T ويخبر الجهاز المناعي فعليًا بالتراجع. المرضى الذين كانت أورامهم تحتوي على KCTD1 أقل كانوا يميلون إلى العيش لفترات أطول، مما يشير إلى أن هذا البروتين مرتبط بشدة المرض وقوة الدرع المناعي للورم.
ربط النقاط الجزيئية داخل خلايا السرطان
لفهم كيفية تعزيز KCTD1 لـ PD-L1، لجأ الفريق إلى خطوط خلايا سرطان الكبد المزروعة في المختبر. عندما خفّضوا KCTD1، انخفضت مستويات بروتين PD-L1 وتعرض ما تبقى منه لتحلّل أسرع، مما يدل على أن KCTD1 يساعد في تثبيت PD-L1 بدلًا من مجرد تشغيل جيناته. باستخدام تجارب السحب البيوكيميائية والمجهرية الفلورية، أظهروا أن KCTD1 يرتبط فعليًا بسائق سرطاني أساسي آخر، البروتين الورمي c-Myc، داخل نواة الخلية. يحدث هذا التفاعل من خلال مناطق تلامس محددة في كلا البروتينين ويؤدي إلى استقرار أكبر لـ c-Myc، والذي بدوره يعزز إنتاج PD-L1. عندما نُقص c-Myc بمفرده، انخفض PD-L1 حتى لو كان KCTD1 وافرًا، مما يضع c-Myc كرابط الوسيط الحاسم في سلسلة KCTD1–c-Myc–PD-L1.
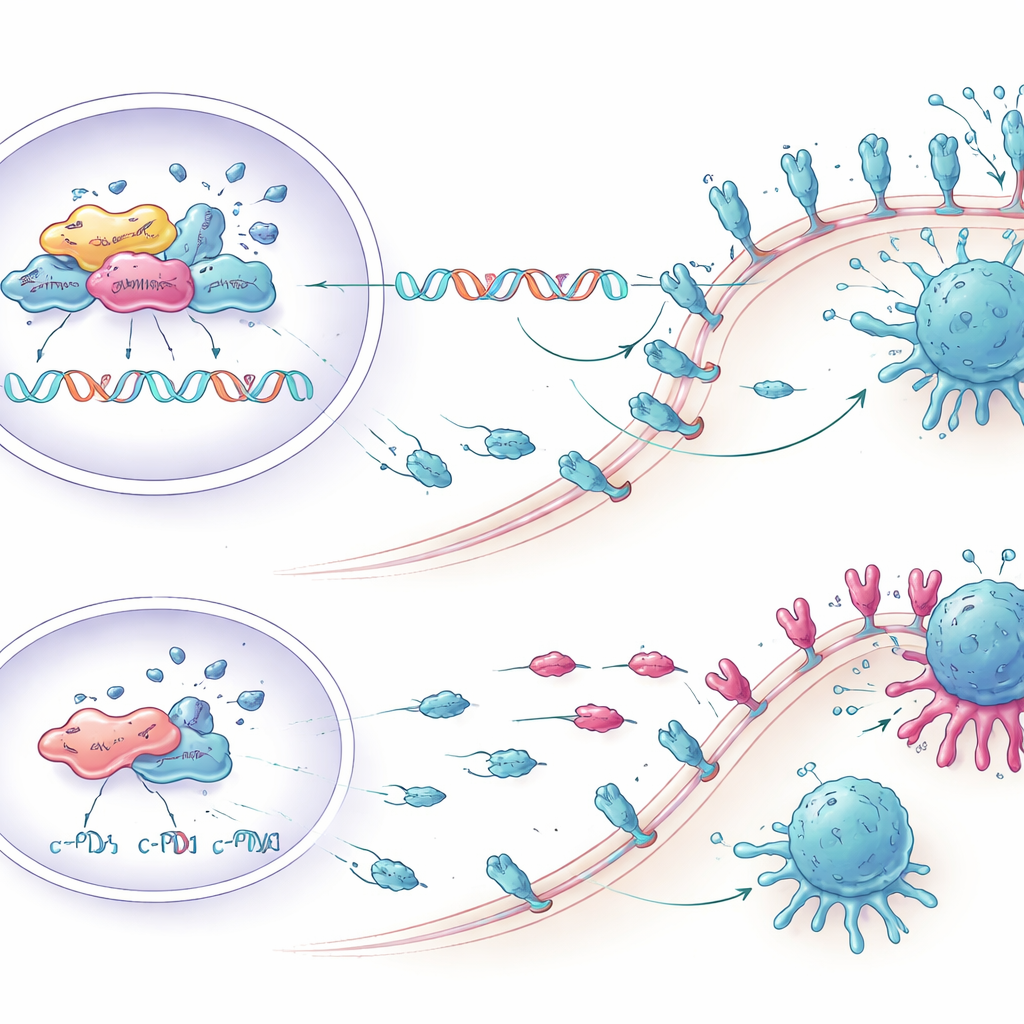
إيقاظ خلايا T مجدداً في المختبر
ثم تساءل الباحثون عما إذا كان خفض KCTD1 يمكن أن يقوّي فعلاً الهجوم المناعي. شاركوا خلايا سرطان الكبد البشرية مع خلايا مناعية مأخوذة من متبرعين بالدم. الخلايا السرطانية المُعدلة لتحتوي على KCTD1 أقل، وبالتالي PD-L1 أقل، حفّزت استجابات أقوى من خلايا CD8 T—القاتلة الرئيسية للخلايا السرطانية في الجهاز المناعي. أفرز عدد أكبر من هذه الخلايا جزيئات التهابية مثل TNF-α والإنترفيرون-غاما، واظهرت مؤشرات أعلى للنمو والنشاط، وكانت تحمل دلائل أقل على الإرهاق. ونتيجة لذلك، خضعت نسبة أكبر من خلايا الورم للموت المبرمج عندما تم قمع KCTD1، مما يبرهن أن التغيرات الجزيئية تحولت إلى زيادات فعلية في القتل المناعي.
اختبار الآلية في الفئران
لمعرفة ما إذا كان النمط نفسه ينطبق في كائنات حية، زرع الفريق خلايا سرطان الكبد الفأرية التي تفتقر إلى KCTD1 مباشرة في كبد الفئران. تشكلت أورام ذات KCTD1 منخفضة على شكل عقيدات أقل وحجمًا أصغر، وأظهرت انقسامًا خلويًا أبطأ، وكان بها المزيد من خلايا السرطان التي تخضع للموت الخلوي. كما عبرت هذه الأورام عن مستويات أقل من c-Myc وPD-L1. إزالة خلايا CD8 T من الفئران ألغت جزءًا كبيرًا من هذه الفائدة، مما يشير إلى أن تباطؤ نمو الورم اعتمد بدرجة كبيرة على نشاط خلايا T. أخيرًا، عندما جمع الباحثون خفض KCTD1 مع جسم مضاد مضاد لـ PD-1—دواء تحقق المناعي موجود—كان لدى الفئران أقل عبء ورمي وأعلى مستويات من خلايا CD4 وCD8 T متسللة في أورامها.
ما الذي قد يعنيه هذا للمرضى
مجتمعًا، تكشف النتائج أن KCTD1 يعمل كمنسق مركزي يثبّت c-Myc، ويعزز PD-L1 على خلايا سرطان الكبد، ويضعف هجوم خلايا CD8 T. تعطيل هذا المسار يجعل الأورام أكثر عرضة للجهاز المناعي وأكثر استجابة لأدوية حاصرة لـ PD-1 في الفئران. للمرضى، يشير هذا إلى أن الأدوية المستهدفة لـ KCTD1 أو لسطح تلاقيه مع c-Myc قد تُقرَن في المستقبل بالعلاجات المناعية الحالية لمساعدة المزيد من مرضى سرطان الكبد على الاستفادة من تحكم مناعي دائم في مرضهم.
الاستشهاد: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
الكلمات المفتاحية: سرطان الكبد الكبدي, المناعة المناعية للأورام, مسار PD-1 PD-L1, إشارة c-Myc, المناعة الخلوية التائية ضد الأورام