Clear Sky Science · ar
رؤى جزيئية حول التأثيرات المضادة للسرطان لدى سيلودوسين: استراتيجية واعدة لإعادة توظيف الدواء لعلاج سرطان الثدي
لماذا يحظى دواء قديم باهتمام جديد
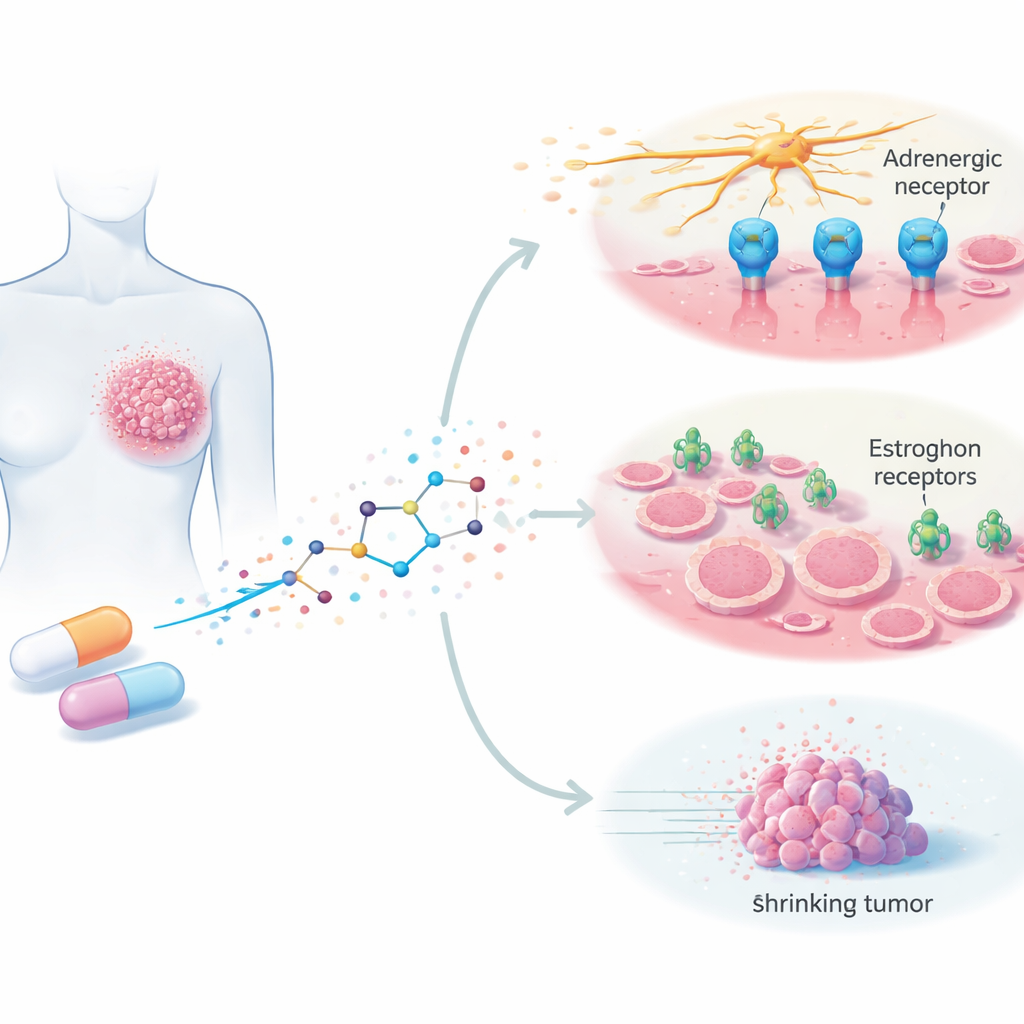
يظل سرطان الثدي واحداً من أكثر السرطانات انتشاراً وفتكاً لدى النساء، وينفد لدى كثير من المرضى الخيارات العلاجية الفعالة في نهاية المطاف. تستكشف هذه الدراسة ما إذا كان من الممكن إعادة توظيف سيلودوسين، وهو قرص يُستخدم بأمان حالياً لمشاكل المسالك البولية لدى الرجال، لمكافحة سرطان الثدي. وبما أنه دواء مُعتمد وميسور التكلفة وله سجل سلامة معروف، فإن إثبات أنه قادر على إبطاء أو قتل خلايا سرطان الثدي قد يسرّع الطريق إلى علاجات جديدة، خصوصاً للأشخاص الذين يعانون من أمراض عدوانية.
دواء مألوف بدور جديد
يُصرف سيلودوسين حالياً لتخفيف الأعراض البولية الناتجة عن تضخم البروستاتا من خلال حجب إشارات عصبية معينة تُعرف بالإشارات الأدرينالية. هذه الإشارات لا تقتصر مهمتها على التحكم في العضلات؛ فهناك أدلة متزايدة تشير إلى أنها قد تساعد أيضاً الأورام على النمو والانتشار وتكوين أوعية دموية جديدة. تساءل الباحثون عما إذا كان سيلودوسين يمكن أن يتداخل مع هذه الإشارات الضارة في خلايا سرطان الثدي كذلك. اختبروا الدواء على عدة سلالات بشرية من خلايا سرطان الثدي مزروعة في المختبر، تمثل الأورام الحساسة للهرمونات والأورام الصعبة العلاج ثلاثية السلبية، وقارنوا تأثيراته مع تأثيراته على خلايا الثدي السليمة.
إبطاء النمو وتحفيز موت الخلايا
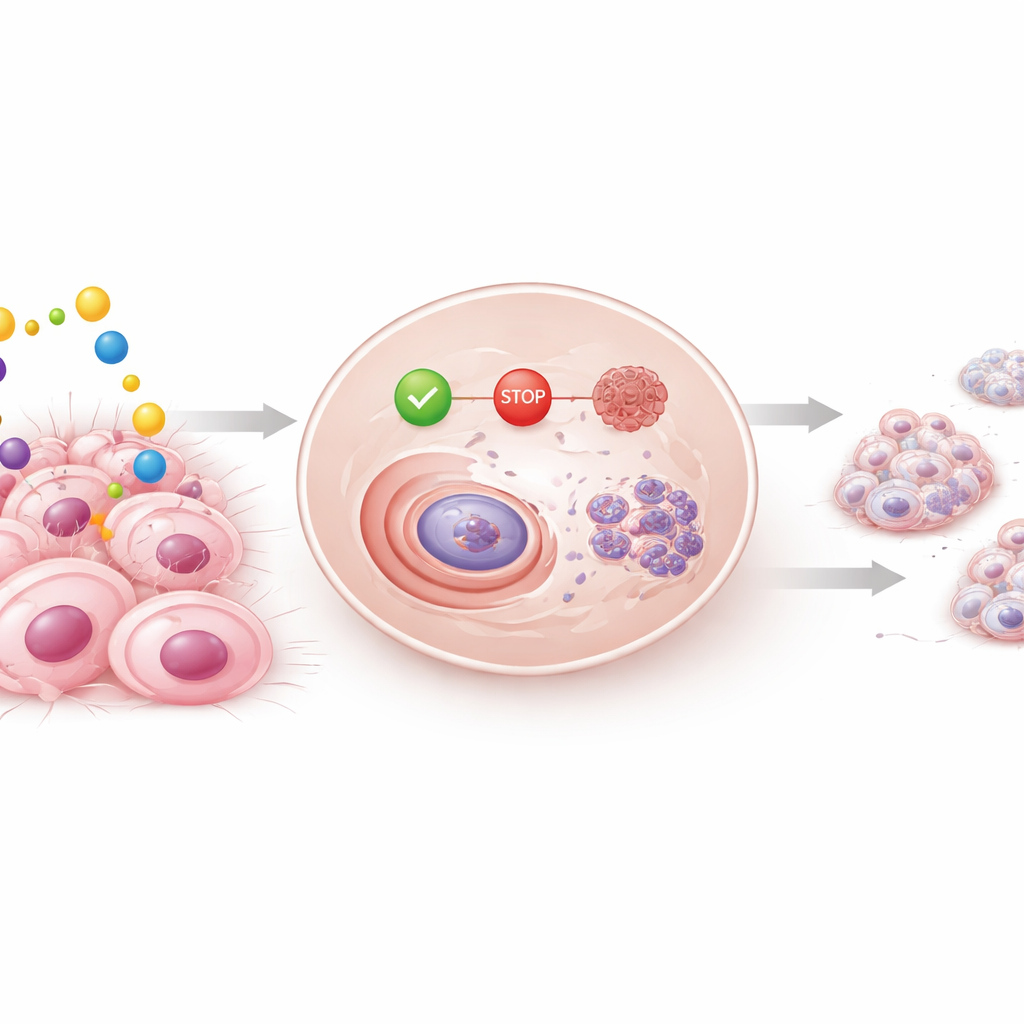
عند تعريض خلايا سرطان الثدي لسيلودوسين، تباطأ نموها بطريقة تعتمد على الزمن والجرعة. كانت الخلايا الحساسة للهرمونات متأثرة بشكل خاص، لكن حتى الخلايا العدوانية ثلاثية السلبية أظهرت قدرة متقاعدة على البقاء وتشكيل مستعمرات مع مرور الوقت، بينما تَجَنَّبت خلايا الثدي الطبيعية معظم هذه الآثار. كشفت تجارب إضافية ما يحدث داخل الخلايا: عرقل سيلودوسين تقدمها في طور مبكر من دورة الخلية، وهي سلسلة الخطوات التي يجب أن تكملها الخلية للانقسام. تراجعت مستويات بروتينات "التحفيز" التي تدفع الخلايا نحو الانقسام، في حين ارتفعت بروتينات "التوقف" والبروتين الحامي المعروف p53. كما دفع الدواء الخلايا السرطانية نحو الموت المبرمج، كما دلّت الزيادة المتدرجة في عدد الخلايا ذات الحمض النووي المجزأ.
حجب الحركة والنمو الشبيه بالأورام ثلاثية الأبعاد
يصبح السرطان مهدداً للحياة عندما تهاجر الخلايا وتؤسس أوراماً جديدة في أماكن أخرى. باستخدام خدش شبيه بالجرح على طبقة من الخلايا، وجد الباحثون أن سيلودوسين أبطأ السرعة التي يمكن بها كل من خلايا سرطان الثدي الحساسة للهرمونات وثلاثية السلبية أن تتحرك لسد الفجوة. لجأ الفريق أيضاً إلى الكُرات ثلاثية الأبعاد، وهي تجمعات خلوية كروية صغيرة تُحاكي الأورام الحقيقية أفضل من الطبقات الخلوية المسطحة. قلل سيلودوسين بشكل ملحوظ من تكوين وحجم هذه الكُرات. وفي الوقت نفسه، خفّض مستويات E-cadherin، الجزيء الذي يساعد الخلايا على الالتصاق ببعضها ويشارك أيضاً في إشارات النمو والبقاء، مما يوحي بأن تعطيل اتصالات الخلية بالخلية قد يكون إحدى الطرق التي يتداخل بها الدواء مع تنظيم الورم وانتشاره.
هدف ثانٍ مفاجئ داخل الخلايا السرطانية
صُمم سيلودوسين ليمنع مستقبلات أدرينالية، لكن البيانات لم تتوافق مع سردية بسيطة تقوم على "هدف واحد فقط". بعض خلايا سرطان الثدي التي استجابت بقوة للدواء كانت تحتوي على مستقبل أدرينالي من النوع الذي يُفترض أن يستهدفه سيلودوسين قليل أو غير قابل للكشف، والخلايا التي تحتوي على المزيد من هذا المستقبل لم تكن بالضرورة أكثر حساسية. للبحث عن أهداف أخرى، استخدم المؤلفون النمذجة الحاسوبية لرؤية ما إذا كان سيلودوسين قد يتناسب أيضاً مع مستقبلات الإستروجين، المفاتيح الجزيئية التي تحرك العديد من سرطانات الثدي وهي الأهداف الرئيسية لأدوية مثل تاموكسيفين. أظهرت محاكاةهم أن سيلودوسين يمكنه الارتباط بالنوعين الرئيسيين من مستقبل الإستروجين بقوة ذات مغزى، متفاعلاً مع نفس نقاط الاتصال الرئيسية التي يستهدفها التاموكسيفين. هذا يوحي بأن سيلودوسين قد يعمل كمعدّل لمستقبل الإستروجين بالإضافة إلى حجب الإشارات العصبية.
ماذا قد يعني هذا للمرضى
بشكل مجمل، تشير التجارب إلى أن سيلودوسين قد يكون مهاجماً متعدد الأوجه لخلايا سرطان الثدي: يبطئ نموها، ويدفعها نحو الانتحار الخلوي المنظم، ويعوق حركتها، ويمنعها من التنظيم إلى كُرات تشبه الأورام، بينما يبدو أنه يعمل على مسارات محركة بالأدرينالين والإستروجين على حد سواء. الجرعات الفعالة في أطباق الخلايا أعلى من المستويات التي تُبلَّغ لدى المرضى بالجرعات المعيارية في طب المسالك البولية، لذا ستكون هناك حاجة لمزيد من العمل في الحيوانات وتجارب تجمعات دوائية لتقدير الإمكانات في العالم الحقيقي. ومع ذلك، وبما أن سيلودوسين مُصدق عليه ومتحمَّل عموماً بشكل جيد، فإن هذه الدراسة تمهد الطريق لإعادة توظيفه كجزء من استراتيجيات علاجية جديدة، لا سيما للمرضى ذوي الخيارات المحدودة مثل المصابين بسرطان الثدي ثلاثي السلبية.
الاستشهاد: Pellegrino, M., Occhiuzzi, M.A., Marra, M. et al. Molecular insights into Silodosin’s anti-cancer effects: a promising repurposing strategy for breast cancer. Cell Death Discov. 12, 128 (2026). https://doi.org/10.1038/s41420-026-02973-8
الكلمات المفتاحية: سرطان الثدي, إعادة توظيف الأدوية, سيلودوسين, مستقبل الإستروجين, سرطان الثدي ثلاثي السلبية