Clear Sky Science · ar
الزيادة الواقية في ميتالوثيونين-2A في تخلخل الأقراص الفقرية تثبط فِرُوبتوسيس خلايا النواة اللبية عبر تنشيط مسار PI3K/AKT/mTOR
لماذا تهم هذه المشكلة في الظهر
يؤثر ألم أسفل الظهر على مئات الملايين من الناس حول العالم ويُعد سببًا رئيسيًا للعجز. أحد المسببات الرئيسية هو التدهور التدريجي للوسادات بين عظام العمود الفقري، والتي تُعرف بالأقراص الفقرية. يطرح هذا البحث سؤالًا واعدًا: هل يمكن لجزيئات الحماية الذاتية في الجسم أن تقي هذه الأقراص من التلف، وهل قد يشير تعزيزها إلى علاجات جديدة لألم الظهر المزمن؟ 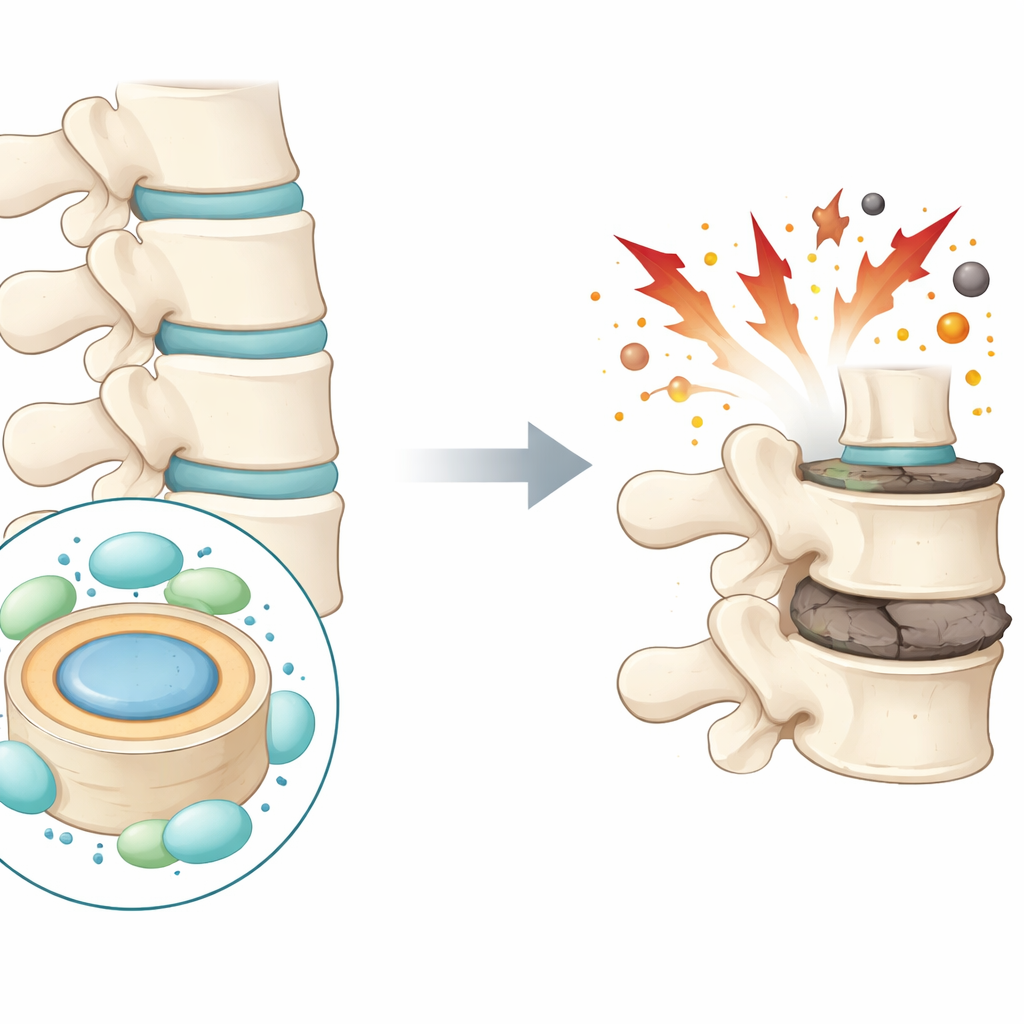
الوسادات داخل العمود الفقري
كل قرص فقري يحتوي على مركز ناعم شبيه بالهلام يُسمى النواة اللبية، يحيط به حلقة أكثر صلابة. تعمل هذه الهياكل كممتصات للصدمات للعمود الفقري. مع تدهور الأقراص، تموت الخلايا في المنطقة المركزية وتتآكل مصفوفة البروتينات والماء الداعمة. يتسطح القرص ويتشقّق، مما قد يؤدي إلى الألم وتقييد الحركة. يركز المؤلفون على نوع محدد من موت خلايا القرص الذي جذب الانتباه حديثًا في العديد من الأمراض: موت مدفوع بالحديد والاحتراق التأكسدي المعروف بالفِرُوبتوسيس. ويشتبهون أن هذه العملية تلعب دورًا رئيسيًا في انهيار القرص.
عندما ينهار توازن الحديد والأكسدة
يُثار الفِرُوبتوسيس عندما يتراكم الحديد الحر وجزيئات الأكسدة التفاعلية داخل الخلايا، مما يتلف الدهون في أغشية الخلايا وخاصة المتقدرات الصغيرة المسؤولة عن الطاقة. حلّل الفريق بيانات جينية خلوية مفردة من أنسجة الأقراص البشرية ووجد علامات واضحة على تغير جينات مرتبطة بالفِرُوبتوسيس في الأقراص المتدهورة. على وجه الخصوص، كانت مؤشرات الحماية التي تحمي الخلايا عادةً من هذا النوع من التلف، مثل الإنزيم GPX4، منخفضة في الأقراص المتآكلة لدى المرضى والجرذان على حد سواء. في الوقت نفسه، زادت مؤشرات تروّج للضرر والالتهاب، مرسمة صورة لخلايا تتعرض لهجوم تأكسدي مع تقدم تدهور الأقراص.
حامي داخلي يربط المعادن
من بين العديد من الجينات التي تغيرت في الأقراص المريضة، برز جين واحد: ميتالوثيونين‑2A (MT2A)، وهو بروتين صغير يربط معادن مثل الزنك ويمكنه امتصاص الجزيئات التفاعلية الضارة. كانت مستويات MT2A أعلى بشكل لافت في الأقراص البشرية الأكثر تدهورًا وفي نموذج جرذ لرضح القرص. للوهلة الأولى يبدو هذا متناقضًا—لماذا يرتفع جزيء واقٍ في نسيج تالف؟ افترض الباحثون أن الجسم يشن استجابة تعويضية، محاولًا مواجهة الارتفاع في الضغط الناتج عن الحديد. في الأطباق المختبرية، عندما تعرضت خلايا القرص لمادة تحاكي الإجهاد التأكسدي، ارتفعت مستويات MT2A مع تدهور صحة الخلايا، مما عزز الفكرة بأنه يُفَعّل كآلية دفاعية.
خفض الحماية وزيادتها
لاختبار ما إذا كان MT2A واقيًا بالفعل وليس ضارًا، ضبط الفريق مستوياته منخفضة أو مرتفعة بعناية في خلايا قرص بشرية. عندما أعاقوا إنتاج MT2A، تسبب الإجهاد التأكسدي بموت خلوي أكبر، وتراكمًا أكبر للحديد، وتلفًا شديدًا للدهون، وإصابة بالغة في المتقدرات. عندما عززوا MT2A بدلاً من ذلك، أو عالجوا الخلايا بعامل معروف يثبط الفِرُوبتوسيس، خفتت العديد من هذه المشكلات: انخفض الحديد والجزيئات التفاعلية، استعادت مضادات الأكسدة الواقية توازنها، وبدا أن المتقدرات أكثر صحة. تجلت هذه التغيرات أيضًا في حفاظ أفضل على بروتينات المصفوفة الداعمة للخلايا، وهي حاسمة للحفاظ على انتفاخ القرص ووظيفته. 
مسار إشاري رئيسي داخل الخلية
بتعمق أكثر، نظر العلماء في كيفية إرسال MT2A لإشارات حماية داخل الخلايا. أشارت تسلسلات الجينات وقياسات البروتين إلى مسار PI3K/AKT/mTOR، وهو نظام داخلي معروف يؤثر في النمو والتمثيل الغذائي والبقاء. خفض MT2A خفّض نشاط هذا المسار، بينما رفع MT2A فعّله. عندما استخدم الباحثون أدوية لحجب خطوات مختلفة في هذا المسار، اختفت فوائد زيادة التعبير عن MT2A: ارتفعت مؤشرات الفِرُوبتوسيس مجددًا، عاود التلف التأكسدي الظهور، وفقدت خلايا القرص المزيد من بروتيناتها الهيكلية. هذا يشير إلى أن MT2A يحمي خلايا القرص إلى حد كبير عن طريق تنشيط هذا المسار الإشاري المؤيد للبقاء، الذي بدوره يقيّد الفِرُوبتوسيس.
دليل مبدئي في الحيوانات
أخيرًا، سأل الفريق ما إذا كان تعزيز MT2A يمكن أن يبطئ فعليًا تَخَلُّخ القرص في كائن حي. في الجرذان، أحدثوا إصابة في القرص بواسطة وخز إبرة ثم أدخلوا فيروسًا مصممًا لزيادة MT2A مباشرة داخل القرص. بعد أسابيع، أظهرت التصوير والتحاليل النسيجية أن الأقراص التي تحتوي على MT2A الزائد حافظت على ارتفاعها أكثر، وكان لها بنية داخلية أوضح، وأظهرت فقدًا أقل لبروتينات المصفوفة الرئيسية مقارنة بالأقراص المصابة وغير المعالجة. كما انخفضت مؤشرات الفِرُوبتوسيس، مما يدعم الفكرة أن MT2A يساعد في حماية وسادة القرص من الانهيار تحت ضغط الأكسدة والحديد.
ما يعنيه هذا لرعاية ألم الظهر في المستقبل
مجتمعةً، توحي النتائج بأن MT2A ليس مجرد مرافقة بل عامل أمان مدمج يرتفع عندما تبدأ الأقراص في الفشل، محاولًا حماية الخلايا من الأكسدة الضارة المدفوعة بالحديد. عبر تنشيط مسار داخلي للبقاء، يحد MT2A من شكل محدد من موت الخلايا، ويحافظ على بنية القرص، ويُبطئ التدهور—على الأقل في النماذج الحيوانية وزُرع الخلايا. للمرضى، يشير ذلك إلى أن MT2A وشركاء إشاراته يمكن أن يكونوا أهدافًا واعدة لأدوية أو علاجات جينية تهدف إلى حماية أو تجديد الأقراص الفقرية، مما قد يقدم أكثر من مجرد تخفيف للألم أو جراحة على المدى البعيد.
الاستشهاد: Cai, H., Zheng, Hl., Chen, Qz. et al. The protective up-regulation of metallothionein-2A in intervertebral disc degeneration inhibits nucleus pulposus cell ferroptosis through activation of the PI3K/AKT/mTOR pathway. Cell Death Discov. 12, 111 (2026). https://doi.org/10.1038/s41420-026-02972-9
الكلمات المفتاحية: ألم أسفل الظهر, تَخَلُّخ الأقراص الفقرية, الفِرُوبتوسيس, ميتالوثيونين-2A, مسار PI3K AKT mTOR