Clear Sky Science · ar
التحليل متعدد الأوميكس يكشف التغايرية والفئات الوظيفية لخلايا السلف النخاعية الدبقية المستحثة من الخلايا الجذعية العصبية البشرية
لماذا حماية عزل الدماغ مهمة
تعتمد الأسلاك العصبية في دماغنا على طبقة دهنية تسمى الميالين، تلتف حول الألياف العصبية مثل عزل الكابلات الكهربائية. عندما يتضرر الميالين، كما يحدث في التصلب المتعدد واضطرابات أخرى، تتباطأ الإشارات أو تفشل، مما يسبب مشاكل في الحركة والرؤية والتفكير. تستكشف هذه الدراسة مجموعة خاصة من الخلايا البشرية القادرة على إعادة بناء الميالين وتطرح سؤالاً عملياً: أي الخلايا هي الأفضل للاستخدام في علاجات خلوية مستقبلية لإصلاح هذا العزل الحاسم؟
من خلايا بداية الدماغ إلى صانعي الميالين
بدأ الباحثون بالخلايا الجذعية العصبية البشرية—خلايا بداية متعددة القدرات مأخوذة من نسيج دماغي جنيني ومهيأة لأن تتحول إلى خلايا الجهاز العصبي. حفّزوا هذه الخلايا في المختبر لتتحول إلى خلايا سلف نخاعية دبلجية، أو hOPCs، وهي السلف المباشرة للخلايا التي تُكوّن الميالين. تحت المجهر تغيرت أشكال الخلايا من دوائر بسيطة إلى أشكال أكثر تعقيداً ذات تفرعات متعددة، وشغّلت بروتينات مميزة تشير إلى خطوات على طول الطريق نحو خلايا ناضجة منتجة للميالين. قدم هذا مصدرًا موثوقًا ونَسبيًا آمناً لسلف بشري لبناء الميالين لإجراء تحليلات مفصلة.
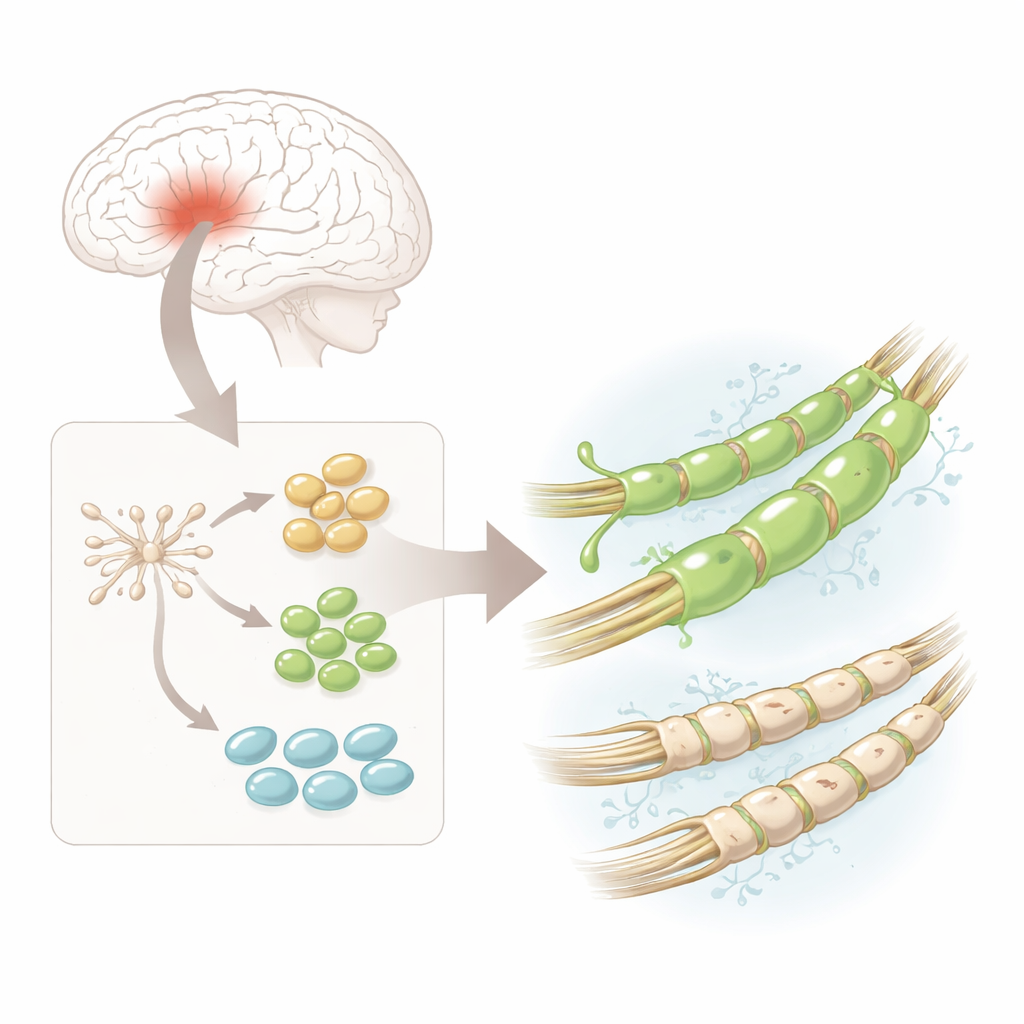
نوع واحد من الخلايا، عدة أصناف مخفية
باستخدام تسلسل RNA أحادي الخلية—أسلوب يقرأ أي الجينات نشطة في آلاف الخلايا الفردية—اكتشف الفريق أن خلايا hOPCs لم تكن متشابهة جميعها. بل تفرعت إلى ثلاث مراحل رئيسية: «ما قبل السلف» المبكرة، والسلف الأكثر التزامًا، وخلايا تقترب من هوية الضامة النخاعية الكاملة. عبر كل هذه المراحل، برز جين واحد: PDGFRA، الذي يشفر مستقبلًا سطحيًا. أكدت طريقة تصوير حساسة للغاية تسمى RNA-Scope أن رسالة PDGFRA وبروتينه كانت أكثر وفرة من علامات أساسية أخرى في كل مرحلة، ما يوحي أن هذا المستقبل قد يميز خلايا ذات قدرة خاصة على بناء الميالين.
فرز أقوى خلايا الإصلاح
لاختبار هذه الفكرة، فصل العلماء خلايا hOPCs إلى مجموعتين اعتمادًا على وجود مستقبل PDGFR-α على سطحها. ثم قارنوا الخلايا الموجبة لـPDGFR-α، والخلايا السالبة، والخلايا غير المفروزة في سلسلة من الاختبارات الوظيفية. عند زرعها في فئران «شيفرر»—التي لا تستطيع تكوين ميالين طبيعي—نتجت خلايا PDGFR-α الإيجابية ميالينًا أكثر كثافة وتماسكًا حول الألياف العصبية من المجموعات الأخرى. كما هاجرت هذه الخلايا لمسافات أبعد وتكاثرت بسرعة أكبر في اختبارات المختبر. بمعنى آخر، كانت مجموعة PDGFR-α الإيجابية الأكثر نشاطًا في الانتقال إلى المواقع المطلوبة، والازدياد في العدد، وإعادة بناء العزل.
الإشارات الداخلية التي تقود النمو والإصلاح
بتعمق أكثر، قارن الفريق نشاط الجينات بين الخلايا الموجبة والسالبة لـPDGFR-α. وجدوا أن الخلايا الموجبة شغّلت شبكات جينية متورطة في نمو الخلايا الدبقية وتكوين الميالين، بالإضافة إلى عدة مسارات إشارات داخل الخلية. برز مساران بشكل خاص: PI3K–AKT–mTOR، المرتبط منذ زمن بنمو الخلايا وإنتاج الميالين، وإشارة TGF-β، التي تؤثر في كيفية اختيار الخلايا الدماغية الشابة لمصائرها. اقترحت البيانات أن تفعيل PDGFR-α يتغذى إلى PI3K–AKT–mTOR، الذي بدوره يعزز الإشارات المتعلقة بـTGF-β، مجتمعةً دافعةً الخلايا نحو أن تصبح صانعي ميالين فعّالين.
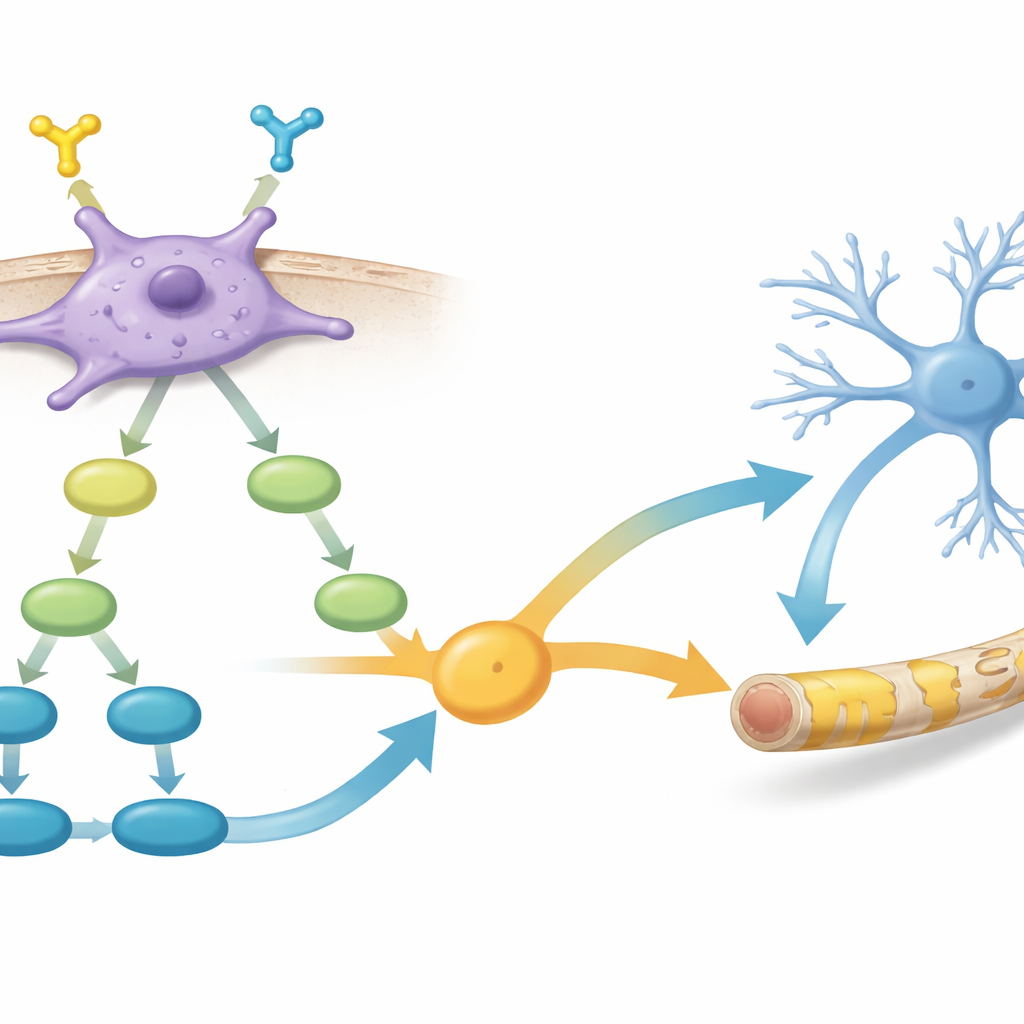
تعزيز إصلاح الميالين بمساعد كيميائي
سأل الباحثون بعد ذلك ما إذا كان بإمكانهم تعزيز هذه الخلايا الواعدة أكثر. عالجوا خلايا hOPCs الإيجابية لـPDGFR-α بجزيء صغير ينشط مسار TGF-β وفحصوا كل من نشاط الجينات والسلوك. بعد المعالجة، أظهرت هذه الخلايا مستويات أعلى من عدة جينات مرتبطة بالميالين وأنتجت أغلفة ميالين أكثر سمكًا واكتمالًا عند زرعها في فئران شيفرر، مقارنة بالخلايا الإيجابية لـPDGFR-α غير المعالجة. يدعم ذلك فكرة أن ضبط الإشارات الداخلية بعناية في خلايا السلف المختارة جيدًا يمكن أن يحسن أدائها كأدوات حية لإصلاح الميالين.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن ليست كل خلايا سلف بناء الميالين متساوية. من خلال الجمع بين أدوات قراءة الجينات والتصوير القوية، تحدد هذه الدراسة مجموعة مميزة—خلايا hOPCs الموجبة لـPDGFR-α—التي تهاجر أفضل، وتنقسم أكثر، وتعيد بناء الميالين بشكل أكثر فعالية من نظرائها. كما تسلط الضوء على مسارات إشارات داخلية يمكن دفعها كيميائيًا لجعل هذه الخلايا أكثر قوة. معا، ترسم هذه الرؤى خارطة طريق لتصميم علاجات خلوية أكثر أمانًا وكفاءة لاستعادة عزل الدماغ في الأمراض التي يفقد فيها الميالين.
الاستشهاد: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
الكلمات المفتاحية: إصلاح الميالين, خلايا السلف النخاعية الدبقية, الخلايا الجذعية العصبية, علاج خلوي, تسلسل RNA أحادي الخلية