Clear Sky Science · ar
التواصل بين الطاقة الميتوكوندرية وSASP يحدد فعالية السنوليتكس في الشيخوخة الناجمة عن العلاج
لماذا يصعب القضاء على خلايا السرطان «الزومبي»
الكثير من أدوية السرطان الحديثة لا تقتل كل خلية ورمية مباشرة. بدلاً من ذلك، تدخل بعض الخلايا حالة شبيهة بالفراغ تُسمى الشيخوخة الخلوية: تتوقف عن الانقسام لكن تظل حية، أشبه بخلايا «زومبي». قد تكون هذه الخلايا المتسببة في الشيخوخة الناجمة عن العلاج مفيدة مبدئياً، لكن إذا استمرت فقد تغذي الانتكاس والمقاومة والآثار الجانبية. لذلك يختبر العلماء أدوية سنوليتكس المصممة لقتل الخلايا المسنة بشكل انتقائي. تسأل هذه الورقة سؤالاً بسيطاً بظاهر الأمر: لماذا تموت بعض خلايا السرطان المسنة عند تعرضها للسنوليتكس بينما تصمد أخريات بعناد؟
محطات طاقة تتذكر ماضيها
تبني الدراسة على الميتوكوندريا، محطات الطاقة الصغيرة داخل الخلايا. فحص الباحثون ما إذا كانت طريقة حرق الميتوكوندريا لوقودات مختلفة — مثل السكريات والدهون والأحماض الأمينية — تؤثر في حساسية خلايا السرطان المسنة لأدوية سنوليتك التي تستهدف بروتين البقاء BCL‑xL. باستخدام اختبار عالي الإنتاجية (MitoPlate S‑1)، شكّلوا «بصمة وظيفية» لنشاط الميتوكوندريا في عدة خطوط خلوية سرطانية قبل وبعد تحفيز الشيخوخة بعلاجات مختلفة (أدوية مُتلفة للحمض النووي، مثبطات الانقسام الخلوي، إجهاد تأكسدي، أو مثبطات دورة الخلية). وجدوا أن الشيخوخة الناتجة عن العلاج لا تَنتج حالة ميتوكوندرية موحدة واحدة. بل ترك كل دواء «بصمة طاقة» مميزة، تغيّر مدى وشدة قدرة الميتوكوندريا على استخدام مصادر طاقة متنوعة. والأهم أن هذه المرونة تُضاف إلى أساس موجود سلفاً: التكوين الميتوكوندري الأصلي للخلايا السرطانية الأب وضع حدّاً أعلى — «السقف» — لمدى استجابة السنوليتكس اللاحقة.
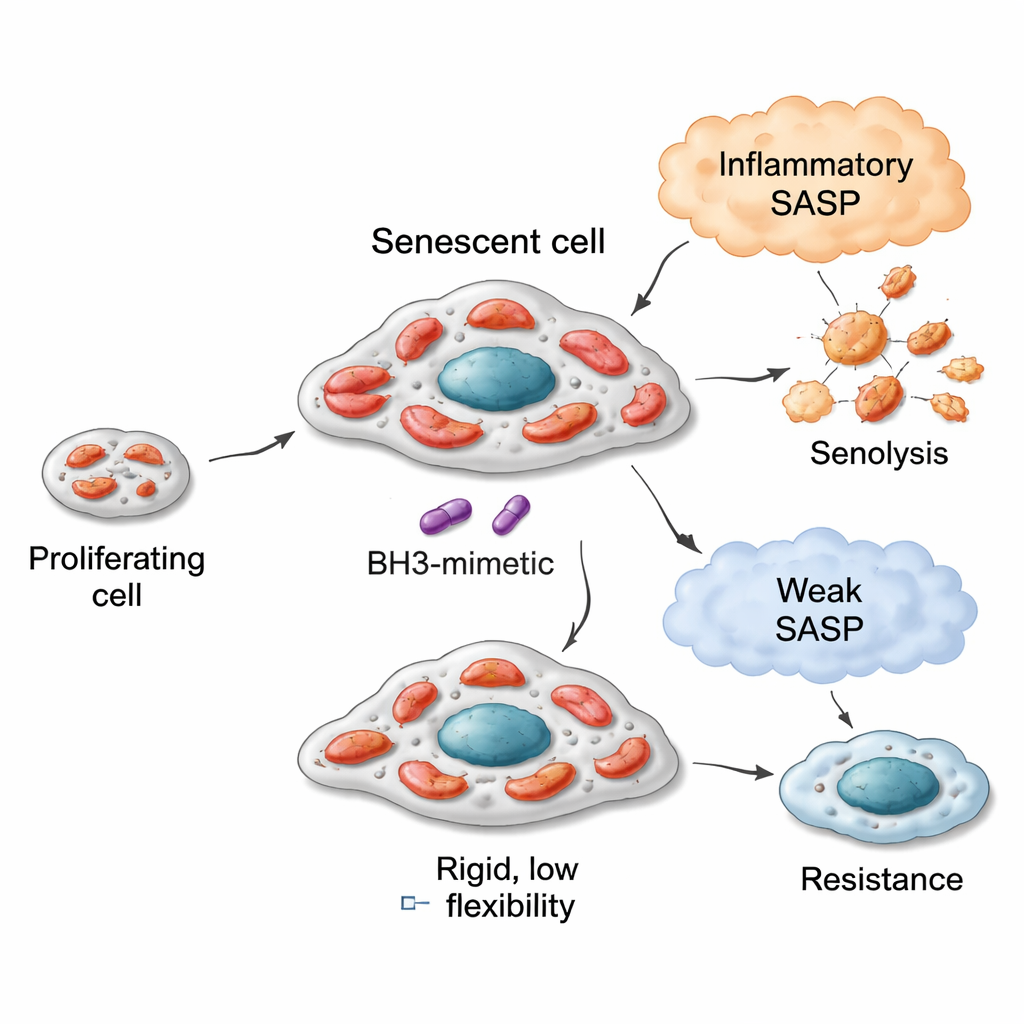
محركات مرنة، وقود مختلف، وحساسية للسنوليتكس
في نماذج سرطان الرئة والثدي والقولون، كانت الخلايا المسنة ذات ميكروفيديوكوندريات أكثر مرونة — قادرة على أكسدة مجموعة أوسع من الوقود — تميل لأن تكون أكثر عرضة للسنوليتكس المستهدفة لـ BCL‑xL مثل نافيتوكلكس (ABT‑263) وA1331852. على سبيل المثال، طوّرت خلايا سرطان الرئة التي تم دفعها إلى الشيخوخة بواسطة الدواء بليومايسين ميتوكوندريا تستخدم بقوة العديد من الركائز، خصوصاً تلك المرتبطة بتفكك الأحماض الدهنية ومسارات حمض أميني معينة. كانت هذه الخلايا شديدة الحساسية للسنوليتكس. بالمقابل، أظهرت الخلايا التي أدخلت في الشيخوخة بواسطة مثبط CDK4/6 (بالبوسيكليب) مجموعة أيضية أضيق واستجابت بشكل ضعيف لنفس عوامل السنوليتكس. ومع ذلك، كان لهذه العلاقة حدود: فقد أصبحت خلايا سرطان الثدي أيضاً مرنة أيضياً بعد الشيخوخة، لكن لأن ميتوكوندرياتها الابتدائية كانت أقل استعداداً للموت المبرمج، كان أقصى استجابة سنوليتك لديها متواضعاً. ظلت خلايا سرطان القولون ذات الآلية المبرمجة للموت المعطلة مقاومة بغض النظر عن كيفية تحول الأيض. مقياس واحد—مدى قدرة الخلايا على أكسدة الوقود السكسينات في الحالة القاعدية—خدم كمؤشر بسيط على هذه السعة الميتوكوندرية الموروثة.
عندما يتحدث الأيض إلى الالتهاب
الخلايا المسنة سيئة السمعة بوجود SASP، وهو كوكتيل من العوامل الالتهابية ونموّية المفرزة التي يمكن أن تؤثر على الأنسجة المحيطة. استكشفت الفريق كيف يرتبط الاستقلاب الميتوكوندرى بهذا السلوك الإفرازي باستخدام خلايا مهندَسة بمؤشر لـ miR‑146a، وهو ميكروRNA يتم تشغيله بواسطة المنظم الالتهابي الرئيسي NF‑κB. وجدوا أنه بينما تُحدَّد ملفات SASP العامة إلى حد كبير بنوع الخلية، فإن حالات مسنة معينة فقط هي التي فعّلت محور NF‑κB/miR‑146a. وكانت تلك نفسها الحالات التي استجابت جيداً لسنوليتكس المستهدفة لـ BCL‑xL. والأهم أن هذه الخلايا المسنة الموجبة لـ «SASP الالتهابية» أظهرت أيضاً استخداماً معززاً لأكسدة الأحماض الدهنية وارتفاعاً في التعبير الجيني لجينات تنقل الدهون طويلة السلسلة إلى الميتوكوندريا. قمع دخول الأحماض الدهنية باستخدام الدواء إيتو موكسير قلّل تنشيط miR‑146a دون عكس الشيخوخة بشكل كامل، مما يوحي بأن اختيار وقود الميتوكوندريا يساعد في إضفاء صفة التهابية تسمح بالاستجابة للسنوليتكس.
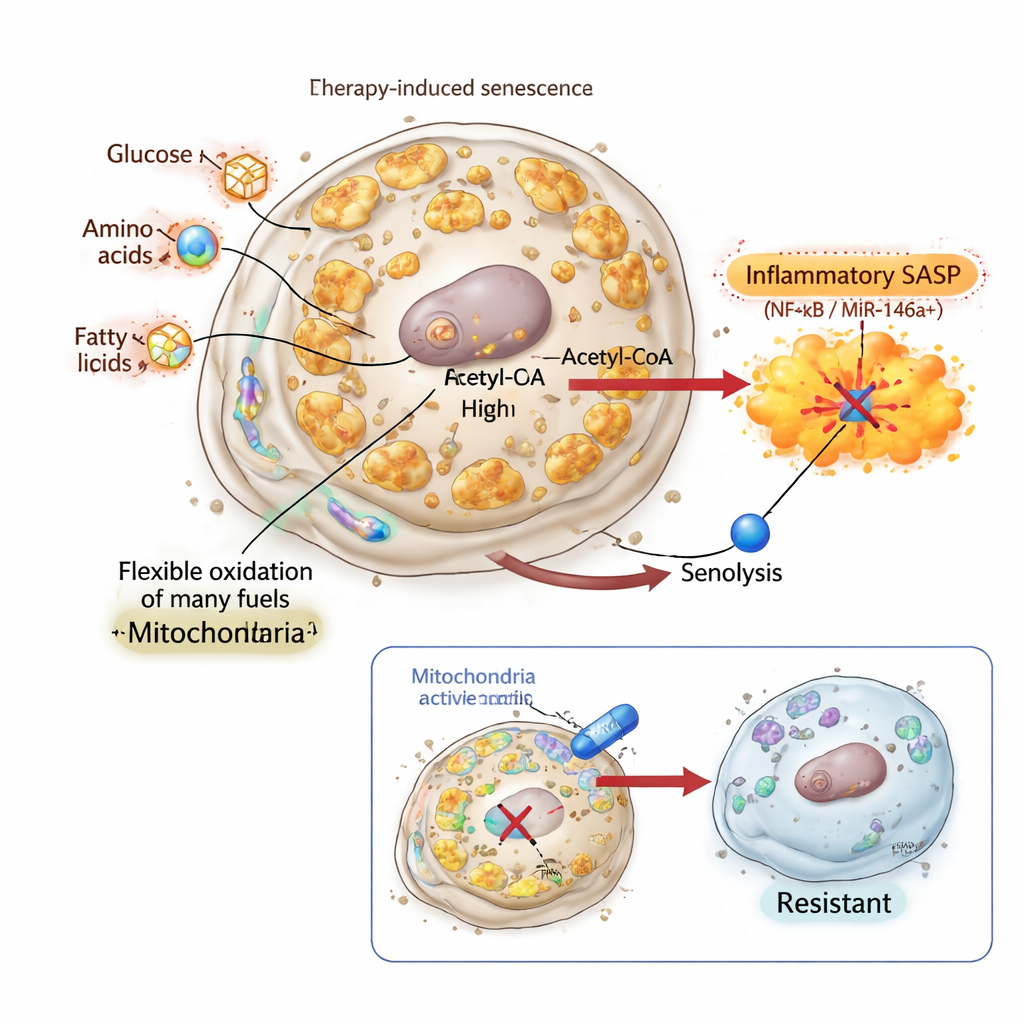
إسكات الإشارة وابتكار خلايا مسنة لا تُقهر
لاختبار ما إذا كان SASP الالتهابي مطلوباً فعلاً لقتل السنوليتكس، لجأ الباحثون إلى إنفلاكرومين، مركب يربط بروتينات الكروماتين HMGB1 وHMGB2 ويمنع دورها في تنشيط جينات SASP. في خلايا سرطان الرئة والثدي، أحدث إنفلاكرومين نمط شيخوخة كلاسيكي: أصبحت الخلايا كبيرة، توقفت عن الانقسام، وتراكمت عليها علامات الشيخوخة. ارتفع كتلة الميتوكوندريا ونشاطها البايوإينرجيتيكي بشكل ملحوظ، وأُعيد تشكيل استخدام الوقود بوضوح. ومع ذلك، تراجع SASP وبقي مؤشر miR‑146a صامتاً إلى حد كبير. وبشكل لافت، كانت هذه الخلايا المسنة الخالية من SASP مقاومة تماماً لسنوليتكس المستهدفة لـ BCL‑xL، رغم امتلاكها ميتوكوندريات نشطة وُعيد برمجتها وانخفاض التعبير عن جين البقاء الكلاسيكي BCL2. أظهر ذلك أن التغيرات الميتوكوندرية وحدها غير كافية؛ فبدون مخرج التهابي مدفوع بالميتوكوندريا، تفشل «اللكمة الثانية» للسنوليتكس.
ما يعنيه هذا لعلاجات السرطان المستقبلية
للقارئ غير المتخصص، خلاصة الدراسة أن قتل خلايا السرطان «الزومبي» الناجمة عن العلاج محكوم بدائرة متعددة الطبقات. أولاً، صحة وتوصيل الميتوكوندريا الأصليان في خلية الورم يحدّان مدى ما يمكن أن تحققه أدوية السنوليتكس. ثانياً، العلاج المحدد الذي يسبب الشيخوخة يمكن أن يدفع الأيض الميتوكوندري نحو مرونة أكبر أو أقل، مُقرباً الخلايا أو بعيداً عن حافة الموت المبرمج. ثالثاً — والأهم — تعمل أدوية السنوليتكس جيداً فقط إذا نجح إعادة برمجة الأيض في تحفيز برنامج SASP التهابي يُجَاوِب النواة. بدون ذلك الحوار الالتهابي، يمكن أن تصبح الخلايا المسنة حالة مسدودة ومقاومة للأدوية. عملياً، يقترح هذا أن العلاجات المستقبلية قد تُحسَّن عن طريق اختبار مرونة الميتوكوندريا والتهاب SASP في الأورام، ثم اختيار أزواج من أدوية تحفيز الشيخوخة والسنوليتكس التي تضمن أن خلايا «الزومبي» ليست مجمّدة فحسب، بل متهيئة للإزالة.
الاستشهاد: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
الكلمات المفتاحية: الشيخوخة الخلوية, الميتوكوندريا, السنوليتكس, تمثيل الطاقة في السرطان, SASP الالتهابي