Clear Sky Science · ar
خفض SREBP1 يحفّز الفيروبتوسيس عبر قمع محور Nrf2-XCT/GPX4 في سرطان المبيض
تحويل مصنع الدهون لدى السرطان ليضربه من الداخل
غالبًا ما يُكتشف سرطان المبيض في مراحل متأخرة ويكون صعب العلاج. تستكشف هذه الدراسة نقطة ضعف مفاجئة في هذه الأورام: اعتمادها الشديد على صنع الدهون والزيوت. تُظهر الدراسة أن تعطيل مفتاحٍ رئيسيٍّ لهذا "المصنع الدهني" في خلايا السرطان يمكن أن يبطئ نموها ويشغّل نوعًا خاصًا من موت الخلايا، وفي الوقت نفسه يسهل على الجهاز المناعي مهاجمة الورم.
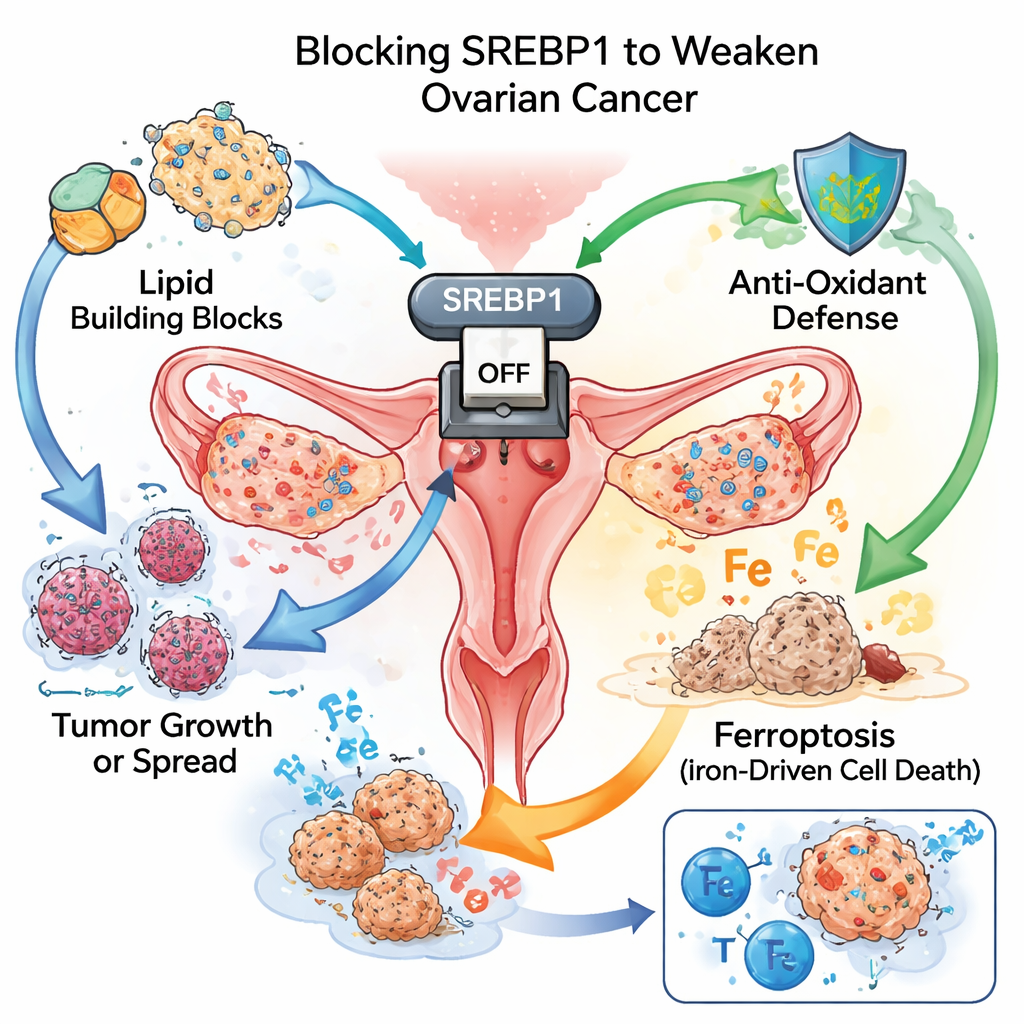
مفتاح رئيسي لوقود الورم
مثل الأعشاب الضارة سريعة النمو، تحتاج خلايا السرطان كميات هائلة من اللبنات والطاقة. وإحدى طرق تلبية هذا الطلب هي إعادة توصيل آليات صنع واستخدام الدهون. ركز الفريق على SREBP1، بروتين يعمل كمفتاح رئيسي لإنتاج الدهون. في عينات نسيجية من أكثر من مئة مريضة، كانت مستويات SREBP1 في الأورام المبيضية أعلى بكثير من الأنسجة الطبيعية المجاورة. النساء اللائي أظهرت أورامهن تلونًا أقوى لـ SREBP1 كنَّ مرتبطات بمرض أكثر عدوانية وببقاء أقصر، مما يجعل هذا البروتين محركًا للتقدّم وعلامة تحذير لتوقعات سيئة.
إبطاء النمو والانتشار بقطع إمداد الدهون
في خطوط خلايا سرطان المبيض المزروعة مخبريًا، أدى خفض SREBP1 إلى تراجع حاد في قدرة الخلايا على التكاثر وتشكيل المستعمرات. علِقت الخلايا في مراحل محددة من دورة الخلية، ما منعها من الانقسام بكفاءة. كما لوحظت علامات أقل للحركة والغزو: اختبارات الخدش وTranswell أظهرت أن الخلايا ذات SREBP1 المنخفض كانت أقل قدرة على الهجرة، وتحولت مؤشرات عملية التحول الشكلي المعروفة بـ EMT نحو حالة أكثر "طبيعية". في الوقت نفسه، انخفضت مقاييس الدهون الثلاثية والكوليسترول، وأظهرت الصبغات قطرات دهنية أقل داخل الخلايا، مؤكدة أن آلية صنع الدهون الداخلية لديها قد تراجعت.
إحداث موت خلوي مدفوعًا بالحديد
أبرز أثر لحجب SREBP1 كان تنشيط الفيروبتوسيس، شكل موت خلوي تم التعرف عليه مؤخرًا يقوده الحديد وتأكسد أغشية الخلايا. لم تتمكن إلا مادة مانعة للفيروبتوسيس، وليس مثبطات مسارات موت أخرى، من إنقاذ الخلايا التي أُخمد فيها SREBP1، ما يشير إلى أن الفيروبتوسيس هو السبب الرئيسي لموتها. أظهرت الاختبارات الكيميائية مزيدًا من نواتج التلف نتيجة دهون مؤكسدة، وانخفاضًا في مضاد التأكسد غلوتاثيون، وارتفاعًا في جزيئات دهنية تفاعلية. اثنان من البروتينات التي تحمي الخلايا عادة من الفيروبتوسيس، المسماة xCT وGPX4، انخفضت بشدة عندما نُقص SREBP1، مما أزال حاجزًا وقائيًا حاسمًا ضد هذه العملية المدمرة.
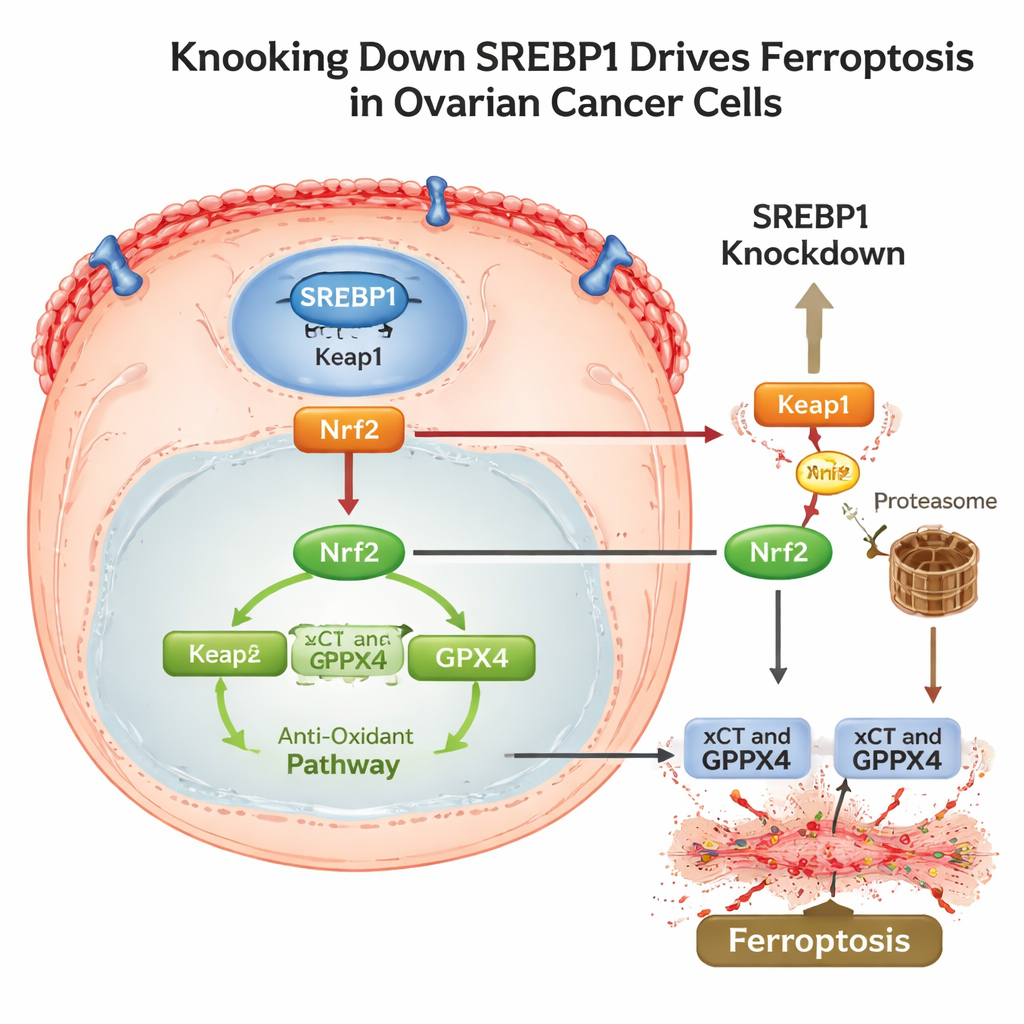
تعطيل درع الخلايا المضاد للأكسدة وحيل الهروب المناعي
لفهم كيف يربط SREBP1 بهذا البرنامج المموّت، تتبّع العلماء مسارًا عبر بروتين استجابة للضغط آخر مهم، Nrf2. في الظروف الطبيعية، يساعد Nrf2 الخلايا على البقاء عبر تشغيل جينات مضادة للأكسدة، بما في ذلك xCT وGPX4. وجدت الدراسة أن خفض SREBP1 زاد مستويات Keap1، وهو بروتين يعلّم على Nrf2 للتخلص منه، مما أدى إلى مزيد من تكسّر Nrf2 وقلة وصوله إلى النواة. مع تراجع Nrf2 ضعفت دفاعاته التالية واندلع الفيروبتوسيس. والأهم من ذلك، أظهرت الأورام الغنية بـ SREBP1 أيضًا مستويات أعلى من PD-L1، وهو بروتين سطحي يساعد خلايا السرطان على الاختفاء من خلايا تي المهاجمة. عندما أُخمد SREBP1 في أورام فئران، نمت السرطانات أبطأ، وأظهرت مزيدًا من علامات تلف الدهون، وقلَّ Nrf2 وGPX4 وPD-L1، إلى جانب نشاط مناعي متزايد.
لماذا هذا مهم للعلاجات المستقبلية
بعبارات بسيطة، يبدو أن أورام المبيض تستخدم SREBP1 كأداة بحدين للبقاء: تغذي نموها عبر تعزيز إنتاج الدهون وفي الوقت نفسه تزوّدها بدرع مضاد للأكسدة وغلاف منيع ضد المناعة. تُظهر هذه الدراسة أن إيقاف SREBP1 يمكن أن يجوع الورم من الدهون، ويزيل حمايته ضد تلف الحديد، ويقلل قدرته على التملّص من الهجوم المناعي. هذا يجعل من SREBP1 هدفًا جذابًا للأدوية الجديدة ويدعو إلى إمكانية الجمع بين مثبطات SREBP1 وعلاجات تُحفّز الفيروبتوسيس أو تطلق الجهاز المناعي للحصول على تحكّم أكثر فعالية وطويل الأمد في المرض.
الاستشهاد: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
الكلمات المفتاحية: سرطان المبيض, استقلاب الدهون, الفيروبتوسيس, SREBP1, مناعة الورم