Clear Sky Science · ar
آلية جديدة لاستجابة الخلايا العصبية لنقص الأكسجين: تنشيط الميتوفاجي المعتمد على PINK1 بوساطة HIF-1α/STOML2 ضد إصابة الخلايا العصبية
لماذا تهم استجابة الدماغ لانخفاض الأكسجين
العديد من الحالات الشائعة — بما في ذلك السكتة الدماغية، توقف التنفّس أثناء النوم، فشل القلب، وحتى التعرض لمرتفعات شاهقة — تحرم الدماغ من الأكسجين. عندما ينخفض الأكسجين، تواجه الخلايا الدماغية خطر التلف الدائم، مما يؤدي إلى مشاكل في الذاكرة ومشكلات عصبية أخرى. تكشف هذه الدراسة عن نظام “حماية ذاتي” مدمج تستخدمه الخلايا العصبية في المراحل المبكرة من نقص الأكسجين للحفاظ على بقائها وعملها. قد يفتح فهم هذا النظام الباب أمام علاجات جديدة تحمي الدماغ قبل حدوث إصابة خطيرة.
مشكلة مبكرة، لكن ليست كارثة بعد
لاستكشاف كيفية استجابة الدماغ لنقص الأكسجين، عرّض الباحثون الفئران لهواء يحتوي على نحو 13% أكسجين — مشابه للعيش على هضبة مرتفعة — لفترات زمنية مختلفة. خلال الأيام القليلة الأولى، بدت الحيوانات طبيعية في اختبارات الذاكرة والمتاهة، وكانت خلايا دماغها سليمة تحت المجهر. لم تظهر علامات فقدان الذاكرة أو تفتت بنية الخلايا الدماغية بوضوح إلا بعد أسبوع كامل من انخفاض الأكسجين. يشير هذا النمط إلى أنه، على الأقل في المراحل الأولى، لا تكون الخلايا العصبية ضحايا سلبيين لفقدان الأكسجين؛ بل يبدو أنها تشغّل استجابات وقائية تؤخر أو تمنع التلف.
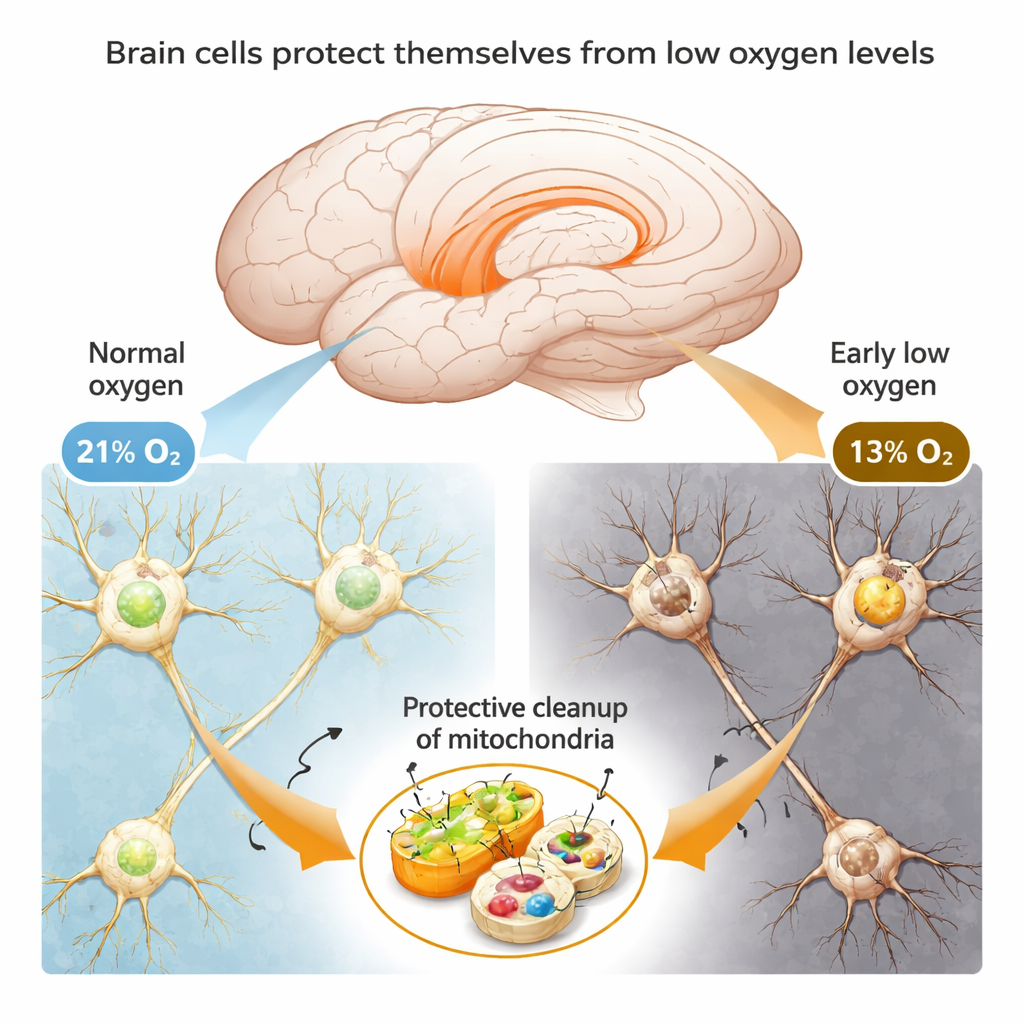
تنظيف خلوي: التخلص من محطات الطاقة التالفة
تركز الدراسة بشكل كبير على محطات طاقة الخلية — الميتوكوندريا — التي تكتسب أهمية خاصة في الخلايا العصبية لأن التفكير والذاكرة يتطلبان كميات كبيرة من الطاقة. في ظل انخفاض الأكسجين، قد تتعطل الميتوكوندريا وتُسرّب نواتج ضارة تضر الخلايا. وجد الفريق أنه في المرحلة المبكرة من نقص الأكسجين، تزيد الخلايا العصبية مؤقتًا من عملية تنظيف متخصصة تسمى الميتوفاجي، التي تزيل بشكل انتقائي الميتوكوندريا المتضررة مع الحفاظ على السليمة منها. في أدمغة الفئران وفي خلايا عصبية بشرية مشتقة مزروعة في أطباق، ارتفعت مؤشرات هذه العملية التنظيمية بعد وقت قصير من انخفاض الأكسجين، تمامًا عندما كانت الخلايا لا تزال تعمل جيدًا. عند حظر الميتوفاجي كيميائيًا، انخفضت بقاء الخلايا وازداد ظهور علامات الإصابة، مما يبين أن هذه خطوة التنظيف الحيوية ضرورية للحماية.
تتابع وقائي داخل الخلايا العصبية
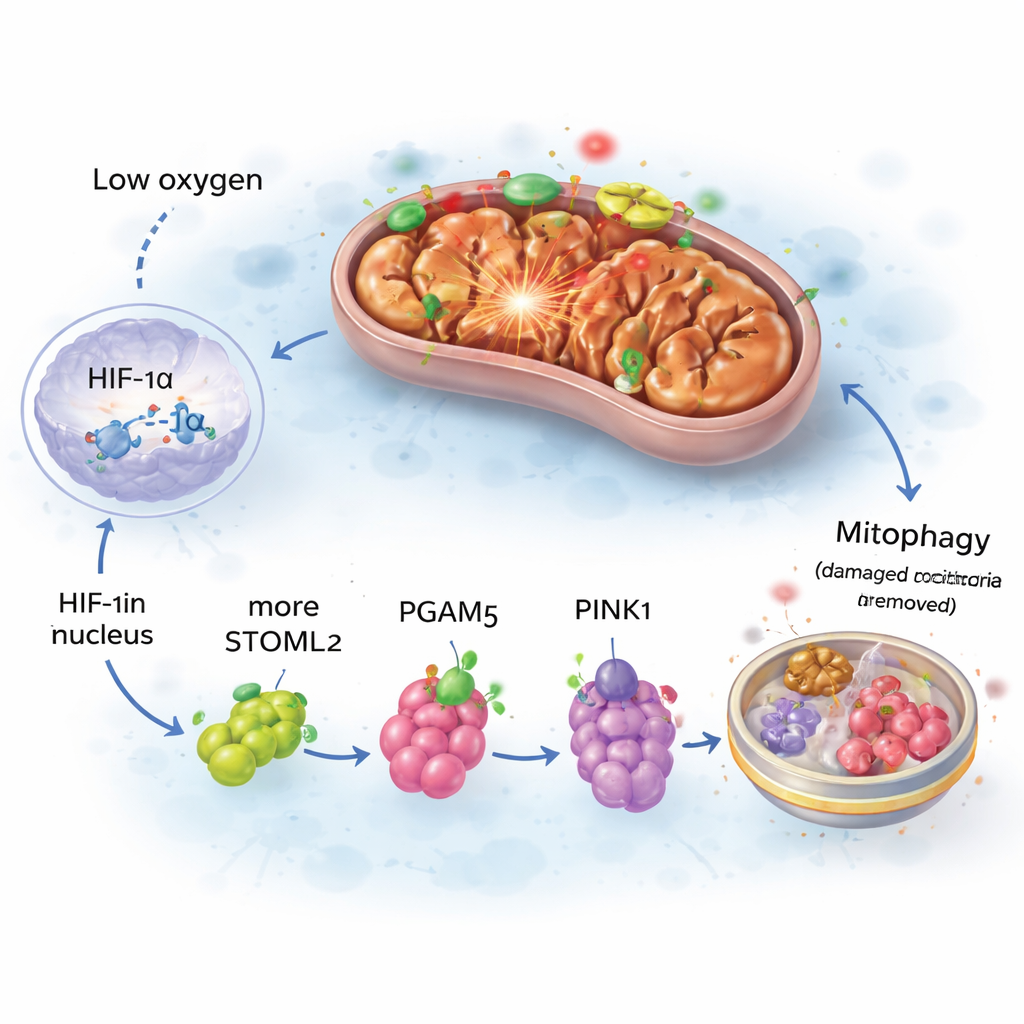
بتعمق أكثر، تتبّع الباحثون كيفية تشغيل هذا التنظيف الميتوكوندري. يؤدي انخفاض الأكسجين إلى تثبيت بروتين حساس يسمى HIF‑1α، الذي ينتقل إلى نواة الخلية ويغير نشاط الجينات. أحد أهدافه هو STOML2، بروتين ينتقل إلى سطح الميتوكوندريا. هناك، يساعد STOML2 في الحفاظ على بروتين آخر، PGAM5، في شكله الكامل. بدوره يسمح PGAM5 لجزيء آخر، PINK1، بالتراكم على السطح الخارجي للميتوكوندريا المتضررة. ثم يقوم PINK1 بوضع علامة على هذه المحطات الطاقوية المعطلة لإزالتها عبر آلية إعادة التدوير الخلوية. عندما خفض الفريق تحديدًا مستويات HIF‑1α أو STOML2 أو PGAM5 أو PINK1 في أدمغة الفئران، اختفت موجة الميتوفاجي المبكرة وازدادت إصابة الخلايا أثناء التعرض لنقص الأكسجين. برز هذا التتابع — من HIF‑1α إلى STOML2 إلى PGAM5 إلى PINK1 — كمسار وقائي أساسي.
تدريب الدماغ بنقص أكسجين متقطع
اختبرت الدراسة أيضًا استراتيجية “تكييف” تسمى نقص الأكسجين المتقطع، حيث تعرّضت الفئران لدورات قصيرة ومتكررة من انخفاض وعودة الأكسجين إلى الطبيعي قبل مواجهة نقص الأكسجين طويل الأمد. أطلقت هذه المعالجة المسبقة نفس مسار HIF‑1α/STOML2/PGAM5/PINK1 وعزّزت الميتوفاجي في الدماغ. بشكل لافت، حافظت الفئران التي خضعت لنقص الأكسجين المتقطع على أداء الذاكرة حتى بعد أسبوع من نقص الأكسجين المستمر، بينما تدهورت حالة الحيوانات غير المعالجة. تشير هذه النتائج إلى أن فترات محكمة من انخفاض الأكسجين يمكن أن تدرب الخلايا العصبية على تفعيل آليات التنظيف الذاتي بفعالية أكبر، تمامًا كما يُعِدّ التمرين العضلات للتعامل مع الإجهاد.
ما الذي يعنيه هذا لحماية الدماغ
بعبارات مبسطة، توضح الدراسة أن الخلايا العصبية تمتلك خطة طوارئ مدمجة لمواقف انخفاض الأكسجين: تستشعر التغيير بسرعة، ترفع سلسلة وقائية من البروتينات، وتطهر محطات الطاقة التي تعمل بشكل خاطئ قبل أن تتسبب في تلف واسع النطاق. عندما تُعرَض هذه الخطة للانقطاع، تصبح خلايا الدماغ أكثر عرضة للخطر. من خلال رسم خريطة هذا المسار بتفصيل وإظهار أن نقص الأكسجين المتقطع يمكن أن يفعّله بأمان، يشير العمل إلى علاجات مستقبلية قد تحاكي أو تعزز هذا الدفاع الطبيعي. قد تساعد مثل هذه الأساليب يومًا ما في حماية الدماغ من السكتات الدماغية واضطرابات التنفس المرتبطة بالنوم وحالات أخرى تتعرض فيها إمدادات الأكسجين للخطر.
الاستشهاد: Li, Y., Xu, Z., Tian, Z. et al. Novel mechanism of neuronal hypoxia response: HIF-1α/STOML2 mediated PINK1-dependent mitophagy activation against neuronal injury. Cell Death Discov. 12, 104 (2026). https://doi.org/10.1038/s41420-026-02960-z
الكلمات المفتاحية: نقص أكسجة الدماغ, المايتوفاجي, حماية الخلايا العصبية, نقص الأكسجين المتقطع, الميتوكوندريا