Clear Sky Science · ar
يعزز PDHA1 المقاومة ضد الفيروپتوزيس في سرطان البروستاتا المقاوم للانويكيس عن طريق زيادة التعبير عن AIFM2
لماذا ترفض بعض خلايا سرطان البروستاتا الموت
عندما تنفصل الخلايا السرطانية عن ورم وتدخل مجرى الدم، يفترض أن يموت معظمها قبل أن تصل إلى عضو جديد. ومع ذلك، ينجو طيف خطير من الخلايا، ويسافر ويؤسس نقائل غالبًا ما تكون قاتلة. تطرح هذه الدراسة سؤالاً أساسياً: ما الذي يمكّن بعض خلايا سرطان البروستاتا من مقاومة شكل من أشكال الموت الخلوي الذي عادةً ما يحدث عندما تفقد الخلايا اتصالها بنسيجها الأصلي؟ من خلال كشف دائرة بقاء مخفية داخل هذه الخلايا، يشير البحث إلى طرق جديدة لعرقلة النقائل من مصدرها.
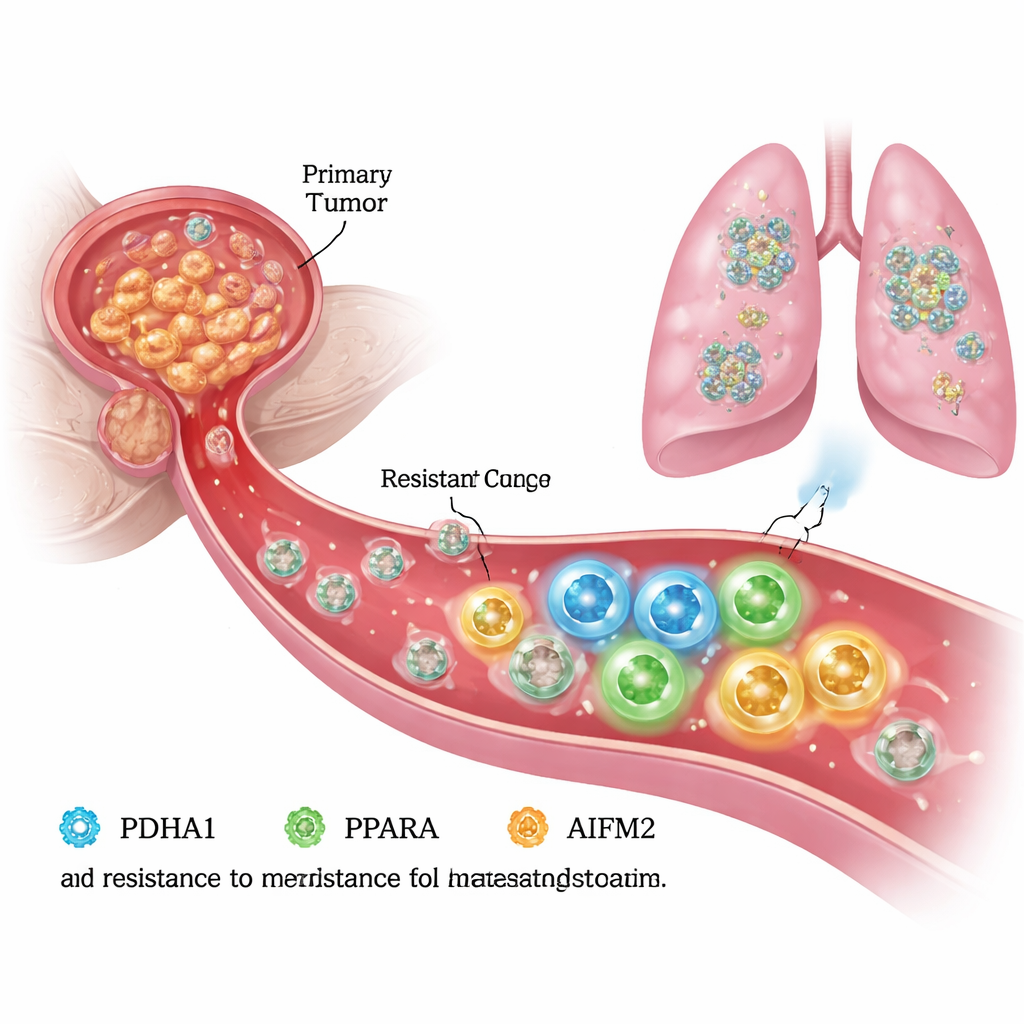
الهروب من الموت في مجرى الدم
للانبثاث، يجب أن تتحمل خلايا سرطان البروستاتا الحياة دون دعم النسيج المحيط بها، المعروف بالمصفوفة الخارجية للخلايا. في ظل هذه الظروف «المنفصلة»، تخضع الخلايا السليمة لموت مبرمج يُدعى الانويكيس، والعديد من الخلايا السرطانية تكون عرضة أيضاً لعملية موت مرتبطة بالحديد تسمى الڤيروپتوزيس. أنشأ المؤلفون خلايا سرطان بروستاتا مقاومة للانويكيس في المختبر وقارنوها بخلاياها «الأبوية» الأصلية. وجدوا أن الخلايا المقاومة لم تكتفِ بالهجرة والارتشاح بشكل أكبر، بل نجت أيضاً بشكل أفضل عند الانفصال، مما يوحي بأنها أعادت برمجة آلياتها الداخلية لتجنب الڤيروپتوزيس والاستمرار في النمو.
تحول أيضي يقوم بوظيفة ثانية
بالغوص أعمق، ركز الفريق على إنزيم أيضي يُدعى PDHA1، المعروف أساساً بمساعدته الخلايا على تحويل البيروفات المستمدة من السكر إلى أسيتيل‑CoA في المتقدرات، مما يزود إنتاج الطاقة. في الخلايا المقاومة للانويكيس، كانت مستويات ونشاط PDHA1 أعلى بشكل ملحوظ، وأظهرت عينات المرضى مزيداً من PDHA1 في الأورام الأساسية لدى رجال انتشر سرطانهم إلى العقد الليمفاوية أو إلى مواقع بعيدة. عندما قلل الباحثون من PDHA1، فقدت الخلايا المقاومة جزءاً كبيراً من قدرتها على الحركة والارتشاح والبقاء. والمفاجئ أن جزءاً كبيراً من PDHA1 في هذه الخلايا لم يعد محصوراً داخل المتقدرات؛ انتقل إلى النواة، حيث يُغلف الحمض النووي مع الهيستونات التي يمكن تعديلها كيميائياً لتشغيل أو إيقاف الجينات.
إعادة كتابة نشاط الجينات لعرقلة الڤيروپتوزيس
داخل النواة، بدا أن PDHA1 يغذي الإنتاج المحلي لأسيتيل‑CoA، وهو لبنة أساسية لتعديل الأسيتلة على الهيستونات. أظهر المؤلفون أن PDHA1 النووي عزز علامة محددة، أسيتلة H3K9، في منطقة التحكم بجين يُسمى PPARA. عمل هذا التغير كأنه يرخّي «بكرات» الكروماتين، مما يسهل تشغيل PPARA. بدورها، عملت PPARA كمفتاح رئيسي زاد إنتاج بروتين آخر، AIFM2، عن طريق الارتباط بمحفزاته ورفع نسخها. بدلاً من تعديل جين AIFM2 مباشرة، عمل PDHA1 عبر PPARA، مثبتاً مساراً متعدد الخطوات من التغير الأيضي إلى تعديل تنظيم الجينات.
بناء درع ضد الضرر الناتج عن الحديد
يُعرف AIFM2 بأنه فرامل داخلية للڤيروپتوزيس: يساعد في حماية الدهون في أغشية الخلايا من الأكسدة المدمرة. في خلايا سرطان البروستاتا المقاومة، أدت زيادة PDHA1 إلى رفع مستويات AIFM2، بينما خفضت مقاطعة PDHA1 تلك المستويات. أظهرت الاختبارات الوظيفية أن تقليل PDHA1 ضاعف معالم الڤيروپتوزيس—مزيد من أنواع الأكسجين التفاعلية، ومزيد من ضرر الدهون، وانخفاض في جهد غشاء المتقدرة، وانكماش مميز للمتقدرات—لا سيما عند تعريض الخلايا للمادة المحفزة للڤيروپتوزيس إراستين. عكس الإفراط في التعبير عن AIFM2 هذه التأثيرات، محققاً إنقاذ بقاء الخلايا في الأطباق واستعادة النقائل الرئوية في الفئران، حتى عندما كان PDHA1 مكبوحاً. أكد هذا أن AIFM2 هو منفذ حاسم لقاعدة مقاومة الڤيروپتوزيس التي يقودها PDHA1.
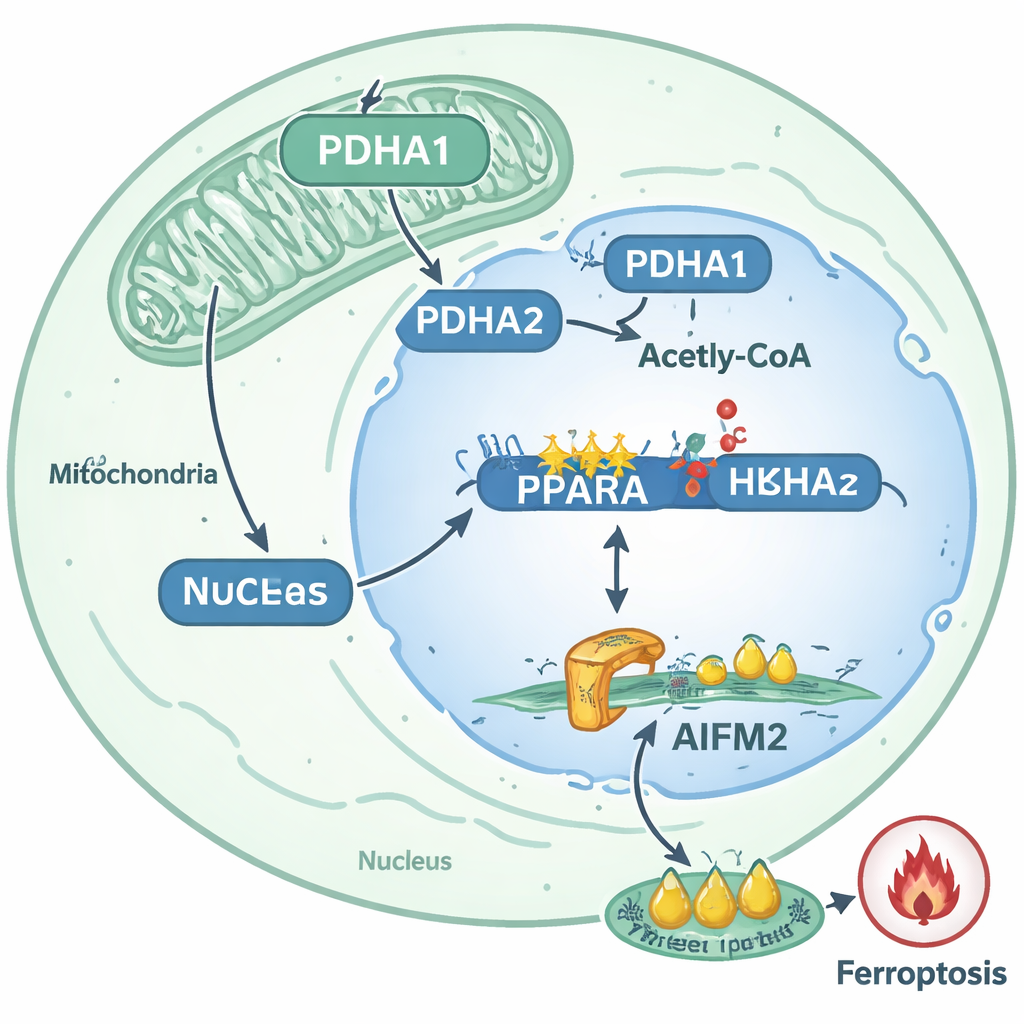
من الدائرة الجزيئية إلى أفكار علاجية
من خلال رسم خريطة هذه الأحداث، تحدد الدراسة مساراً واضحاً يجعل خلايا سرطان البروستاتا المنفصلة أصعب في القتل: يتحرك PDHA1 إلى النواة، يزيد أسيتلة الهيستون عند جين PPARA، يعزز نشاط PPARA، ومن ثم يرفع مستويات AIFM2 لعرقلة الڤيروپتوزيس. يرتبط هذا المسار بقوة بالسلوك النُّقيلي في أورام المرضى وفي النماذج الحيوانية. للمطالعة العامة، الخلاصة هي أن بعض الخلايا السرطانية تعيد توظيف إنزيم أيضي اعتيادي كأداة إبجِنِيتِية تعيد توصيل نشاط الجينات وتبني درعاً كيميائياً حيوياً ضد شكل قوي من الموت الخلوي. يقترح المؤلفون أن أدوية تستهدف PDHA1 أو PPARA أو AIFM2—أو علاجات تُحرّض الڤيروپتوزيس مقصوداً—قد تُجمع في المستقبل لسحب ميزة البقاء هذه من خلايا سرطان البروستاتا النُّقيليَّة وجعلها أكثر عرضة أثناء رحلتها الأكثر هشاشة: القفزة من عضو إلى آخر.
الاستشهاد: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
الكلمات المفتاحية: انتقال سرطان البروستاتا, الڤيروپتوزيس, مقاومة الانويكيس, PDHA1, AIFM2