Clear Sky Science · ar
ليبوكالين-2 الخلوية للعظام تنظّم تكوين العظم محليًا عبر الفِيروبتوس المعتمد على الحديد وكبت Wnt
عندما تشكّل خلايا العظام بصمت صحة الجسم ككل
معظمنا يعتقد أن العظام هياكل جامدة، لكنها حيّة بخلايا تعيد بناء هيكلنا العظمي وتصلحه باستمرار. تكشف هذه الدراسة كيف لبروتين صغير واحد تصنعه خلايا العظم، يُدعى ليبوكالين-2، القدرة على إضعاف العظام من الداخل عبر إزعاج تعامل الخلايا مع الحديد والطاقة. فهم هذه العملية الخفية قد يفتح طريقًا لعلاجات جديدة لهشاشة العظام وفقدان العظام المرتبط بالشيخوخة.
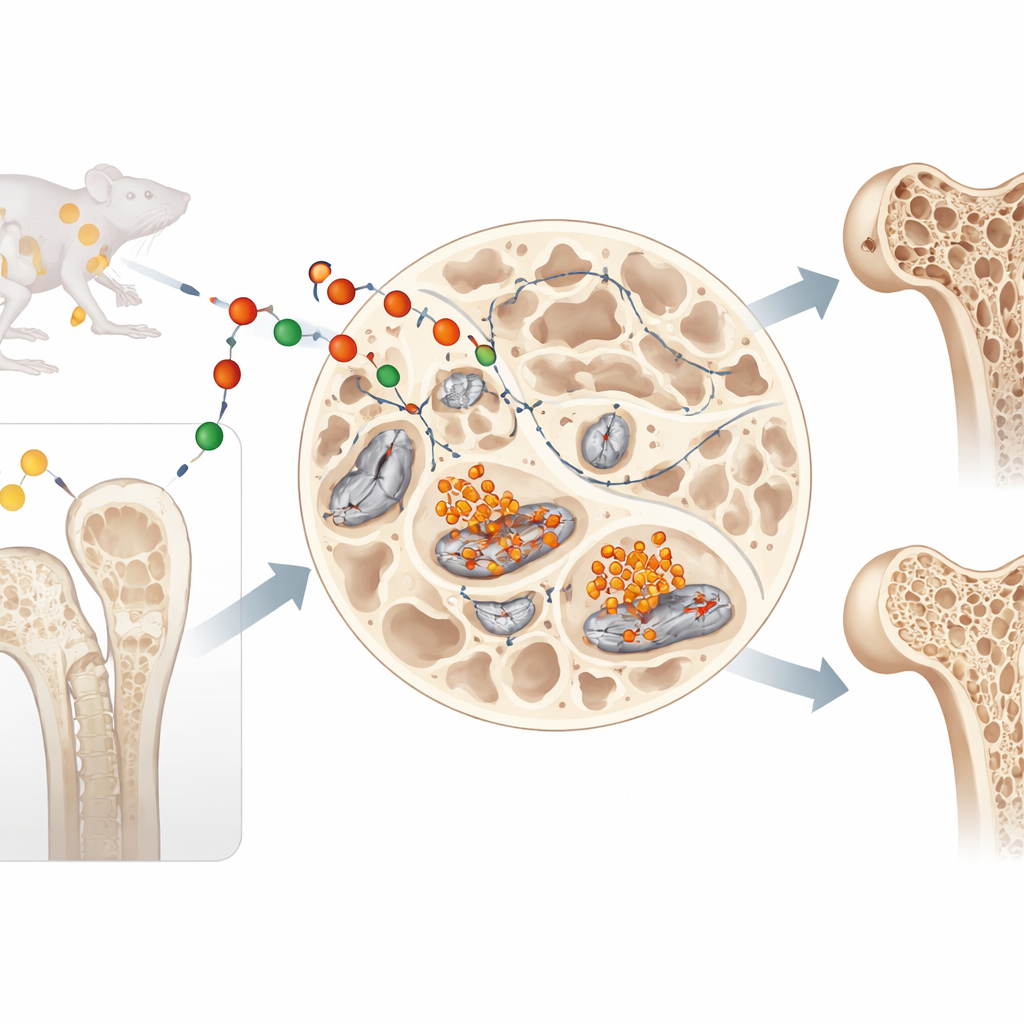
بروتين رسول ذو حياة مزدوجة
كان معروفًا أن ليبوكالين-2 يعمل كهرمون متجول ينتقل عبر الدم، يساهم في ضبط الشهية ووزن الجسم ويدافع عن العدوى عبر ربط الحديد. لكن مؤلفي هذه الورقة طرحوا سؤالًا مختلفًا: ماذا يفعل ليبوكالين-2 حيث يُنتَج مباشرة، داخل العظم نفسه؟ ركزوا على الخلايا العظمية (الأوستيوسايتس)، خلايا طويلة العمر مدفونة داخل العظم تستشعر القوى الميكانيكية وتوجّه إعادة تشكيل العظم. وجد الفريق أن الخلايا العظمية لا تكتفي بصنع ليبوكالين-2 أثناء نضجها، بل تزيد بالفعل من إنتاجه، ما يشير إلى دور محلي قوي داخل الهيكل العظمي.
حمولة الحديد وموت خلوي أشبه بالصدأ
بما أن ليبوكالين-2 يمكنه نقل الحديد، اختبر الباحثون ما إذا كان يدفع لتراكم الحديد في الخلايا العظمية. في خلايا عظمية مزروعة، أدى إضافة ليبوكالين-2 إلى تراكم الحديد داخل الخلايا، وزيادة الجزيئات المؤكسدة الضارة، والتسبب في تلف شديد لأغشية الخلايا الغنية بالدهون. هذه سمات شكل موت خلوي مُعَرَّف حديثًا يُدعى الفِيروبتوس، حيث يعمل الحديد مثل الصدأ محرضًا تفاعلات كيميائية مدمرة. منعت مجمّعات الحديد (المُعالِبة) الضرر والموت الخلوي تمامًا، مؤكدة أن العملية تعتمد على الحديد.
المستقبل الحارِس وتداعيات الميتوكوندريا
لفهم كيف يدخل ليبوكالين-2 حمولة الحديد إلى الخلايا العظمية، توجه الفريق إلى مستقبل سطحي خلوي محدد، SLC22A17. عندما قلّلوا هذا المستقبل في خلايا شبيهة بالخلايا العظمية، لم يعد ليبوكالين-2 يدفع دخول الحديد أو الإجهاد التأكسدي أو موت الفِيروبتوس، حتى في ظروف فرط التحميل بالحديد. أظهرت الدراسة أيضًا أن ليبوكالين-2 يقوّض مَصادر طاقة الخلية: الميتوكوندريا. تسبب وجود ليبوكالين-2 الزائد في فقدان أغشية الميتوكوندريا الجهد الطبيعي وتقليل إنتاج الطاقة، بينما أدى إزالة ليبوكالين-2 إلى استعادة وظيفة الميتوكوندريا. في عظام الفئران التي تفتقر إلى ليبوكالين-2 في الخلايا العظمية، تم تشغيل جينات تدعم التنفّس الميتوكوندري ومراقبة الجودة، ما يوحي بأن هذه الخلايا كانت أكثر قدرة طاقية.
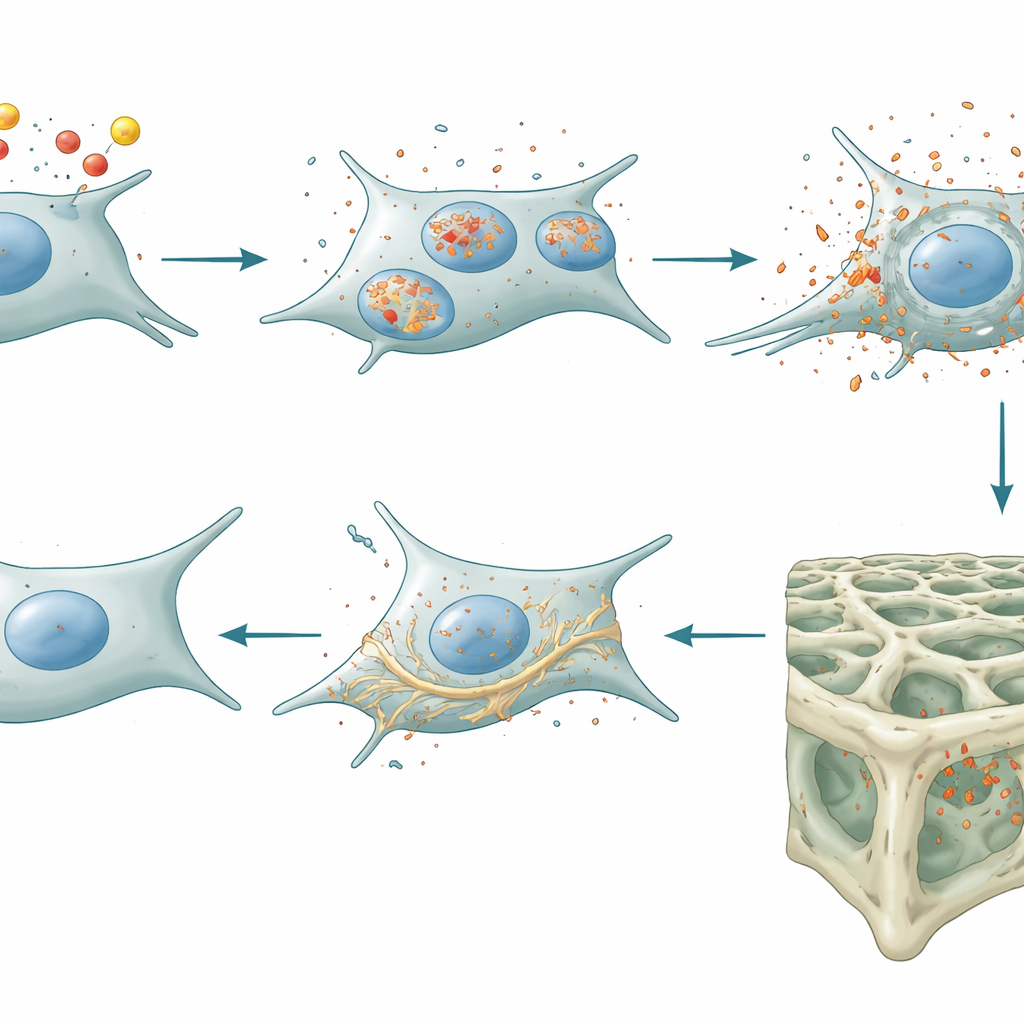
من إجهاد الخلايا إلى عظام أضعف، وكيف يساعد رفع المكابح
نظَر الباحثون بعد ذلك إلى فئران سليمة مُهندَسة لحذف ليبوكالين-2 تحديدًا في الخلايا المكوِّنة للعظم المتأخرة والمُخزّنة. تراكمت هذه الحيوانات على نحو أقل من الحديد داخل خلايا العظم وأظهرت دفاعات مضادة للأكسدة أقوى تحارب الفِيروبتوس. والأهم من ذلك، أنتجت أيضًا مستويات أدنى من بروتينين رئيسيين—سكليروستين وDKK1—الذي يعملان عادة كمكابح على مسار Wnt/β-catenin، وهو محرك رئيسي لتكوين العظم. مع تخفيف تلك المكابح، زاد الإشارة التي تشجع الخلايا البانية على بناء العظم. أكدت صور الميكرو-CT وتجارب وسم العظم النتيجة: الفئران الخالية من ليبوكالين-2 الخلوي بنت عظم إسفنجي (تربيكولار) أكثر وكثافة وترابطًا أفضل، وكان ذلك بشكل أساسي عبر تعزيز تكوين العظم بدلًا من إبطاء تحلله. ورغم هذه التغيرات في الهيكل العظمي، بقيت أوزان أجسامها وضبط السكر في الدم والتمثّل الغذائي ومستويات النشاط طبيعية، مما يدل على أن التأثير محلي في العظم وليس نتيجة هرمونية على مستوى الجسم كله.
ما معنى هذا للحفاظ على قوة العظام
ببساطة، تُظهر هذه الدراسة أن ليبوكالين-2 داخل خلايا العظم يعمل كمفتاح محلي يرفع مستويات الحديد، يجهد الميتوكوندريا، يهيّئ الخلايا لتلف الفِيروبتوس، ويخفّض مسار نمو رئيسي، ما يجتمع لتقييد تكوين العظم الجديد. عندما يُزال هذا المكبح الداخلي، تبقى الخلايا العظمية أكثر صحة، وتبعث إشارات داعمة للبناء بشكل أكبر، وتزداد كثافة وترابط العظم التربيكولاري دون الإخلال بالتمثّل الغذائي العام. وبما أن مستويات ليبوكالين-2 وعدم توازن الحديد يرتفعان مع التقدّم في العمر والالتهاب المزمن، قد يوفر استهداف نظام ليبوكالين-2–المستقبل مسارًا جديدًا لحماية العظام من «الصدأ» الداخلي.
الاستشهاد: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
الكلمات المفتاحية: صحة العظام, الخلايا العظمية, تمثّل الحديد, الفِيروبتوس, إشارة Wnt