Clear Sky Science · ar
البلعمة الميتوخلطية في سرطان البنكرياس: رؤى آلية وتداعيات لاستراتيجيات علاجية جديدة
لماذا تهم محطات الطاقة الخلوية في سرطان البنكرياس
سرطان القنوات البنكرياسية الغدي هو واحد من أكثر السرطانات فتكًا، ويرجع ذلك جزئيًا إلى أن الأورام تتعلم بسرعة مقاومة كل علاج تقريبًا يقدمه الأطباء. تستعرض هذه المقالة استعراضًا لاعبًا غير متوقع في قصة المقاومة هذه: البلعمة الميتوخلطية، وهو نظام الخلية الداخلي لتحديد وإعادة تدوير الميتوكوندريا البالية، تلك «محطات الطاقة» الصغيرة التي تولد الطاقة. قد يفتح فهم كيفية اختطاف سرطان البنكرياس لعملية التنظيف هذه مسارات جديدة لعلاجات أكثر فاعلية ودوامًا.
عناصر التنظيف الخلوية وحيل بقاء السرطان
تقوم الميتوكوندريا بأدوار تتجاوز توليد الطاقة؛ فهي تساهم في تنظيم الاستقلاب، والموت الخلوي، والتعامل مع الجزيئات الضارة المعروفة باسم أنواع الأكسجين التفاعلية. عندما تتعرض الميتوكوندريا للتلف أو تصبح زائدة، تستخدم الخلايا البلعمة الميتوخلطية لوصمها وإزالتها. يمكن أن يحدث ذلك عبر مسارين رئيسيين. الأول، المعروف بمسار PINK1/Parkin، يعتمد على مستشعر للضرر (PINK1) وإنزيم وسم (Parkin) لوضع علامة على الميتوكوندريا المعطوبة لتدميرها. المسار الآخر يستخدم بروتينات مستقبلية مثل BNIP3 وNIX وFUNDC1 الموجودة على أسطح الميتوكوندريا لربطها مباشرة بأكياس التخلص من النفايات الخلوية، المسماة الأوتوفاجوسومات، دون خطوة الوسم نفسها. كثيرًا ما تعمل هذه المسارات معًا، مما يمنح الخلايا وسائل مرنة لتعديل مخزون الميتوكوندريا استجابةً لضغوط مثل نقص الأكسجين أو التعرض للأدوية. 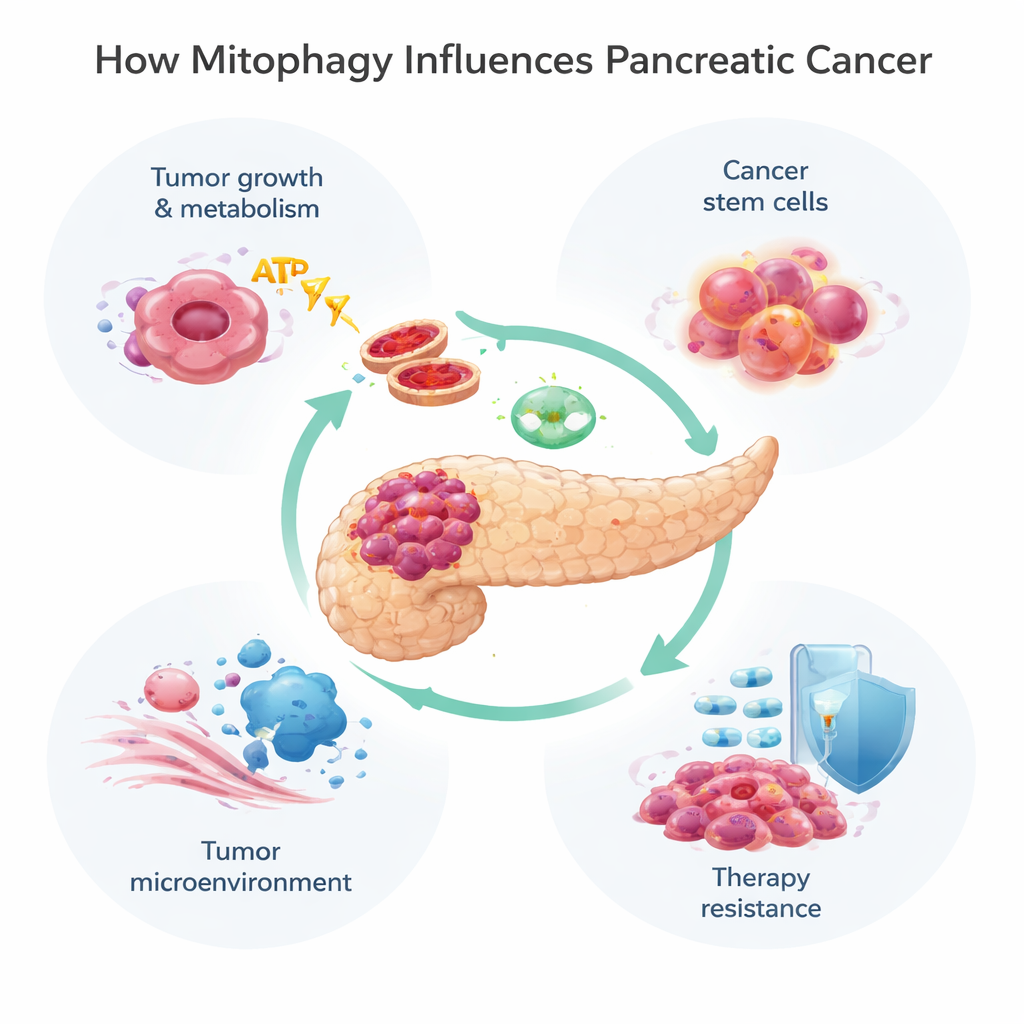
كيف تعيد الأورام البنكرياسية تشكيل استخدام الطاقة
تعيش أورام البنكرياس في بيئة قاسية: إمدادها بالدم والأكسجين ضعيف ومحاطة بنسيج كثيف يشبه الندبة. للبقاء، تعيد الخلايا السرطانية توصيل أنظمة طاقتها، وغالبًا ما تتحول من التنفس القائم على الأكسجين في الميتوكوندريا إلى عملية أكثر بدائية لحرق السكر تعرف بالتحلل السكري (اللاهوائي). تساعد البلعمة الميتوخلطية في ضبط هذه التحولات. في مراحل التطور المبكرة للورم، يؤدي فقدان PINK1 أو Parkin إلى تسريع تكوّن السرطان عبر السماح بتراكم الحديد، وزيادة أنواع الأكسجين التفاعلية، ودفع الخلايا نحو التحلل السكري. في الوقت نفسه، يمكن لبروتين بلعمية ميتوخلطية آخر، NIX، أن يساعد في إزالة الميتوكوندريا التي لا تزال تعمل، مما يدفع الخلايا أكثر نحو الاستقلاب التحللي ونمو أسرع. بالمقابل، يظهر BNIP3 نمطًا أكثر تعقيدًا: ففي المراحل المبكرة يظهر، ثم يُكبت لاحقًا في العديد من الأورام المتقدمة، وعند استعادته يمكن أن يبطئ نمو الخلايا السرطانية، ما يشير إلى أن بعض مسارات البلعمة الميتوخلطية تقيد السرطان بينما تغذّي مسارات أخرى نموه.
خلايا سرطان الجذعية وبيئة الورم المحيطة
ليست كل الخلايا السرطانية متماثلة. مجموعة صغيرة، غالبًا ما تُسمى خلايا جذعية سرطانية، قادرة على التجدد الذاتي، وبذر أورام جديدة، ومقاومة العلاج الكيميائي بشكل خاص. في سرطان البنكرياس، تعتمد هذه الخلايا على البلعمة الميتوخلطية للحفاظ على مرونتها الاستقلابية. بروتين معدل يُدعى ISG15 يدعم هذه العملية ويساعد في الحفاظ على صفاتها الشبيهة بالجذعية، رابطًا البلعمة الميتوخلطية مباشرةً بالانتكاس وفشل العلاج. إلى جانب الخلايا السرطانية نفسها، تشكل البلعمة الميتوخلطية أيضًا بيئة الورم الدقيقة — مزيج الخلايا الداعمة، والخلايا المناعية، والنسيج الضام المحيط بالورم. على سبيل المثال، يمكن أن تُدفع الخلايا الليفية المرتبطة بالسرطان إلى ما يُسمى «تأثير واربرغ العكسي»، حيث تزيد من بلعمها الميتوخلطي والتحلل السكري لديها، ثم تزود الورم بمنتجات ثانوية غنية بالطاقة. تؤثر البلعمة الميتوخلطية أيضًا في كيفية تعرف الخلايا المناعية على السرطان ومهاجمته، من خلال تغيير عرض إشارات مناعية مثل MHC‑I وعناصر الكبح مثل PD‑L1 التي تستخدمها الأورام للاختباء.
لماذا يمكن أن يغير منع أو تعزيز التنظيف استجابة الدواء
تتلف العديد من العلاجات القياسية والتجريبية لسرطان البنكرياس، بما في ذلك الدواء الكيميائي جيمسيتابين وعقار جديد مستهدف ضد طفرة KRAS‑G12D الشائعة، الميتوكوندريا. غالبًا ما تستجيب الخلايا الورمية بتشغيل البلعمة الميتوخلطية، ما يزيل التلف ويمكّنها من النجاة. تظهر الدراسات أن البلعمة الميتوخلطية المدفوعة بـPINK1 يمكن أن تخفف من تأثيرات القتل للعلاج الكيميائي وبعض المركبات الطبيعية، مما يساعد الخلايا السرطانية على النجاة. من ناحية أخرى، في ظل ظروف معينة، قد يؤدي دفع البلعمة الميتوخلطية إلى أقصى حد — خاصة عبر BNIP3 وNIX — إلى تجريد الخلايا من عدد كبير من الميتوكوندريا العاملة، مما يدفعها إلى أزمة طاقة ويعزز موت الخلايا. هذه الطبيعة المزدوجة تعني أن البلعمة الميتوخلطية قد تحمي الأورام من العلاج أو، إذا تم توجيهها بالطريقة المناسبة، تجعلها أكثر عرضة. 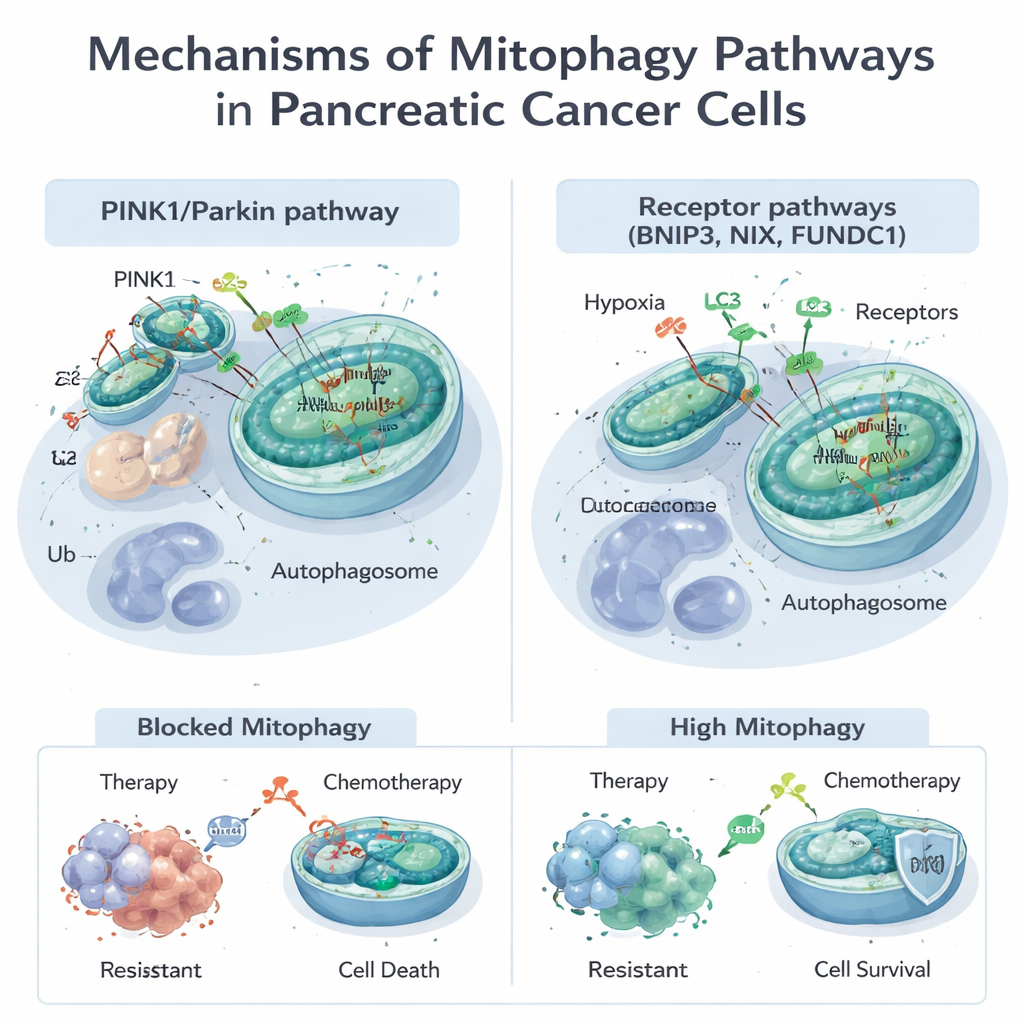
أفكار علاجية جديدة والحاجة إلى مطابقة ذكية للمرضى
بما أن البلعمة الميتوخلطية تجلس عند تقاطع الاستقلاب واستجابات الإجهاد والموت الخلوي، فهي هدف جذاب لعلاجات التوليفة. تركز استراتيجيات الأدوية الحالية غالبًا على التأثير غير المباشر: بعض المركبات تتداخل مع انقسام واندماج الميتوكوندريا؛ وأخرى، مثل الكلوروكين والهيدروكسي كلوروكين، تمنع المراحل النهائية لعملية إعادة التدوير عن طريق تعطيل اندماج أكياس النفايات مع الحواجز الحمضية للتحلل. تختبر عدة تجارب سريرية هذه الأدوية جنبًا إلى جنب مع العلاج الكيميائي القياسي في سرطان البنكرياس. ومع ذلك، كانت النتائج حتى الآن مختلطة — يستفيد بعض المرضى بينما لا يستفيد آخرون. جزء من المشكلة أن الأورام تختلف اختلافًا واسعًا في مستويات البلعمة الميتوخلطية الأساسية وملفاتها الاستقلابية: يعتمد بعضها اعتمادًا كبيرًا على التنفس الميتوكوندري، بينما يعتمد البعض الآخر على التحلل السكري. يجادل المؤلفون بأن النجاح المستقبلي سيعتمد على مؤشرات حيوية وتواقيع جينية أفضل لتجميع المرضى حسب نشاط البلعمة الميتوخلطية واستخدامهم للطاقة، وعلى تطوير أدوية أكثر دقة تعدل مسارات بلعمية ميتوخلطية محددة بدلًا من تفعيل التلقيم العام للبلمرة أو إيقافها بشكل غامض. للقراء العامين، الخلاصة الأساسية هي أن تعلم قراءة هذا النظام التنظيفي الميتوكوندري وتعديله بعناية قد يساعد في تحويل سرطان البنكرياس من خصم عنيد إلى مرض أكثر قابلية للإدارة.
الاستشهاد: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
الكلمات المفتاحية: سرطان البنكرياس, البلمرة الميتوخلطية, الميتوكوندريا, مقاومة العلاج الكيميائي, استقلاب الورم