Clear Sky Science · ar
الخلايا الجذعية الميزنشيمية المُهيئة تخفف تليف البلهارسيا عن طريق تعزيز تحول الفئات الماكروفاجية والبلع الخلوي عبر محور Itgb2-Rac1
تقليل ندوب الكبد الناتجة عن طفيلي شائع
البلهارسيا، المرض الطفيلي الذي يصيب أكثر من 200 مليون شخص حول العالم، غالبًا ما يترك ندوبًا عنيدة في الكبد حتى بعد قتل الديدان. هذه الندوب، المعروفة بالتليف، قد تتطور إلى تليف كبدي متقدّم وفشل كبدي مهدد للحياة. تستكشف هذه الدراسة علاجًا خلويًا جديدًا يعلّم خلايا الجهاز المناعي الذاتية كيفية تنظيف التلف بكفاءة أكبر، مقدمًا منظورًا جديدًا لعكس ندوب الكبد الناتجة عن الطفيليات.
لماذا يصعب شفاء ندوب الكبد
عندما تضع ديدان الشستوسوما بيضًا في الكبد، يبني الجهاز المناعي تجمعات خلوية محكمة—الحمالات—حول البيض. مع مرور الوقت، يؤدي هذا الاستجابة الوقائية إلى ترسيب نسيج ندبي مفرط، مما يجعل الكبد أكثر صلابة تدريجيًا. يلعب الماكروفاج دورًا محوريًا في هذا المشهد كطواقم التنظيف في الجسم. أحد الأنماط الفرعية، الماكروفاجات «الملتهبة»، يغذي التلف بإطلاق إشارات كيميائية قاسية؛ بينما النوع الآخر، الأكثر «حسمًا» أو المساهم في الشفاء، يساعد على تفكيك النسيج الندبي وتهدئة الالتهاب. السؤال المركزي في هذا العمل هو ما إذا كان بإمكاننا دفع الماكروفاجات بأمان من الحالة الضارة إلى الحالة الشافية.
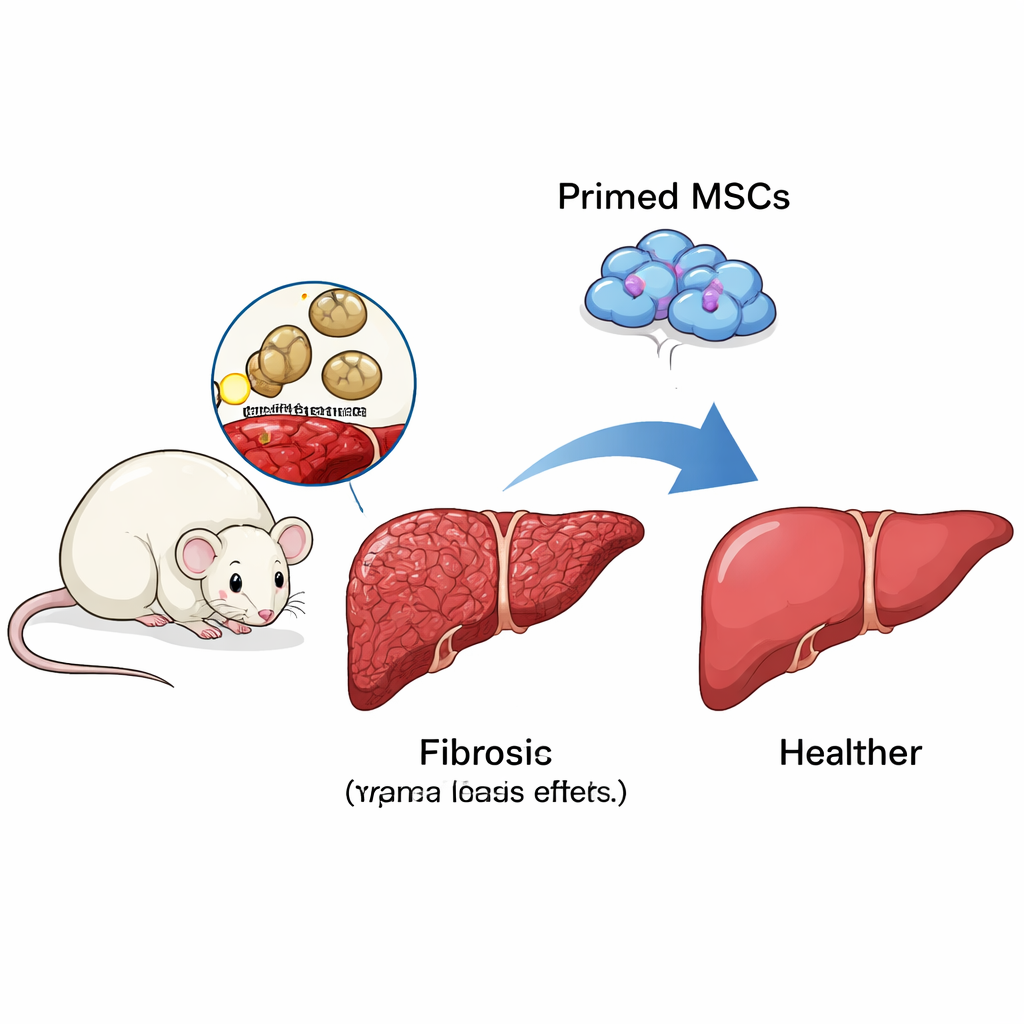
تدريب الخلايا الجذعية لتوجيه الجهاز المناعي
الخلايا الجذعية الميزنشيمية (MSCs)—خلايا متعددة الاستخدامات توجد في نخاع العظام وأنسجة أخرى—حظيت بالاهتمام كعلاج محتمل لتليف الكبد. لكنها بمفردها لا تعمل دائمًا بشكل كافٍ. وجد الباحثون أن «تهيئة» MSCs في المختبر بإشارتين مناعيتين، IFN‑γ وLPS، حسّنت أدائها بشكل كبير في الفئران المصابة بشستوسوما جاپونيكوم. مقارنةً بالحيوانات غير المعالجة أو تلك التي أعطيت MSCs غير مهيأة، ظهرت كبد الفئران التي تلقت MSCs المهيأة أكثر صحة بالعين المجردة، وكسبت وزنًا أكبر، وأظهرت حمالات أصغر بكثير وترسّبًا أقل للكولاجين تحت المجهر. كما انخفضت مؤشرات الخلايا النشطة المكونة للندوب، مما يشير إلى انخفاض حقيقي في التليف، وليس مجرد تغييرات تجميلية.
إعادة برمجة طواقم التنظيف في الجسم
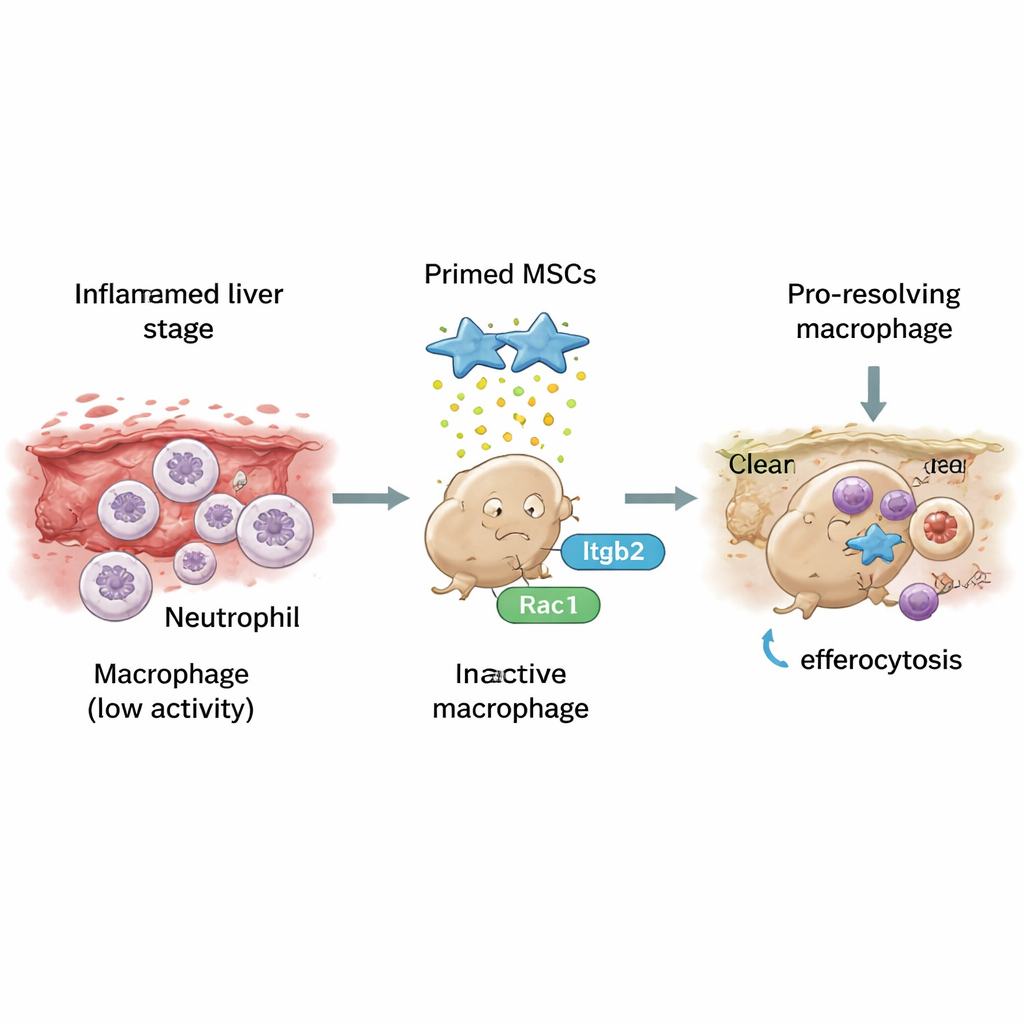
باتباع نهج أعمق، قاس الفريق كيف أثّرت MSCs المهيأة في سلوك الماكروفاجات. في الكبد المعالج، كان هناك ماكروفاجات ملتهبة أقل والمزيد من النمط الفرعي المسهم في الحسم الذي يجيد تفكيك النسيج الندبي. في الوقت نفسه، انخفض مستوى الجزيئات الالتهابية الكلاسيكية، في حين حافظت عوامل الشفاء على توازن مفيد بدلًا من أن تُدفع إلى تطرف. عندما منع الباحثون وصول الماكروفاجات الملتهبة الجديدة إلى الكبد، تقلصت كل من أعداد الخلايا الحاسمة والفوائد على التليف. وهذا يشير إلى أن MSCs المهيأة لا تضيف خلايا جديدة فحسب، بل تحوّل الماكروفاجات الملتهبة الوافدة إلى شكل أكثر هدوءًا وموجهًا نحو الإصلاح.
مساعدة الماكروفاجات على «الأكل» نحو الشفاء
انتقلت الدراسة بعد ذلك إلى عملية تُسمى البلع الخلوي—«أكل» الخلايا الميتة بشكل منظم، وخصوصًا العدلات المنتهية العمر، وهو نوع آخر من خلايا المناعة. في الفئران المصابة التي أعطيت MSCs المهيأة، كانت الماكروفاجات الكبدية أكثر احتمالًا بكثير لأن تُرى وهي تحتوي على عدلات مهضومة، علامة على تنظيف نشط. في الأطباق المختبرية، أصبحت الماكروفاجات المعرضة لـMSCs المهيأة أفضل في ابتلاع العدلات المبرمَزة للموت، وبالتوازي غيرت نشاطها الجيني نحو ملف تعبيري مساعد على الحسم. حدَّد الباحثون مقبضًا جزيئيًا رئيسيًا لهذا التغيير: مستقبل يُدعى Itgb2 على الماكروفاجات، يتواصل مع مفتاح داخلي، Rac1، الذي يتحكم بهيكل الخلية وحركة الالتقام. عززت MSCs المهيأة نشاط كل من Itgb2 وRac1؛ وإعاقة أي منهما قلّلت بشدة من البلع الخلوي وعكست التحول نحو الماكروفاجات ذات نمط الشفاء.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، توضح هذه الدراسة أن الخلايا الجذعية المهيأة خصيصًا يمكن أن تعمل كـ«مدرّبات» لخلايا الجهاز المناعي بعد البلهارسيا، فتشجّعها على التوقف عن تأجيج الالتهاب وبدلًا من ذلك تنظيف الحطام والنسيج الندبي بشكل أكثر كفاءة. من خلال تفعيل مسار Itgb2–Rac1، تساعد هذه MSCs المهيأة الماكروفاجات على التخلص بسلاسة من الخلايا الميتة، ثم تبني شخصية تميل إلى حل الندبات. وبينما لا يزال هناك الكثير لإنجازه قبل تجربة هذا النهج على البشر، تقدّم الدراسة خارطة طريق آلية واضحة لتصميم علاجات تعتمد على MSCs لا تكتفي بكبح الضرر فحسب، بل تساعد الكبد بنشاط على إعادة بناء نفسه بعد العدوى الطفيلية.
الاستشهاد: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
الكلمات المفتاحية: البلهارسيا, تليف الكبد, الخلايا الجذعية الميزنشيمية, الماكروفاجات, البلع الخلوي