Clear Sky Science · ar
استهداف إشارات NXPH4/ALDH1L2 يثبط مقاومة الإنزالوتاميد في سرطان البروستاتا
لماذا يهم هذا مرضى سرطان البروستاتا
يعتمد كثير من الرجال المصابين بسرطان البروستاتا المتقدم على دواء قوي يعيق الهرمونات يُدعى الإنزالوتاميد. في البداية غالبًا ما يكون فعالًا، فيقلص الأورام ويبطئ تقدّم المرض. لكن لدى معظم المرضى يجد السرطان في نهاية المطاف طريقًا للتحايل على الدواء ويبدأ بالنمو مجددًا. تبحث هذه الدراسة في كيفية حدوث هذا الهروب وتبرز نقطة ضعف جديدة في الأورام المقاومة للأدوية — ما يوفر مسارًا محتملاً لجعل العلاجات الحالية تعمل لفترة أطول وبفعالية أكبر.
علاج شائع يواجه مرضًا عنيدًا
يرتبط نمو سرطان البروستاتا ارتباطًا وثيقًا بالهرمونات الذكرية، أو الأندروجينات، التي تعمل عبر بروتين يُدعى مستقبل الأندروجين. صُمم الإنزالوتاميد لإيقاف هذا المستقبل وهو علاج قياسي عندما تتوقف الأورام عن الاستجابة للعلاج التقليدي بخفض الهرمونات. مع الأسف، تتكيف العديد من الأورام لتصبح ما يسميه الأطباء سرطان البروستاتا المقاوم للخصي. سعى مؤلفو هذه الورقة لاكتشاف أي الجينات تساعد خلايا السرطان على النجاة من الإنزالوتاميد، على أمل أن تعطيل هذه المساعدات قد يعيد فعالية الدواء.
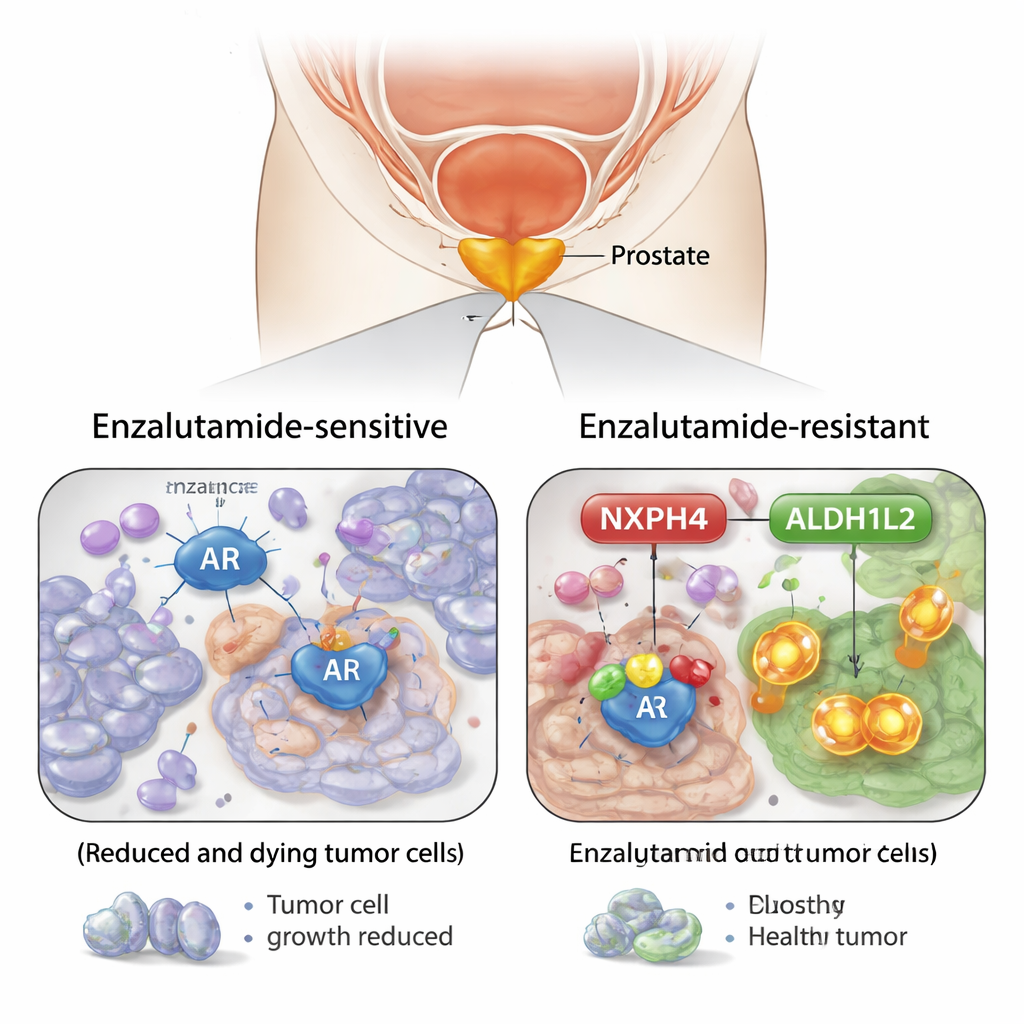
تسليط الضوء على جزيء مساعد مفاجئ
بمقارنة خلايا سرطان البروستاتا الحساسة للإنزالوتاميد مع خلايا أصبحت مقاومة، حدد الفريق بروتينًا يُدعى NXPH4 كلاعب رئيسي. كانت الخلايا المقاومة تُنتج كميات أكبر بكثير من NXPH4، وارتفعت مستوياته تدريجيًا عندما تعرّضت الخلايا للإنزالوتاميد مع مرور الوقت. أظهرت عينات الأنسجة من المرضى نفس النمط: مستويات أعلى من NXPH4 في الأورام الأكثر عدوانية وفي السرطانات التي لم تعد تستجيب للدواء. عندما خفّض الباحثون مستويات NXPH4 في الخلايا المقاومة، أصبحت هذه الخلايا أسهل في القتل بالإنزالوتاميد وشكلت مستعمرات أقل، سواء في الأطباق أو في الفئران. بالمقابل، جعلت زيادة إنتاج NXPH4 الخلايا أكثر صعوبة في المعالجة.
كيف تدفع الهرمونات NXPH4 إلى العمل
سألت الدراسة أيضًا لماذا يكون NXPH4 وفيرًا في هذه الأورام. أشارت الإجابة مرة أخرى إلى مستقبل الأندروجين. أظهر الباحثون أنه عندما عولجت الخلايا بالهرمون ديهدروتستوستيرون، ارتفعت مستويات NXPH4. عندما أضافوا مستقبل أندروجين إضافي، زاد NXPH4؛ وعندما قاموا بحجب المستقبل، انخفض NXPH4. أكدت تجارب مفصلة على الحمض النووي أن مستقبل الأندروجين يرتبط فعليًا بمنطقة التحكم في جين NXPH4، ويشغّله. هذا يعني أن نظام القيادة الهرموني نفسه الذي يغذي نمو سرطان البروستاتا يجهز الخلايا بـ NXPH4، ممهّدًا الطريق لمقاومة الدواء لاحقًا.
تشغيل مصانع الطاقة داخل الخلية
بتعمق أكبر، وجد الفريق أن NXPH4 يغيّر كيفية إدارة خلايا السرطان للطاقة والإجهاد داخل الميتوكوندريا، وهي مصانع الطاقة الصغيرة في الخلية. في ظل ظروف حجب الهرمونات، ينتقل جزء من NXPH4 إلى الميتوكوندريا ويرتبط ببروتين آخر، ALDH1L2، الذي يلعب دورًا حاسمًا في توليد NADPH، وهو جزيء رئيسي يساعد في التحكم في أنواع الأكسجين التفاعلية الضارة (ROS). في الخلايا المقاومة، يشكل NXPH4 وALDH1L2 مركبًا يعزز تنفس الميتوكوندريا، ويحافظ على الجهد الغشائي، ويزيد NADPH، ويخفض مستويات ROS. يحافظ هذا المزيج على صحة الميتوكوندريا ويسمح لخلايا السرطان بتحمّل الإجهاد الناجم عن الإنزالوتاميد بدلًا من الموت كما تفعل عادة.
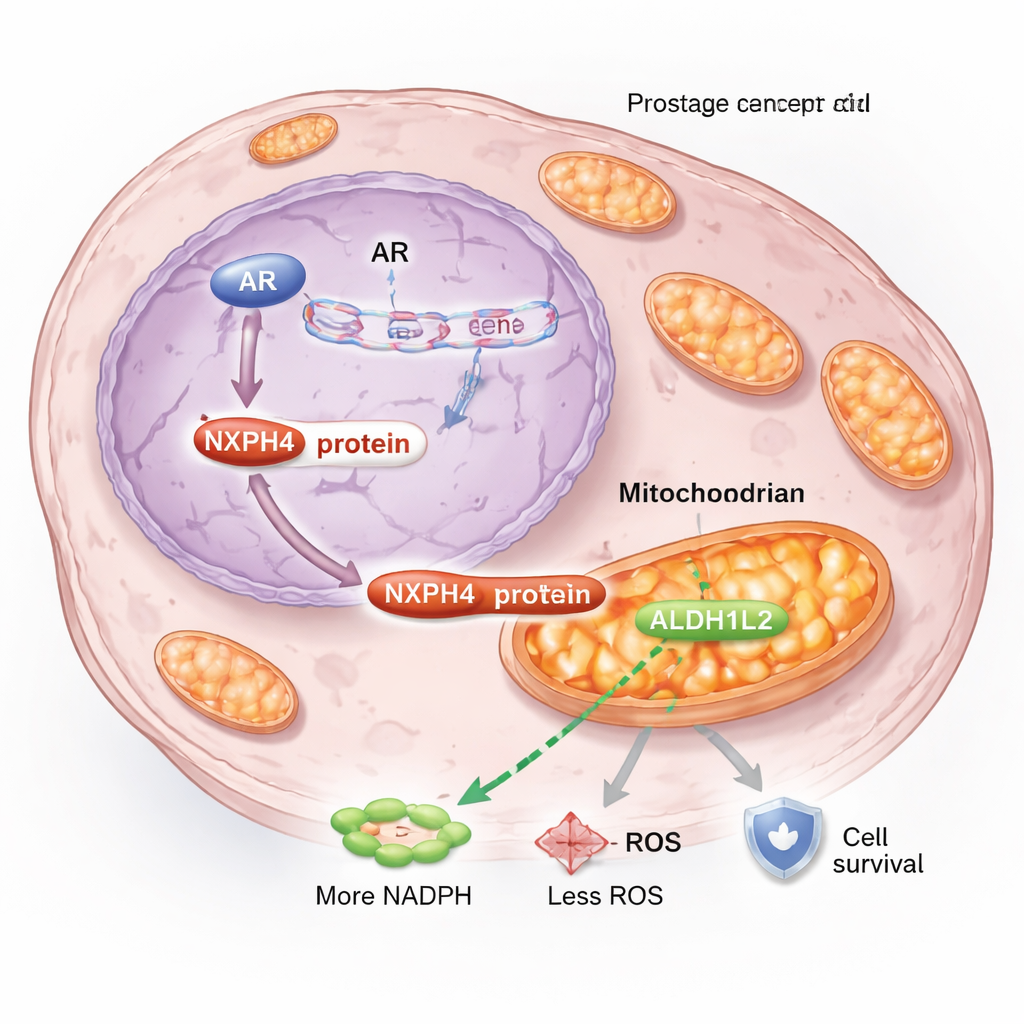
تفكيك دائرة المقاومة
عندما أعاق الباحثون هذا النظام الداعم للميتوكوندريا، كانت النتائج لافتة. أدى خفض NXPH4 في الخلايا المقاومة إلى تقليل نشاط الميتوكوندريا، ورفع الإجهاد التأكسدي، وإبطاء النمو، وجعل الخلايا أكثر عرضة بكثير للإنزالوتاميد. كان لإسكات ALDH1L2 تأثير مشابه ومحو الفوائد الواقية لزيادة NXPH4، مما يؤكد أن هذين البروتينين يعملان معًا. في نماذج الفئران، نمت الأورام التي تفتقر إلى NXPH4 ببطء أكبر، وأضاف الجمع بين فقدان NXPH4 والإنزالوتاميد تأثيرًا أكبر في تقليص الأورام مقارنةً بكل نهج بمفرده. تشير هذه النتائج إلى أن شراكة NXPH4–ALDH1L2 ليست مجرد أثر جانبي للمقاومة بل قوة دافعة وراءها.
ما الذي قد يعنيه هذا للعلاج المستقبلي
ببساطة، تُظهر هذه الدراسة أن بعض سرطانات البروستاتا تبقى على قيد الحياة أثناء علاج الإنزالوتاميد عن طريق إعادة توصيل مصدر طاقتها. يعمل NXPH4، الذي يشغّله مستقبل الأندروجين، مع ALDH1L2 داخل الميتوكوندريا لإبقائها تعمل بنشاط، وحمايتها من الضرر التأكسدي، ومساعدة خلايا الورم على اجتياز علاج حجب الهرمونات. قد يؤدي استهداف NXPH4، أو تداخل تفاعله مع ALDH1L2، إلى إضعاف دائرة البقاء هذه. على الرغم من عدم وجود أدوية تستهدف NXPH4 حاليًا، تبرز الدراسة هذا الثنائي الجزيئي كهدف واعد جديد. في المستقبل، قد يساعد الجمع بين الإنزالوتاميد وأدوية تعطل إشارة NXPH4‑ALDH1L2 المرضى على التفوق على سرطان البروستاتا المقاوم لفترة أطول.
الاستشهاد: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الإنزالوتاميد, تمثيل غذائي ميتوكوندري, NXPH4, ALDH1L2