Clear Sky Science · ar
يُثبّت Trim15 بروتين VDAC3 عبر اليوبيكويتينيشن لكبح الالتهام الذاتي وزيادة الحساسية الكيميائية في سرطان الخلايا الحرشفية للبلعوم السفلي
لماذا تهم هذه الدراسة السرطانية
سرطان الخلايا الحرشفية في البلعوم السفلي هو سرطان حلق يصعب علاجه، ذو معدلات بقاء منخفضة وقليل من الخيارات الفعالة عندما ينتشر أو يتوقف عن الاستجابة للأدوية. تكشف هذه الدراسة عن مسار خلوي مخفي يساعد في تقرير ما إذا كانت هذه الخلايا السرطانية تموت تحت العلاج أو تتأقلم بهدوء وتبقى على قيد الحياة. من خلال توضيح كيفية سيطرة بروتينين، Trim15 وVDAC3، على عمليات التنظيف الذاتي الخلوي واستجابات الإجهاد، يشير العمل إلى طرق جديدة لجعل أدوية العلاج الكيميائي الحالية أكثر فعالية.
سرطان حلق قاتل يختبئ في وضح النهار
يقع البلعوم السفلي عميقاً في الحلق، لذلك تنمو الأورام هناك غالباً دون أن تُكتشف حتى تصل إلى مرحلة متقدمة. عند هذه النقطة، يضطر الأطباء للاختيار بين جراحة عدوانية قد تؤثر بشدة على الكلام والبلع، أو نهج يحافظ على الأعضاء مثل العلاج الكيميائي والإشعاعي التي لا تُنقذ المرض دائماً. ونظراً لأن معدلات البقاء لم تتحسن كثيراً في العقود الأخيرة، يبحث الباحثون إلى ما وراء العلاجات التقليدية نحو البيولوجيا الأساسية التي تسمح لهذه الأورام بالنمو والانتشار ومقاومة الأدوية. تركز الدراسة الحالية على كيفية تعامل الخلايا السرطانية مع الميتوكوندريا التالفة — مصانع طاقتها — وكيف يشكل ذلك استجابتها للإجهاد والعلاج.
بروتين حارس يختفي
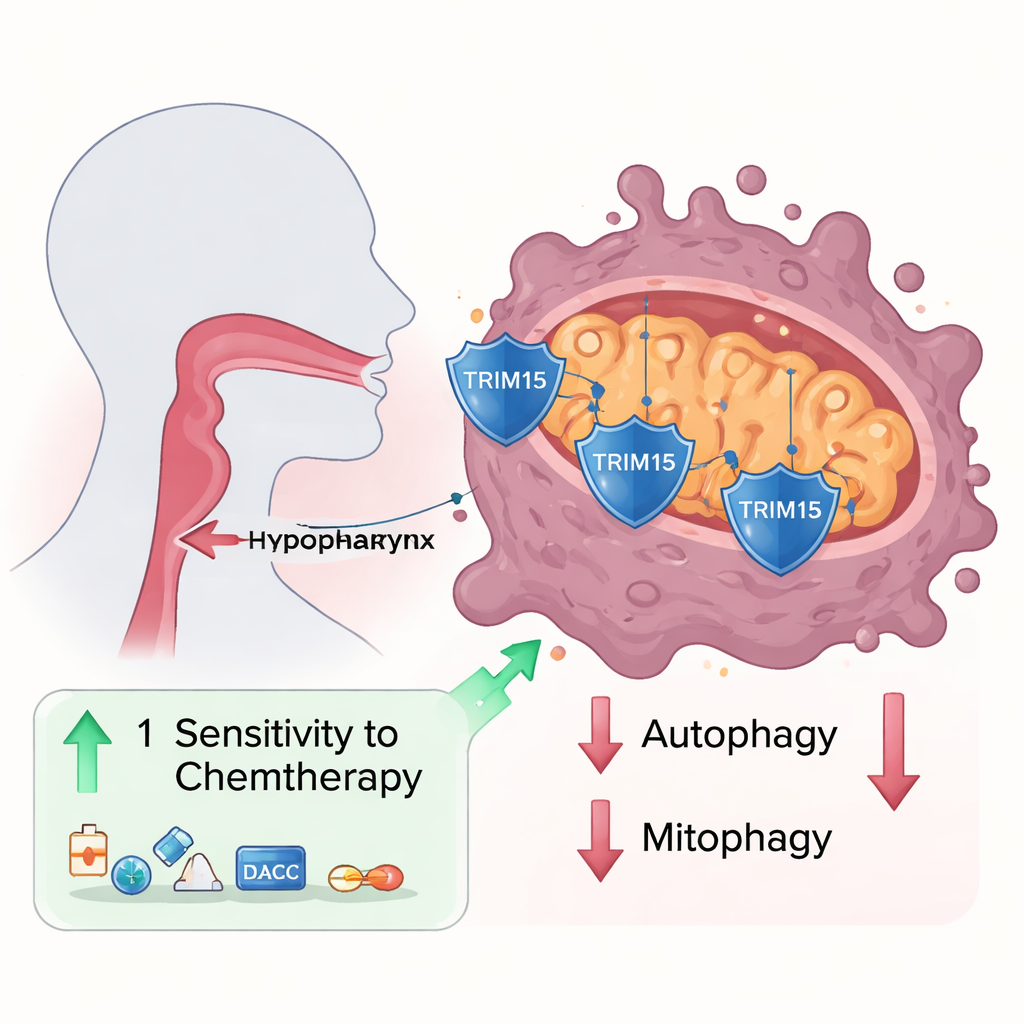
فحص الباحثون عينات أورام وسلاسل خلوية من سرطان البلعوم السفلي ووجدوا أن بروتيناً يُدعى Trim15 كان منخفضاً باستمرار مقارنة بالأنسجة السليمة المجاورة. عندما أجبروا الخلايا السرطانية على إنتاج كميات أكبر من Trim15، نمت الخلايا وتحركت بوتيرة أبطأ؛ وعند إزالته أصبحت الخلايا أكثر عدوانية. باستخدام تجارب سحب بيوكيميائية، اكتشفوا أن Trim15 يتفاعل فعلياً مع بروتين آخر، VDAC3، الموجود في الغشاء الخارجي للميتوكوندريا ويعمل كبوابة للجزيئات التي تتحرك داخلها وخارجها. بدلاً من أن يعلّم Trim15 على تمييز VDAC3 للتدمير، يضيف نوعاً معيناً من الوسوم الجزيئية الذي يعمل فعلياً على تثبيت VDAC3، محافظاً على مستوياته مرتفعة.
كيف تعيد الخلايا السرطانية تدوير مصانع طاقتها
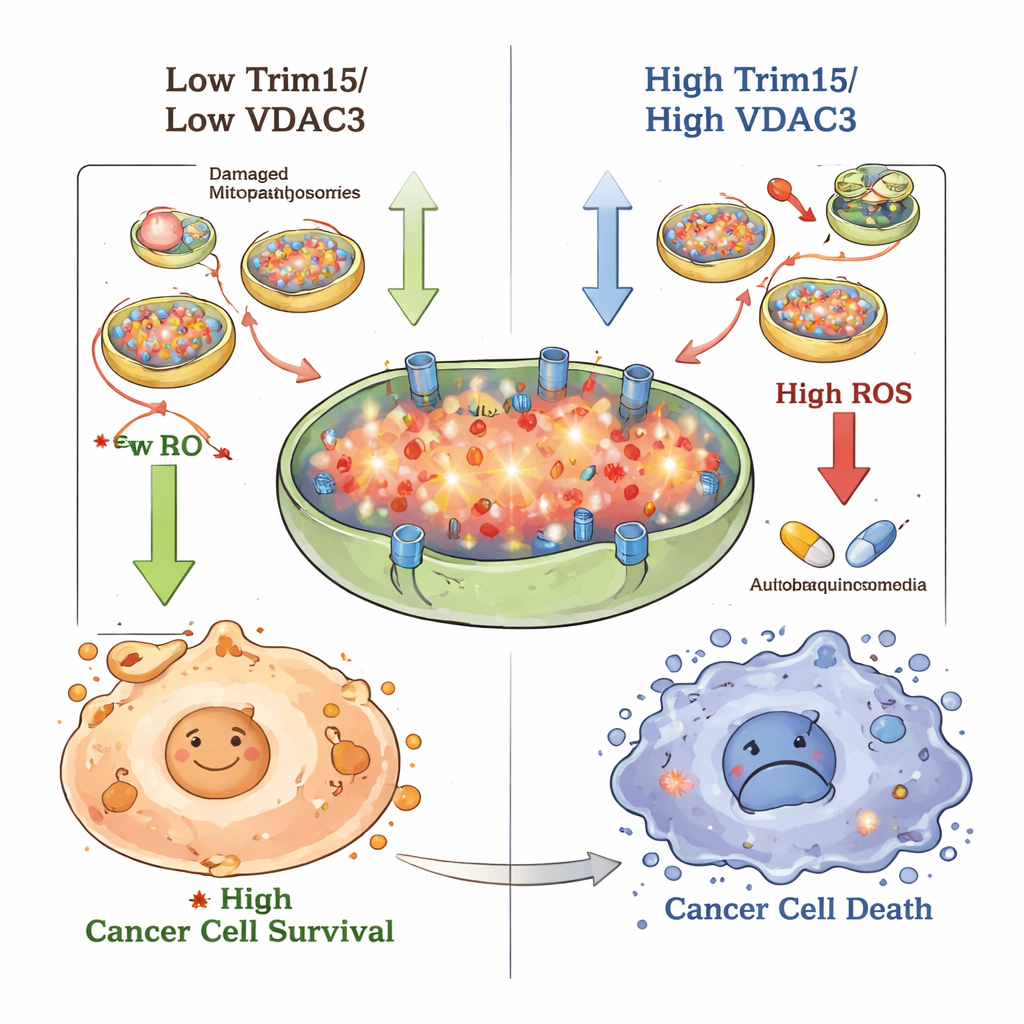
تتم مراقبة الميتوكوندريا باستمرار، وعند تلفها يمكن إزالتها عبر عملية تدوير متخصصة تسمى الميتوفاجي (الالتهام الذاتي للميتوكوندريا). أظهر الفريق أن VDAC3 يعمل عادةً كمكبح على هذا التدوير. عندما كان VDAC3 وفيراً، انخفضت مؤشرات الهضم الذاتي العام (الالتهام الذاتي) والميتوفاجي؛ وعندما انخفض VDAC3، تسارعت هذه العمليات، وابتلعت المزيد من الميتوكوندريا وتحطمت. أثر هذا التغير أيضاً على توازن أنواع الأكسجين التفاعلية (ROS) — جزيئات تفاعلية كيميائياً توصف غالباً كعادم خلوي. دفع وجود VDAC3 العالي مستويات ROS إلى الارتفاع، مما زاد من إجهاد الخلايا، بينما سمح انخفاض VDAC3 للخلايا بالتخلص من الميتوكوندريا التالفة، وخفض ROS، والبقاء بشكل أفضل تحت ظروف قاسية.
الكحول والإجهاد التأكسدي ومقاومة الأدوية
يُعد التعرض المزمن للكحول عامل خطر رئيسي لسرطان البلعوم السفلي، جزئياً لأن الإيثانول المركز يغمر بطانة الحلق مراراً وتكراراً. عندما عرض الباحثون الخلايا السرطانية للكحول في المختبر، انخفضت مستويات كل من Trim15 وVDAC3. بدا هذا الانخفاض كخطوة تكيفية من قبل الخلايا السرطانية: بتضعيف محور Trim15–VDAC3، عززت الميتوفاجي، وحافظت على مستويات ROS في نطاق أكثر أمناً، وتحمّلت الضرر الناتج عن الكحول. حدث استجابة مماثلة مع دواء العلاج الكيميائي القياسي 5‑فلوروأوراسيل (5‑FU): خفض العلاج Trim15 وVDAC3، مما يساعد على الأرجح خلايا الورم على تجنب الإجهاد التأكسدي القاتل ويساهم في المقاومة الكيميائية.
إيقاف الحماية الذاتية لتعزيز العلاج الكيميائي
سأل الفريق بعد ذلك ما إذا كان حجب الالتهام الذاتي قد يزيل هذه الحماية. استخدموا الكلوروكين، دواء قديم مضاد للملاريا يتداخل مع المراحل النهائية للهضم الذاتي الخلوي. في مزروعات الخلايا، أبطأ الكلوروكين بمفرده نمو حركة خلايا سرطان البلعوم السفلي وأزال ميزة النمو الناتجة عن فقدان VDAC3. في الفئران الحاملة لزرعات أورام بشرية، قلل كل من الكلوروكين و5‑FU من حجم الأورام، لكن الجمع بينهما عمل بأفضل شكل، خافضاً حجم ووزن الورم أكثر من أيّ دواء بمفرده من دون سمية ملحوظة مضافة. والأهم من ذلك، أن إجبار الخلايا على إنتاج كميات زائدة من Trim15 أو VDAC3 جعلها أكثر حساسية لـ5‑FU، جزئياً عن طريق رفع ROS إلى مستويات لم تعد الخلايا قادرة على التعامل معها.
ماذا يعني هذا لعلاجات المستقبل
بالنسبة للقارئ العادي، تُظهر الدراسة أن بعض خلايا سرطان البلعوم السفلي تنجو من العلاج الكيميائي عن طريق أن تصبح مُعيدي تدوير أفضل: تزيل بسرعة الميتوكوندريا التالفة وتحافظ على الإجهاد التأكسدي منخفضاً بما يكفي لتجنب الموت. يعمل Trim15 وVDAC3 معاً كقوة موازنة لهذا السلوك — عندما يكونان موجودين، يقيدان التدوير ويزيدان الإجهاد، مما يجعل الخلايا السرطانية أسهل في القتل. من خلال استهداف محور Trim15–VDAC3–الميتوفاجي، مثلاً بأدوية مثل الكلوروكين المضافة إلى العلاج الكيميائي القياسي، قد يتمكن الأطباء في المستقبل من جعل الأورام العنيدة في الحلق أكثر استجابة للعلاج وتحسين نتائج المرضى.
الاستشهاد: Wang, G., Shen, Y., Wang, L. et al. Trim15 stabilizes VDAC3 via ubiquitination to suppress autophagy and enhance chemosensitivity in hypopharyngeal squamous cell carcinoma. Cell Death Discov. 12, 88 (2026). https://doi.org/10.1038/s41420-026-02943-0
الكلمات المفتاحية: سرطان البلعوم السفلي, الالتهام الذاتي, الميتوكوندريا, مقاومة العلاج الكيميائي, الكلوروكين