Clear Sky Science · ar
روتليرين يحفّز تحلّلًا مزدوجًا لـ SLC7A11 وGPX4 ليُحدث الفيروسبْتوس ويسهّل الاستجابة للعلاج الكيميائي في سرطان الكبد الكبدي
لماذا يهم هذا المركب الطبيعي لسرطان الكبد
سرطان الخلايا الكبدية، الشكل الأكثر شيوعًا لسرطان الكبد الأولي، يتم تشخيصه غالبًا في مراحل متأخرة ويظل صعب المعالجة. تستكشف هذه الدراسة ما إذا كان جزيء مشتق من نبات يُدعى روتليرين، والمعروف منذ زمن بتأثيراته المضادة للسرطان على نطاق واسع، يمكن توظيفه لتحفيز شكل أحدث من موت الخلايا يُسمى الفيروبتوس في خلايا سرطان الكبد. من خلال فهم آلية عمل روتليرين على المستوى الجزيئي، يأمل الباحثون في فتح مسارات جديدة لعلاجات أكثر فعالية وأقل عرضة للمقاومة.
طريقة جديدة لقتل الخلايا السرطانية
تدفع الأدوية المضادة للسرطان التقليدية عادةً الخلايا الورمية نحو برامج موت معروفة مثل الاستماتة. الفيروبتوس مختلف: إنه عملية تعتمد على الحديد يدفعها تراكم الدهون السامة في أغشية الخلايا. خلايا سرطان الكبد عرضة بشكل خاص لهذا النوع من الضرر لأنها تعتمد بشدة على نظم مضادة للأكسدة للحفاظ على هذه السموم الدهنية تحت السيطرة. سأل الفريق ما إذا كان روتليرين يمكنه تخريب تلك الدفاعات وبذلك إجبار خلايا سرطان الكبد على الخضوع للفيروبتوس.
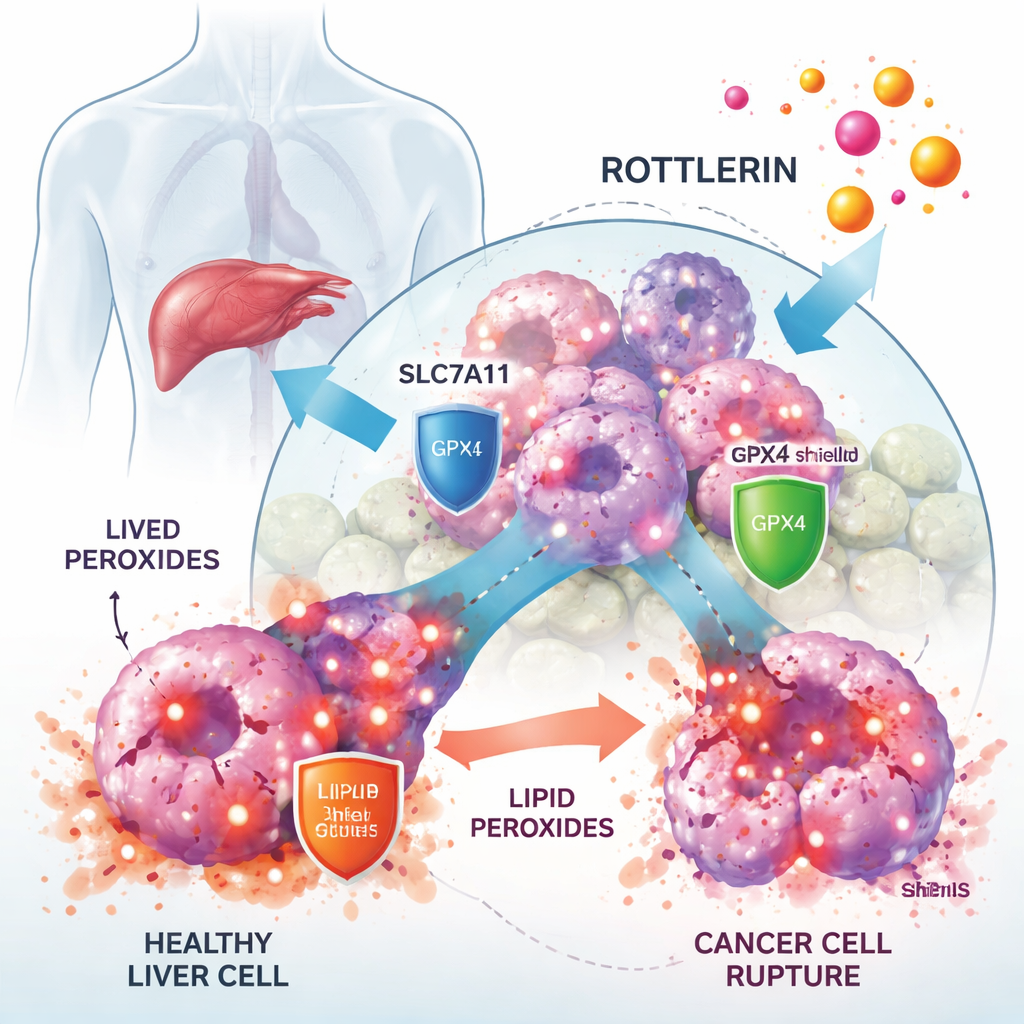
كيف يبطئ روتليرين نمو الورم
بالعمل مع خطوط خلايا سرطان الكبد البشرية، أظهر الباحثون أن روتليرين قلل بشدة من نمو الخلايا السرطانية عند جرعات منخفضة بمقياس الميكرومولار، بينما تأثرت الخلايا الطبيعية المرتبطة بالكبد أقل. عندما أضافوا مُثبِطًا محددًا للفيروبتوس يسمى فيرواستاتين‑1، تم إنقاذ جزء كبير من موت الخلايا الناجم عن روتليرين، مما يشير بقوة إلى أن الفيروبتوس كان النمط الرئيسي للقتل. دعمت المجهرية والاختبارات الكيميائية الحيوية ذلك: حيث تراكمت في الخلايا المعالجة بروتليرين مستويات مرتفعة من البيروكسيدات الدهنية، وظهرت ميتوكوندريا متغيرة، وسجلت الخلايا انخفاضًا في جزيء مضاد الأكسدة الغلوتاثيون، وكلها سمات مميزة للفيروبتوس.
تحييد دروع الخلايا المضادة للأكسدة
تنجو خلايا سرطان الكبد بالاعتماد على محور دفاعي حاسم يتألف من الناقل SLC7A11 والإنزيم GPX4. يستورد SLC7A11 السيستين، وهو لبنة بناء للغلوتاثيون، بينما يستخدم GPX4 الغلوتاثيون لتحييد البيروكسيدات الدهنية قبل أن تضر الأغشية. وجدت الدراسة أن روتليرين تسبب بانخفاض مستويي بروتين SLC7A11 وGPX4 مع مرور الوقت. لم يكن ذلك لأن الخلايا توقفت عن صنعهما، بل لأن البروتينات وُسِّمت بعلامات صغيرة «دمرني» (اليوبيكويتين) وأُرسِلت إلى آلية تحطيم البروتينات في الخلية، المِرْقِم (بروتيازوم). عكس حجب المِرْقِم هذا الفقدان، وعندما زاد الباحثون اصطناعيًا من مستويات SLC7A11 أو GPX4 في الخلايا حماها ذلك جزئيًا من روتليرين. معًا، تُظهر هذه النتائج أن روتليرين يعمل كمحلل مزدوج لدفاعين مركزيين ضد الفيروبتوس.
تعزيز أدوية سرطان الكبد الحالية
يتلقى العديد من المرضى المصابين بسرطان الكبد المتقدم دواء السورافينيب، وهو دواء قياسي من الخط الأول يمكنه بدوره تحفيز الفيروبتوس، لكن المقاومة تحد غالبًا من فائدته. اختبر المؤلفون ما إذا كانت جرعات منخفضة من روتليرين، التي تكون ضعيفة بمفردها، يمكن أن تجعل الخلايا الورمية أكثر حساسية للأدوية المحفزة للفيروبتوس مثل السورافينيب وRSL3. في مزروعات الخلايا، أدت مزيجة روتليرين بجرعة منخفضة مع أي من الدوائين إلى زيادة كبيرة في موت الخلايا السرطانية وتحول في منحنيات الجرعة‑الاستجابة، مما يدل على زيادة الفعالية. ومن المهم أن أثر الحساسية هذا استمر حتى عندما تم تقليل البروتين الهدف الكلاسيكي لروتليرين PKCδ وراثيًا، مما يظهر أن الفعل الرئيسي لم يكن عبر هذه الكيناز بل عبر تحلّل SLC7A11 وGPX4. في نماذج الفئران الحاملة لأورام كبد بشرية، أدى العلاج المشترك بروتليرين والسورافينيب إلى إبطاء نمو الورم أكثر من السورافينيب وحده وخفض مستويات SLC7A11 وGPX4 في الأورام بشكل أكبر.
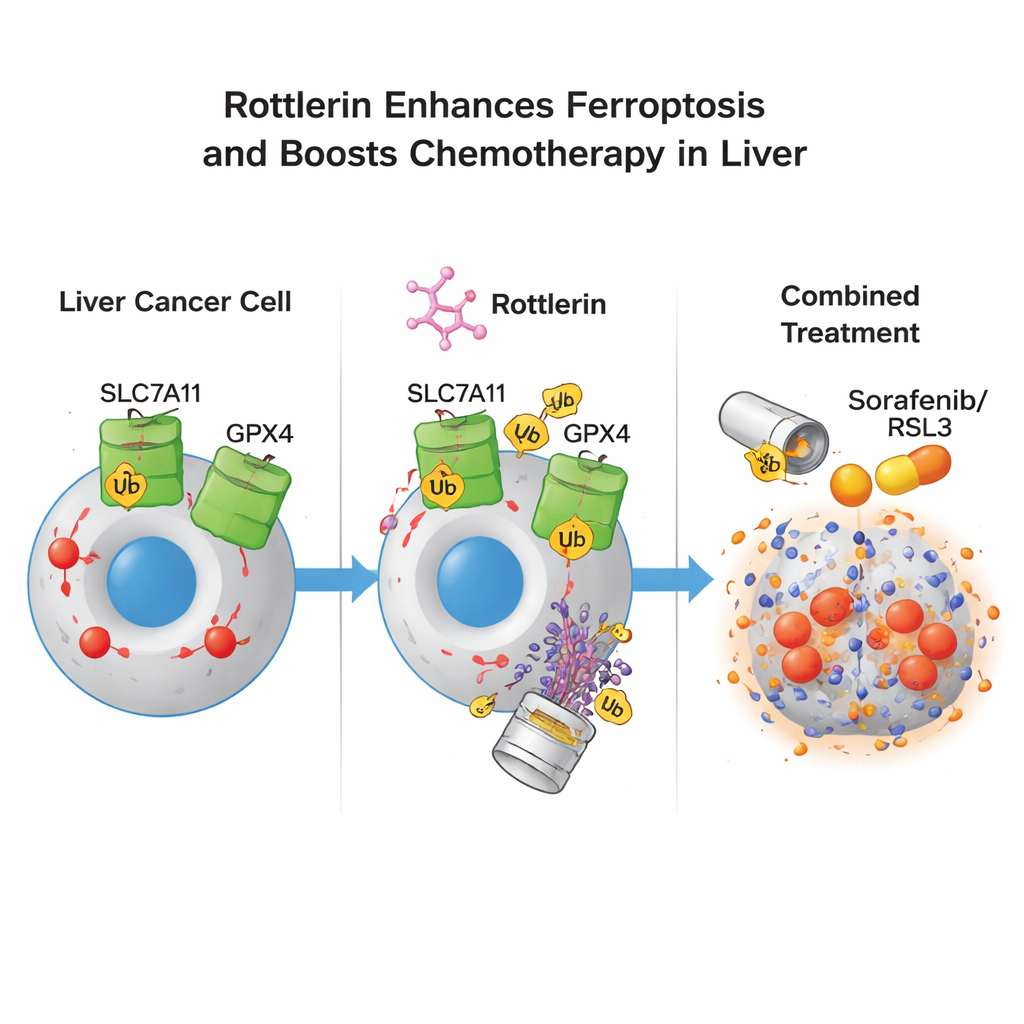
ماذا قد يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الرسالة هي أن روتليرين يعمل مثل "مفتاح ذو قفلين" لخلايا سرطان الكبد: يزيل في الوقت نفسه قفلين حاسمين—SLC7A11 وGPX4—الذين عادةً ما يحميان الخلايا من موجة قاتلة من الأكسدة الدهنية. بمجرد إزالة تلك الأقفال، تصبح الخلايا السرطانية أكثر عرضة للخضوع للفيروبتوس، خاصة عند اقترانها بأدوية موجودة تدفعها في ذلك الاتجاه. في حين أن هناك حاجة لمزيد من العمل قبل أن يُستخدم روتليرين أو مركبات مرتبطة به في المرضى، فإن استراتيجية التحلل المزدوج هذه تقدم وسيلة واعدة للتغلب على الدفاعات التكيفية التي غالبًا ما تجعل أورام الكبد صعبة العلاج.
الاستشهاد: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
الكلمات المفتاحية: سرطان الكبد, الفيروبتوس, روتليرين, SLC7A11, GPX4