Clear Sky Science · ar
استهداف نقاط الضعف الأيضية: منبه REV-ERB SR9009 يعزز فعالية السورافينيب في سرطان الكبد
لماذا يهم تجويع خلايا السرطان من الطاقة
يعد سرطان الكبد من أخطر أنواع السرطان على مستوى العالم، ولا يزال العديد من المرضى المصابين بمرض متقدم يعتمدون على دواء قديم يُدعى السورافينيب. على الرغم من أن السورافينيب يمكن أن يبطئ نمو الورم، إلا أن خلايا السرطان غالبًا ما تتأقلم وتصبح مقاومة، مما يحد من مدة بقاء المرضى. تستكشف هذه الدراسة نهجًا جديدًا لجعل السورافينيب يعمل بشكل أفضل عن طريق مهاجمة كيفية حصول خلايا سرطان الكبد على الوقود، مما يقدّم لمحة عن علاجات مستقبلية قد تضرب الأورام بشدة أكبر من دون إضافة آثار جانبية خطيرة.
كيف تقصر أدوية سرطان الكبد الحالية
كان السورافينيب لفترة طويلة علاجًا أساسيًا للمرضى الذين لا يمكن استئصال أورام كبدهم جراحيًا. تساعد بعض المناعات الجديدة الآن بعض الأشخاص على العيش لفترة أطول، لكن العديد من المرضى إما لا يستوفون شروط هذه العلاجات أو لا يستجيبون لها. لهؤلاء المرضى يبقى السورافينيب مهمًا، ومع ذلك تظهر المقاومة غالبًا خلال أشهر. طرح الباحثون سؤالًا بسيطًا لكنه قويًا: ما التغيرات داخل خلايا سرطان الكبد التي تسمح لها بالهروب من تأثيرات السورافينيب، وهل يمكن تحويل هذه التغيرات إلى نقاط ضعف علاجية جديدة؟
خلايا السرطان ترفع إنتاج مصانع الطاقة لديها
للبحث عن إجابات، قارن الفريق خلايا سرطان الكبد التي لا تزال تستجيب للسورافينيب مع خلايا تعلمت البقاء على قيد الحياة في وجود الدواء. باستخدام تسلسل RNA واسع النطاق، اكتشفوا أن الخلايا المقاومة زادت بشدة من نشاط الجينات المشاركة في الفسفرة التأكسدية الميتوكوندرية — وهي الطريقة الرئيسية التي تولد بها الخلايا الطاقة في "مصانع الطاقة" الصغيرة، الميتوكوندريا. كما ارتفعت أيضًا جينات حماية الإجهاد الأخرى، بما في ذلك تلك المرتبطة بالتعامل مع جزيء يُدعى الهيم. مجتمعة، اقترحت هذه التغيرات أن خلايا السرطان المقاومة تتكيف مع السورافينيب عن طريق إعادة توصيل طرق إنتاج الطاقة وأنظمة حماية الإجهاد بدلًا من تجاهل الأهداف الأصلية للدواء.
دواء ثانٍ يقطع الكهرباء عن الخلايا
توجه الباحثون بعدها إلى SR9009، مركب تجريبي صمم أصلاً للتأثير على بروتينات متعلقة بالساعة البيولوجية تُدعى REV-ERBs والتي تساعد في تنظيم الأيض. يعرف عن SR9009 أنه يتداخل مع نشاط الميتوكوندريا ويكون أكثر ضررًا للخلايا الورمية مقارنة بالخلايا الطبيعية. في خلايا سرطان الكبد لكل من الفأر والإنسان، قلّص الجمع بين SR9009 والسورافينيب بحدة بقاء الخلايا مقارنةً بكل دواء بمفرده. القطعة الدوائيةان خفضتا إنتاج الطاقة الميتوكوندرية تقريبًا إلى الصفر، مما أجبر الخلايا على الاعتماد على مسارات احتراق السكر الاحتياطية التي لم تستطع التعويض الكامل. أظهرت اختبارات المختبر انخفاضات حادة في ATP الخلوية — عملة الطاقة العالمية — وتكوّن مستعمرات أقل من خلايا السرطان الناجية. والأهم من ذلك، أن الخلايا الليفية الطبيعية والخلايا الكبدية غير السرطانية تأثرت بدرجة أقل بكثير، مما يوحي بأن الاستراتيجية قد تستهدف النسيج الورمي بشكل انتقائي.
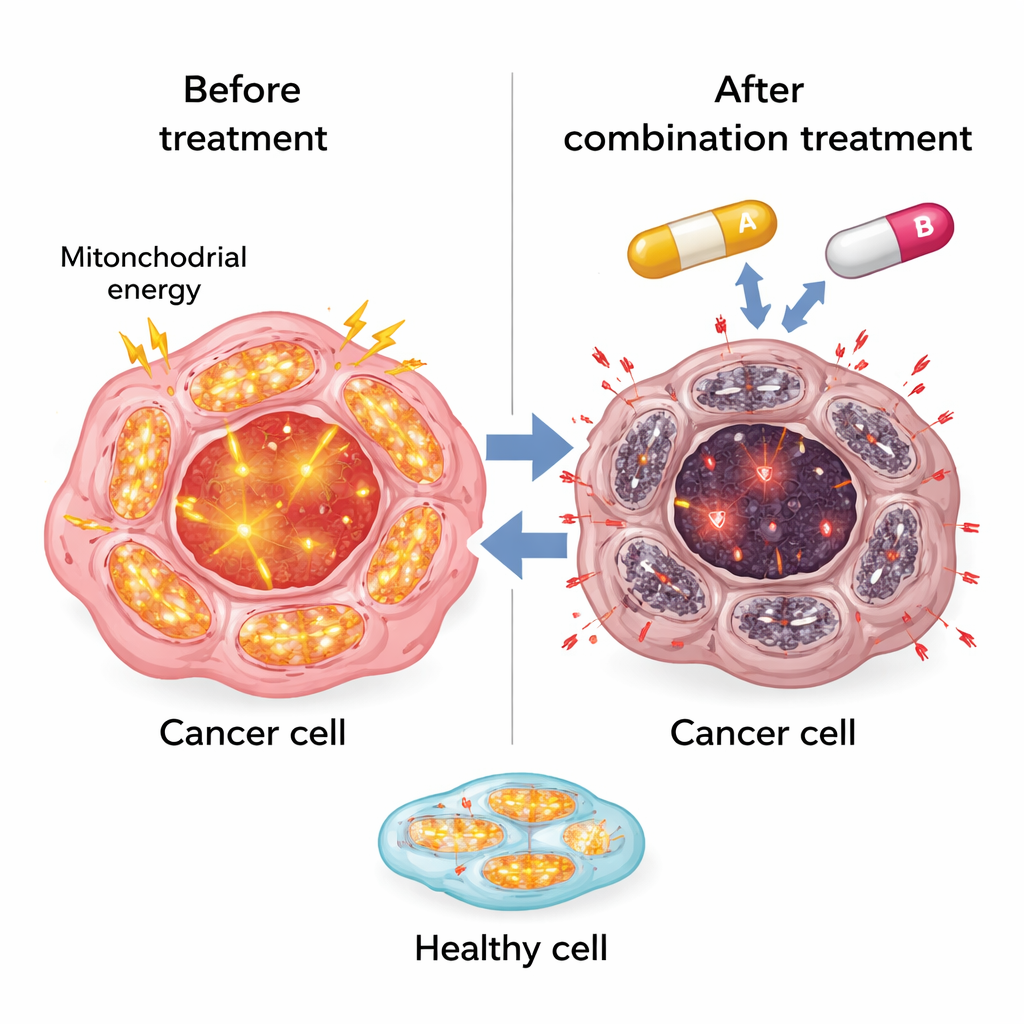
اختلال توازن الهيم وإثارة إجهاد سام
كشفت الدراسة أيضًا عن ضعف ثانٍ: كيفية إدارة الخلايا المقاومة للهيم، وهو جزيء صغير يحتوي على الحديد وضروري للعديد من الإنزيمات، بما في ذلك تلك الموجودة في الميتوكوندريا. فعّلت خلايا سرطان الكبد المقاومة مستويات عالية من HO-1، وهو إنزيم يحلل الهيم الحر، وزادت الفيريتين الذي يخزن الحديد الناتج بأمان. بدا أن هذا يحميها من أضرار متعلقة بالهيم.غيّر SR9009 هذا التوازن. في الخلايا المقاومة، رفع SR9009 مستويات الهيم الحر وزاد مؤشرات الإجهاد التأكسدي مثل الجذور الحرة والتلف الدهني، لا سيما عند الجمع معه مع السورافينيب. وفي الوقت نفسه انخفضت بروتينات الميتوكوندريا، مما يعزز الفكرة أن إغراق مصانع طاقة الخلية وأنظمة حماية الإجهاد يدفع خلايا السرطان إلى نقطة اللاعودة.
مراقبة أقوى للأورام في النماذج الحيوانية
لاختبار ما إذا كانت هذه التأثيرات تمتد إلى ما بعد أطباق الخلايا، جرب الفريق الزوج الدوائي في الفئران. في حيوانات تحمل أورام كبدية عادية ومقاومة للسورافينيب معًا، لم تتقلص الأورام المقاومة إلا عند استخدام مزيج السورافينيب مع SR9009. في نموذج منفصل حيث نشأت سرطانات الكبد تلقائيًا بعد تعرض كيميائي مسبب للسرطان، أدى إضافة SR9009 إلى جرعة مخفضة من السورافينيب إلى تقلص الأورام في أكثر من 90٪ من العقيدات، بينما استمرت الأورام في الفئران المعالجة بالسورافينيب وحده بالنمو إلى حد كبير. ولافت أن التركيبة لم تزيد السمية العامة: حافظت الفئران على وزن مستقر، وبقيت تعداد الخلايا الدموية طبيعيًا، وكانت مؤشرات إصابة الكبد أقل عند إضافة SR9009، مما يشير إلى تأثير وقائي على نسيج الكبد السليم.
ماذا قد يعني هذا للمرضى
بالنسبة للقارئ العام، الرسالة الأساسية هي أن هذا العمل يوضح طريقة ذكية لجعل دواء قائم لسرطان الكبد أكثر فعالية عن طريق استغلال كيفية تأقلم الأورام. خلايا السرطان المقاومة للبقاء على قيد الحياة تفعل ذلك جزئيًا بزيادة مصانع طاقتها وأنظمة التحكم في الإجهاد. يقضي SR9009 على هذه الدعائم، تاركًا خلايا السرطان مجوعة من الطاقة ومثقلة بمنتجات سامة، مع حفظ الخلايا السليمة إلى حد كبير. على الرغم من أن SR9009 نفسه لم يُعتمد بعد كدواء وهذه النتائج مأخوذة من نماذج ما قبل السريرية، تقدم الدراسة خارطة طريق: إقران الأدوية المعيارية مع عوامل تستهدف أيض الورم قد يتجاوز المقاومة ويسمح بجرعات أقل وأكثر أمانًا. على المدى الطويل، قد تمنح مثل هذه الاستراتيجيات المركبة مرضى سرطان الكبد المتقدم وقتًا أفضل وجودة حياة أعلى.
الاستشهاد: Sabbioni, S., Guerriero, P., Shankaraiah, R.C. et al. Targeting metabolic vulnerabilities: REV-ERB agonist SR9009 potentiates sorafenib efficacy in liver cancer. Cell Death Discov. 12, 86 (2026). https://doi.org/10.1038/s41420-026-02940-3
الكلمات المفتاحية: سرطان الكبد, مقاومة الأدوية, أيض السرطان, العلاج التركيبي, الميتوكوندريا