Clear Sky Science · ar
فقدان DIAPH3 يسرّع تكون الورم الدبقي في الفئران
لماذا تهم هذه الدراسة الدماغية
الورم الدبقي الخبيث (غليوبلاستوما) يعد من أخطر أنواع سرطانات الدماغ، وعلى الرغم من الجراحة والإشعاع والعلاج الكيميائي، يعيش معظم المرضى لفترة لا تتجاوز السنة تقريبًا. تطرح هذه الدراسة سؤالًا أساسيًا لكن حاسمًا: ما التغيرات المبكرة داخل خلايا الدماغ التي تدفعها نحو أن تصبح مثل هذه الأورام العدوانية، ولماذا يصعب القضاء على هذه الأورام بالإشعاع؟ من خلال تتبُّع بروتين بنيوي واحد في خلايا دماغ الفئران، يكشف الباحثون كيف يؤدي فقدانه إلى زعزعة استقرار الكروموسومات، وتسريع ظهور الورم، ومساعدة الخلايا الشبيهة بالجذع السرطانية على تحمل الإشعاع الذي من المفترض أن يدمرها.
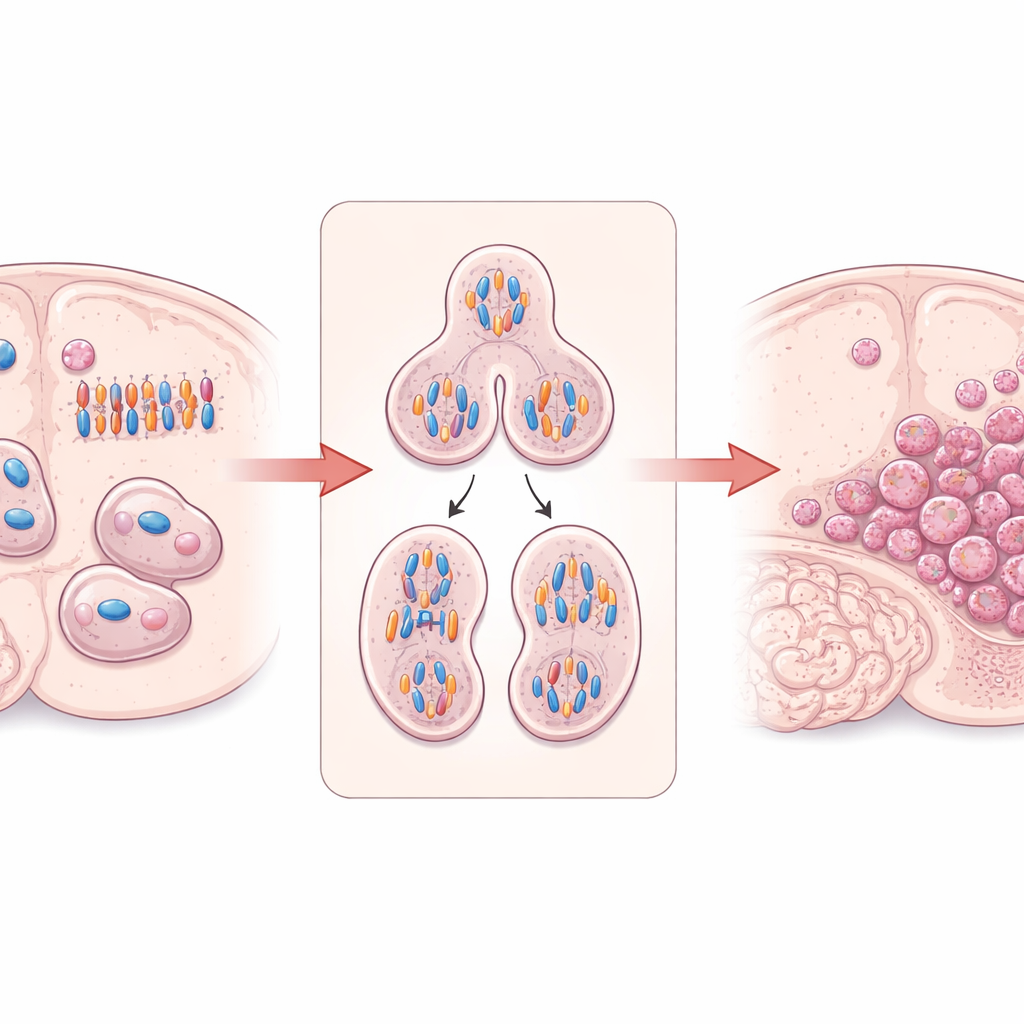
"بنّاء" خلوي يحافظ على انتظام الانقسام
تركز الدراسة على DIAPH3، وهو بروتين يساعد على بناء وتنظيم الهيكل الداخلي للخلية المكون من خيوط الأكتين والأنابيب الدقيقة. في خلايا جذع الدماغ المنقسمة، يعد DIAPH3 ضروريًا لتشكيل المغزل الخلوي السليم—الهيكل الذي يفصل الكروموسومات المكررة—وللتمايز الخلوي إلى خليتين. أظهرت أبحاث سابقة أنه عند غياب DIAPH3 في أدمغة الفئران النامية، تتعامل الخلايا المنقسمة غالبًا بشكل غير صحيح مع الكروموسومات، مما يؤدي إلى أعداد كروموسومات غير طبيعية (عدم التناسق الصبغي)، وتوقف دورة الخلية، وموت الخلايا. ومن اللافت أن منطقة صغيرة من كروموسوم الإنسان 13 التي تحتوي على جين DIAPH3 تُحذف بشكل متكرر في الأورام الدبقية، وربطت مستويات DIAPH3 الأعلى ببقاء أفضل لدى بعض المرضى، ما يوحي بأن هذا البروتين قد يعمل ككابح للأورام في الدماغ.
هندسة أدمغة الفئران لنمو أورام
لاختبار ما إذا كان فقدان DIAPH3 يعزز فعلا السرطان الدماغي، أنشأ الفريق فئرانًا يمكن فيها حذف جينين انتقائيًا في الخلايا الجذعية المكوِّنة للقشرة: Diaph3 وTrp53، الأخير يشفر الحارس المعروف للجينوم، p53. لم تُظهر الفئران التي افتقرت إلى Diaph3 فقط في هذه المنطقة أورامًا حتى بعد عامين، ما يوحي بأن p53 يظل قادرًا على إزالة الخلايا الشاذة بشدة. بالمقابل، تكونت لدى الفئران التي افتقرت إلى Trp53 وحده، أو كل من Trp53 وDiaph3، أورام دبقية منتشرة عالية الدرجة شبيهة جدًا بالمرض البشري تحت المجهر. باستخدام فحوصات رنين مغناطيسي متكررة ذات مجال فائق الارتفاع، أظهر الباحثون أن الحيوانات التي تفتقر إلى الجينين طوّرت أورامًا قابلة للكشف في وقت أبكر، وبمنتصف العمر كانت أكثر عرضة لامتلاك أورام دبقية كبيرة، خاصة في البُصيلات الشمية، مقارنة بالفئران التي تفتقر إلى Trp53 فقط. كان معدل نمو الورم، بعد بدايته، مشابهًا بين المجموعتين—ما تغير هو سرعة ظهور الأورام.
فوضى كروموسومية ونشاط جيني معاد توصيله
للتحقيق في سبب تسريع فقدان DIAPH3 لبدء الورم، فحص الفريق نشاط الجينات في البصيلات الشمية لدى الفئران الصغيرة قبل أن تكون أي أورام مرئية. في الحيوانات التي تفتقر إلى كل من Diaph3 وTrp53، تم التعبير عن 126 جينًا بمستويات مختلفة مقارنة بالطفرات التي تعاني من Trp53 فقط، وكان لنحو نصف هذه الجينات صلات سابقة بالسرطان. تركزت العديد من التغيرات في مسارات تحفز نمو الخلايا وهجرتها وتكوين الأوعية الدموية، بما في ذلك إشارات VEGF وMAPK وRAS وRap1 وcAMP، فضلاً عن شبكات مستقبلات مقترنة ببروتين G. وقد اقترح هذا المشهد الجزيئي المعدَّل أن الخلايا تتجه نحو حالة شبيهة بالسرطان مبكرًا. وكشفت تحليلات النسخ الكامل للجينوم لنسخ العدد عن أن نقص DIAPH3 لم يزد بشكل كبير التغيرات الـDNA البؤرية الصغيرة بل عزز بدلاً من ذلك المكاسب والخسائر الواسعة المدى على مستوى الكروموسومات بأكملها—وهو نمط عدم تناسق صبغي متوقع من فصل كروموسومات معطوب.
أضرار DNA مدمجة وخلايا جذعية للورم أكثر صلابة
حملت الخلايا الورمية ناقصة التناسق الصبغي مستويات أعلى من تلف الـDNA الداخلي، تم اكتشافه عبر ارتفاع مؤشرات كسر الـDNA مثل γ‑H2AX المبعثرة عبر نوى الخلايا. ومع ذلك، استمرت هذه الأورام في النمو، ما يوحي بأنها اكتسبت طرقًا لتحمّل مثل هذا الإجهاد. بمقارنة التعبير الجيني في الأورام الراسخة، وجد الباحثون مئات الجينات المتغيرة بفقدان DIAPH3، بما في ذلك تضخيم ملحوظ وإنتاج مفرط لمستقبل عامل النمو FGFR2 في العديد من الأورام ذات الطفرة المزدوجة. من المعروف أن FGFR2 يعزز آليات إصلاح الـDNA في خلايا الغليوبلاستوما، وربط تفعيله بالمقاومة للإشعاع. عزل الفريق خلايا شبيهة بالجذع من أورام الفئران واختبر استجابتها لجرعة إشعاع مؤينة ذات صلة سريريًا. قبل العلاج، كانت نسبة الخلايا الشبيهة بالجذع نشطة متشابهة في كلا النمطين الجينيين، لكن بعد التعرض للإشعاع، احتفظت المستنبتات من الأورام ناقصة DIAPH3 بما يقرب من ضعف عدد الخلايا الشبيهة بالجذع النشطة مقارنة بتلك من أورام Trp53 فقط، مما يدل على مقاومة إشعاعية أكبر.
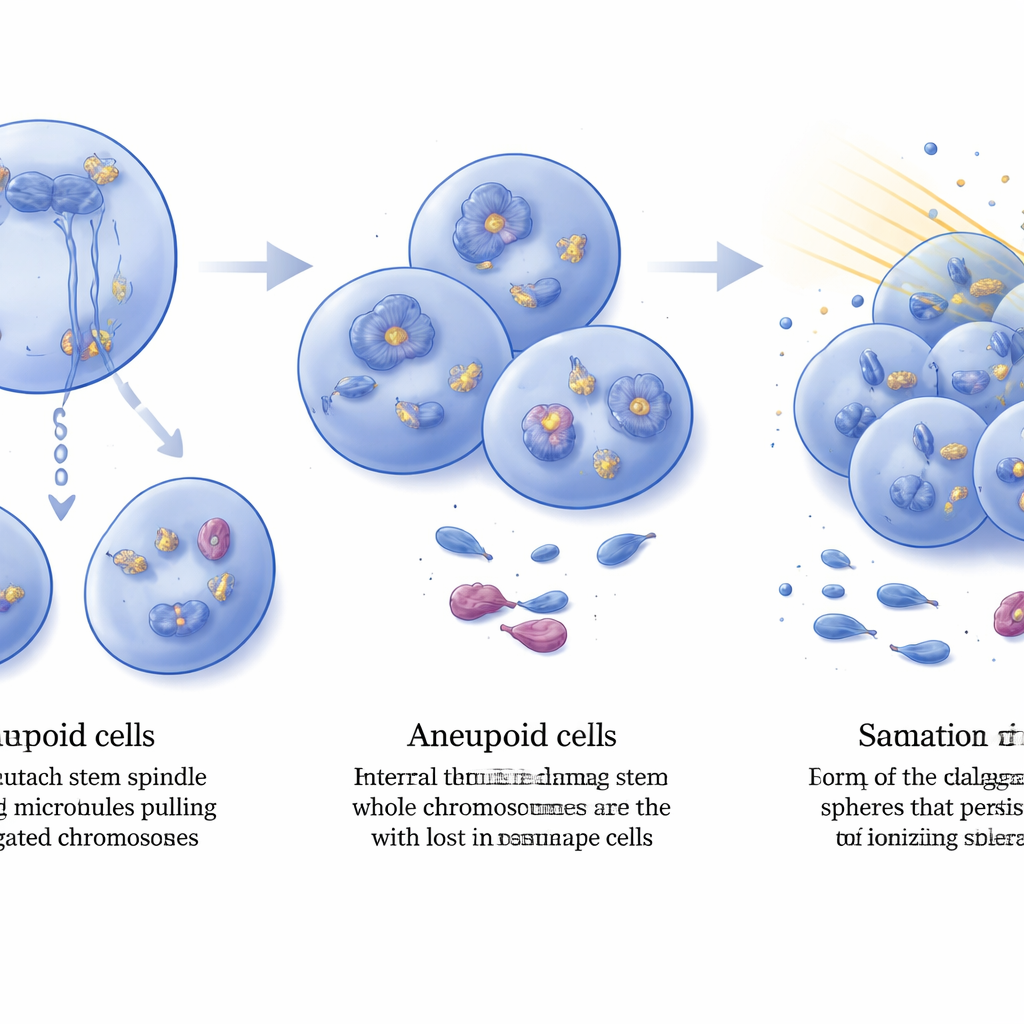
ماذا يعني هذا لسرطان الدماغ
تجتمع النتائج لتصوّر DIAPH3 كحارس يساعد خلايا جذع الدماغ على الانقسام بعدد كروموسومات صحيح. عندما يغيب كل من DIAPH3 وp53، يصبح الانقسام الخلوي عرضة للأخطاء، تُفقَد أو تُكسب كروموسومات كاملة، ويتراكم تلف الـDNA. وبدل أن تموت هذه الخلايا، تتكيف بعضُها عبر تضخيم عوامل مرتبطة بالإصلاح مثل FGFR2، فتتحول إلى أورام دبقية عالية الدرجة غير متناسقة الصبغيات وخلاياها الشبيهة بالجذع أكثر مقاومة للإشعاع بشكل غير عادي. وعلى الرغم من أن نماذج الفئران لا تلتقط كل خصائص الغليوبلاستوما البشرية، تدعم هذه النتائج دور DIAPH3 كمؤشر محتمل للتكهن وكموقع مهم في شبكة العمليات التي تتحكم في بدء الورم، استقرار الجينوم، واستجابة العلاج—مما يفتح دروبًا علاجية قد تجعل هذا السرطان الدماغي المروع أكثر تعرضًا للعلاجات الحالية في المستقبل.
الاستشهاد: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
الكلمات المفتاحية: ورم دماغي نجمي دخني, عدم استقرار كروموسومي, خلايا جذعية لأورام الدماغ, مقاومة الإشعاع, جينات كابحة للأورام