Clear Sky Science · ar
خلايا الورم الأرومي الدبقي التي تفلت من موت الخلايا الناجم عن العلاج الكيميائي الإشعاعي تُظهر برنامجًا تحليليًا مزدوج المسار للجلوكوز
لماذا تهم هذه الدراسة لسرطان الدماغ
الورم الأرومي الدبقي من أخطر سرطانات الدماغ لدى البالغين، وغالبًا ما يعود للنمو بعد الجراحة والعلاج الكيميائي والإشعاعي. تطرح هذه الدراسة سؤالًا حاسمًا: ما الذي يميّز مجموعة الخلايا القليلة داخل الورم التي تنجو من العلاج وتعيد إشعال المرض لاحقًا؟ من خلال تتبُّع كيفية تعامل هذه الخلايا مع السكر عبر الزمن، يكشف الباحثون عن استراتيجية بقاء خفية قد تفسر سبب إخفاق العلاجات الحالية في كثير من الأحيان—وتقترح سبلًا جديدة لقطع شريان حياة الورم.
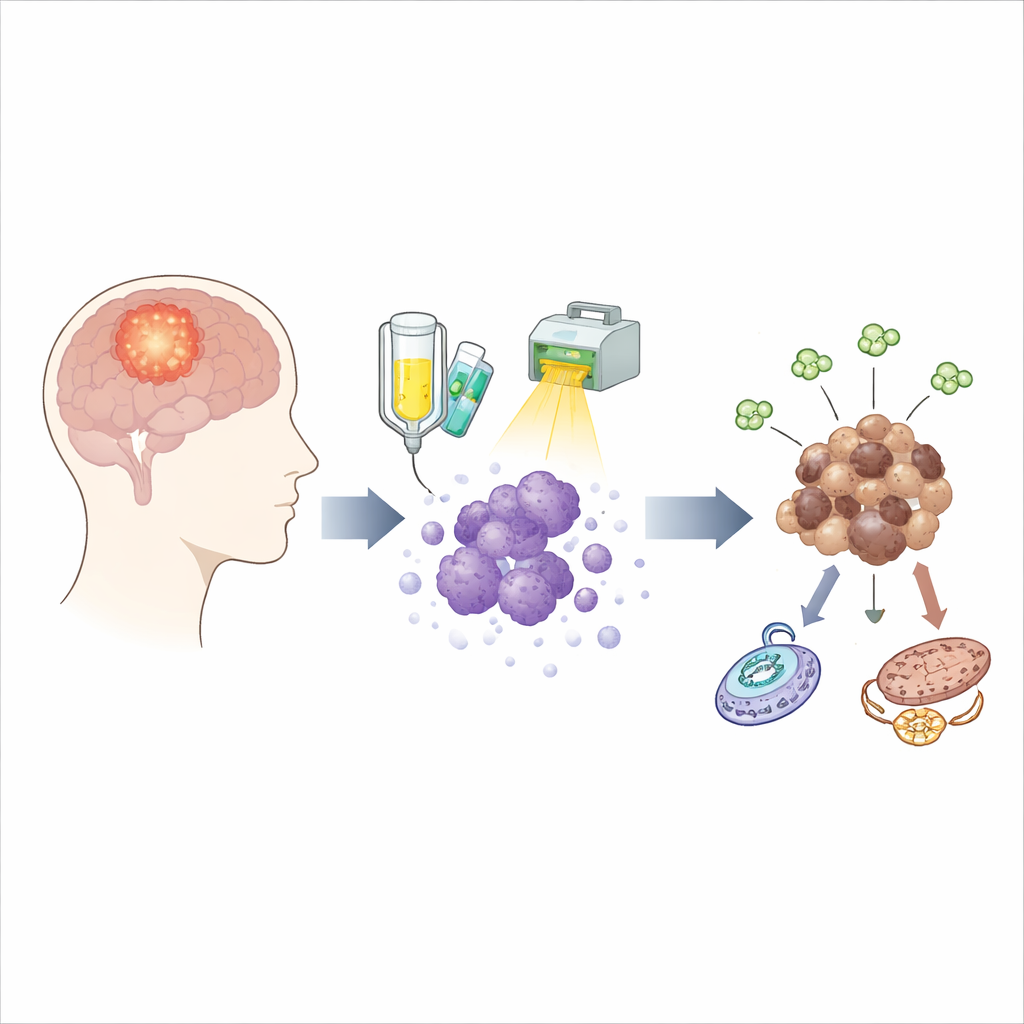
الناجون الخفيون بعد العلاج
الإدارة القياسية للورم الأرومي الدبقي تجمع بين دواء يُدعى تيموزولوميد والإشعاع. بينما تـُقتل هذه التركيبة غالبية خلايا الورم، يبقى نسبة عنيدة تنجو وقد تُنشئ ورمًا جديدًا بعد أشهر. لملاحظة هؤلاء الناجين أثناء العملية، استخدم الفريق خلايا ورمية مأخوذة مباشرة من عشرة مرضى مختلفين وعرضها لجدول علاجي مُحاكٍ بعناية لما يتلقاه المرضى في العيادة. أخذوا عينات للخلايا الحية في عدة نقاط أثناء العلاج وبعده، ودرسوا أيضًا أورامًا مطابقة نمت في فئران، مما أتاح لهم متابعة كيفية تغير الناجين عبر الزمن بدلًا من مقارنة الأورام قبل الانتكاس وبعده فقط.
كيف تغير خلايا الورم طريقة استخدامها للسكر
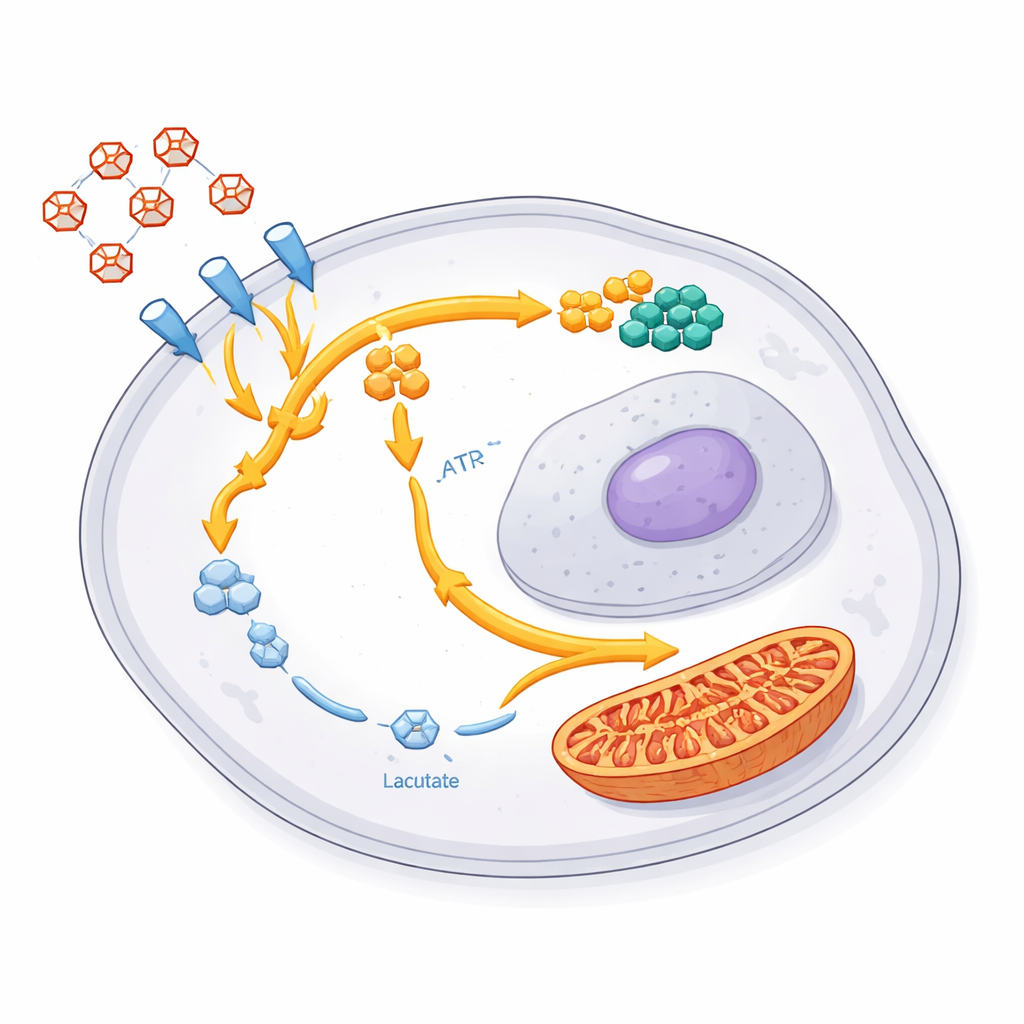
ينفق نسيج الدماغ حصة ملحوظة من سكر الجسم، وخلايا الورم الأرومي الدبقي جائعة بشكل خاص لهذا الوقود. وجد الباحثون أنه مع تقدم العلاج، كانت الخلايا الناجية تمتص المزيد من الجلوكوز من محيطها. لكن، وبشكل مفاجئ، لم تقم هذه الخلايا بحرق هذا الوقود الإضافي بشكل أسرع فحسب. بدلًا من ذلك، خفّضت إنتاج اللاكتات، المنتج الشائع لنهاية تكسير السكر السريع في السرطان. أظهرت قياسات البروتينات الرئيسية نمطًا متشظيًا لافتًا: المكونات التي تُدخل السكر إلى الخلية وتبدأ في تفكيكه ارتفعت، بينما تلك التي تتولى المراحل اللاحقة وتصنع اللاكتات انخفضت. يعني هذا البرنامج «المتفرع» أن السكر يدخل ويبدأ في المعالجة، لكن المسار المعتاد نحو اللاكتات مغلق جزئيًا.
تحويل الوقود إلى لبنات بناء ومحطات طاقة
إلى أين يذهب السكر المحوَّل؟ باستخدام جلوكوز موسوم خصيصًا وقياسات متقدمة للقمائح الأيضية، أظهر الفريق أن الخلايا الناجية تحوِّل قدرًا كبيرًا من هذا الكربون إلى وجهتين رئيسيتين. الأولى هي مسار جانبي يُدعى مسار فوسفات البنتوز، الذي يولد المواد الخام اللازمة لصُنع لبنات بناء الـDNA والـRNA. في هذه الخلايا، ارتفعت العديد من مكونات النيوكليوتيدات والجينات المرتبطة بها، مما يشير إلى دفع قوي نحو إعادة البناء والاستعداد للنمو المتجدد. الوجهة الثانية هي محطات الطاقة داخل الخلية، وهي الميتوكوندريا. زادت إنزيمات دورة الطاقة الميتوكوندرية، وأظهرت أعمال سابقة من نفس المجموعة زيادة في دخول الوقود المستمد من السكر إلى هذه البنى. يكشف هذا معًا عن إعادة توصيل منسقة: تقليل التخمُّر المهدر إلى لاكتات، وزيادة الاستثمار في الإصلاح ومواد النمو وإنتاج طاقة مرن.
كتاب استراتيجيات البقاء المشترك بين الأورام وفي الحيوانات
تختلف أورام الورم الأرومي الدبقي اختلافًا كبيرًا من مريض لآخر، مما يعوق غالبًا العلاجات الموحدة. على الرغم من هذا التنوع، أظهر كل نموذجٍ من النماذج العشرة المستمدة من المرضى نفس التحول الأساسي بعد العلاج الكيميائي الإشعاعي: زيادة في خطوات معالجة السكر المبكرة، نقصان في الخطوات المتأخرة وإنتاج اللاكتات، ونشاط متزايد للميتوكوندريا. والأهم أن نفس البصمة ظهرت في أورام دماغية في الفئران نمت من خلايا المرضى وعولجت بنُسخ معدلة من العلاج القياسي. الأورام المتكررة في هذه الحيوانات احتفظت بالبرنامج السكري المتغير، مما يشير إلى أن هذا ليس تأثيرًا عابرًا بل سمة مستقرة للخلايا التي تنجو من العلاج وتعيد بناء السرطان.
ماذا يعني هذا للعلاج المستقبلي
بالنسبة للقارئ العام، الرسالة الأساسية هي أن خلايا الورم الأرومي الدبقي الناجية لا تكتفي بـ«الاختباء» من العلاج؛ بل تعيد توصيل طريقة استخدام السكر بنشاط للبقاء على قيد الحياة. تمتص المزيد من الجلوكوز، تتجنب تحويله إلى نفايات، وبدلًا من ذلك توجهه لصنع لبنات بناء الـDNA وإمداد الميتوكوندريا بالطاقة—مما يساعدها على إصلاح الضرر، الحفاظ على حالة مرنة شبيهة بالخلايا الجذعية، وفي النهاية إعادة نمو الورم. من خلال كشف حالة بقاء أيضية مشتركة، تشير الدراسة إلى أفكار علاجية جديدة: استهداف خطوات معالجة السكر المبكرة، المسار الجانبي لصنع الـDNA، أو اعتماد الخلايا على الميتوكوندريا قد يجعل العلاج الكيميائي الإشعاعي القياسي أكثر شمولًا، ويترك عددًا أقل من الهاربين ليبدؤوا المرض من جديد.
الاستشهاد: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
الكلمات المفتاحية: الورم الأرومي الدبقي, استقلاب السرطان, استخدام الجلوكوز, مقاومة العلاج, مسار فوسفات البنتوز