Clear Sky Science · ar
محور HNF4α-HKDC1 ينظم إعادة توجيه أيضي لتعزيز الحركة والنقائل في سرطان المعدة المتقدم
لماذا يهم هذا المرضى
تحدث معظم الوفيات الناتجة عن سرطان المعدة ليس بسبب الورم الأصلي نفسه، بل لأن الخلايا السرطانية تنتقل إلى أجزاء بعيدة من الجسم وتستقر هناك. تكشف هذه الورقة العلمية عن «مفتاح تشغيل» جزيئي خفي يساعد خلايا سرطان المعدة على تغيير كيفية استخدام الوقود لتصبح أكثر قدرة على الحركة. والأهم من ذلك، أنها تشير إلى دواء معتمد بالفعل من إدارة الغذاء والدواء الأمريكية قد يُعاد توظيفه لإطفاء هذا المفتاح وإبطاء الانتشار أو منعه.
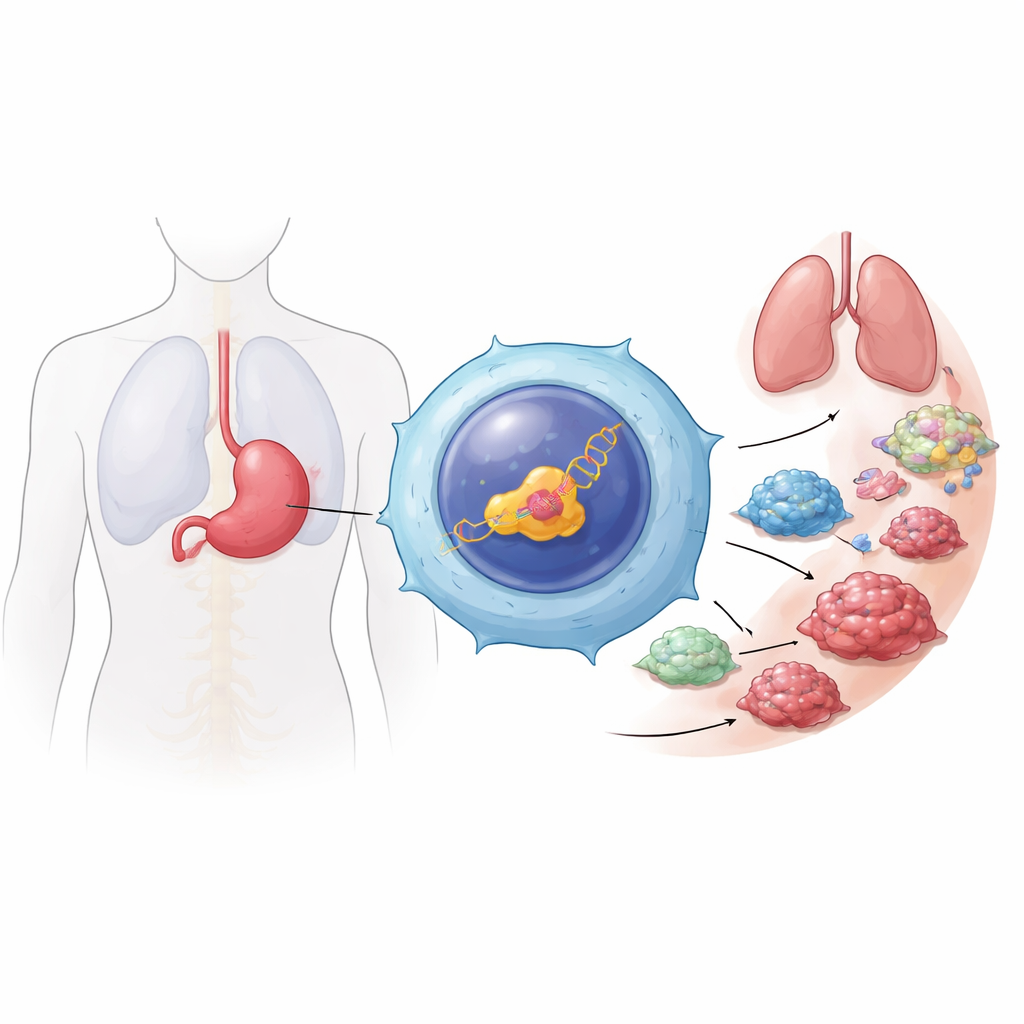
تحول خطير في سرطان المعدة
سرطان المعدة هو خامس أكثر أنواع السرطان شيوعًا عالميًا وغالبًا ما يُكتشف في مراحل متأخرة بعد أن يكون قد انتشر بالفعل. ركز المؤلفون على النقائل—المرحلة التي تنفصل فيها خلايا الورم، وتتحرك عبر البطن أو مجرى الدم، وتستعمر مواقع جديدة. من خلال التنقيب في قواعد بيانات ضخمة عامة لفهم السرطان وفحص عينات أنسجة من مرضى، وجدوا أن شكلًا محددًا من منظمات الجينات يُدعى HNF4α الذي يُدار عبر المُروّج P2 (P2‑HNF4α) يكون وفيرًا بشكل خاص في الآفات النقيلية البعيدة مقارنة بالأورام الأصلية والأنسجة السليمة المجاورة. وُجد هذا الشكل أساسًا داخل الخلايا الورمية، وليس في الخلايا الطبيعية المحيطة، مما يشير إلى ارتباط وثيق بينه وبين السلوك الغازي للسرطان.
مفتاح رئيسي يعزز حركة الخلية
لاختبار العلاقة السببية، عدّل الباحثون مستويات P2‑HNF4α في مجموعة من خطوط خلايا سرطان المعدة البشرية التي تمثل الأنماط الجزيئية الرئيسية للمرض. عندما خفضوا HNF4α في خلايا كانت تعبر عنه طبيعيًا، فقدت الخلايا قدرة كبيرة على التحرك والغزو عبر أغشية صناعية أو إغلاق الجروح في أطباق الزراعة. وعندما أجبروا خلايا ذات مستوى منخفض من HNF4α على إنتاج شكل تمثيلي من P2‑HNF4α، أصبحت تلك الخلايا أكثر قدرة على الحركة والغزو بشكل ملحوظ، بما في ذلك في اختبارات الكُرات ثلاثية الأبعاد التي تحاكي الأورام الحقيقية. في الفئران، شكلت الخلايا المهندسة لإفراز كميات كبيرة من P2‑HNF4α العديد من العقيدات النقيلية في التجويف البطني، مبيّنة أن هذا العامل يدفع الانتشار في الكائن الحي بنشاط.
تغذية الانتشار عبر إعادة توجيه استخدام الطاقة
غالبًا ما تعيد الخلايا السرطانية تشكيل كيفية معالجتها للمغذيات لدعم النمو والحركة. باستخدام تسلسل الحمض النووي الريبوزي ومقاييس المستقلبات معًا، اكتشف الفريق أن خفض HNF4α يضعف مسارًا رئيسيًا لإنتاج الطاقة: التحلل السكري، أي تفكك الجلوكوز. انخفضت مستويات عدة إنزيمات وسلسلة من المنتجات الوسيطة في التحلل السكري، وكذلك مقاييس ناتج الطاقة مثل استهلاك الأكسجين، وإنتاج الحمض، وتوليد ATP. أظهرت تحليلات إضافية أن إنزيمًا واحدًا، HKDC1، هو الأكثر ارتباطًا وباستمرار مع HNF4α. يقع HKDC1 في الخطوة الأولى من معالجة الجلوكوز ويساعد على توجيه السكر نحو كل من إنتاج اللاكتات والتنفس الميتوكوندري — مخرجان يوفّران معًا الطاقة ويخلقان بيئة كيميائية مؤاتية لحركة الخلايا.
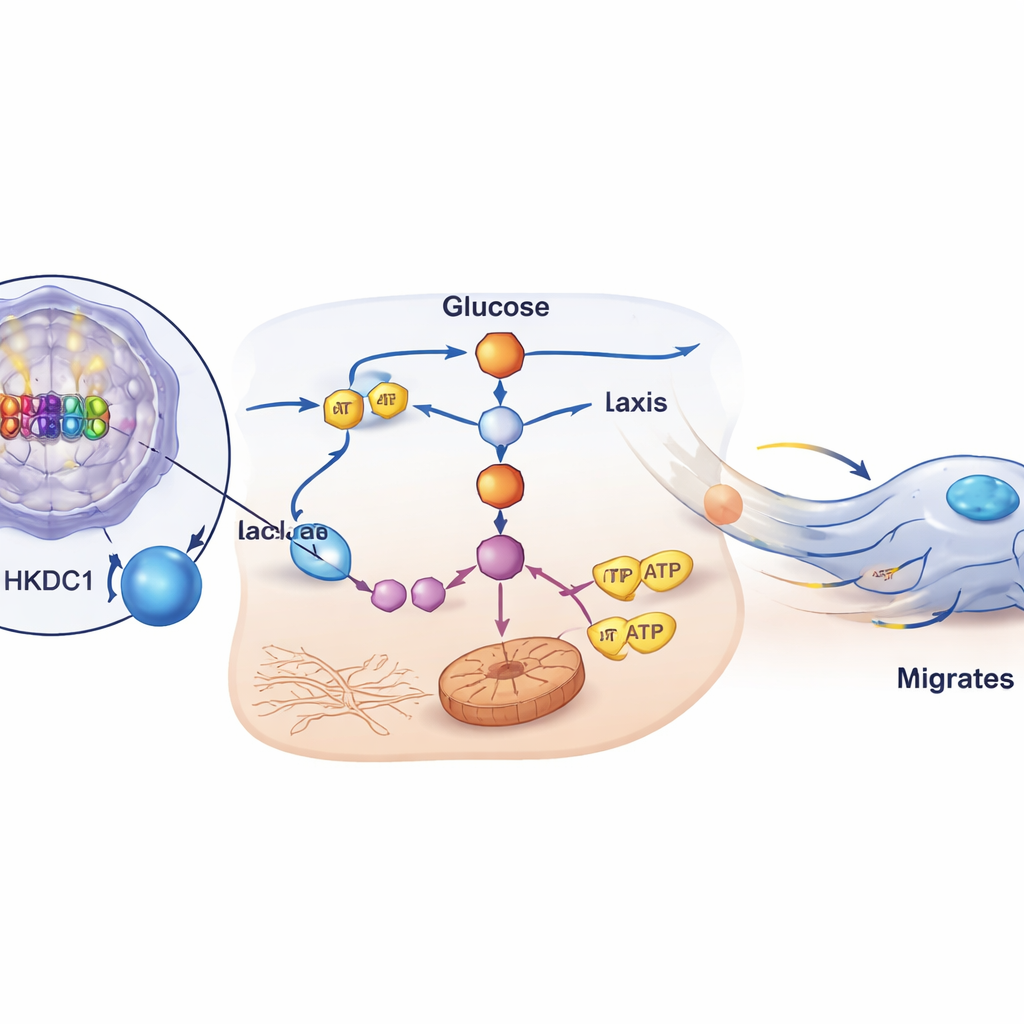
رابط جزيئي مباشر وشريك أساسي
أظهر العلماء أن P2‑HNF4α لا يقتصر وجوده على الارتباط بـ HKDC1 فحسب، بل يشغّله مباشرة. باستخدام بيانات ارتباط واسعة النطاق للجينوم، وتجارب تقاريرية على الحمض النووي، واختبارات ارتباط البروتين–الحمض النووي، رصدوا مواقع محددة في منطقة معزِّزة لجين HKDC1 حيث يرتبط HNF4α وينشّط النسخ. عندما تم خفض HKDC1 في الخلايا، تدنت قدرتها على الحركة وتكوين نقائل صفاقية في الفئران بشكل كبير، رغم أن بقائها على المدى القصير لم يتأثر. والأهم من ذلك، أن إعادة HKDC1 إلى الخلايا التي تم فيها خفض HNF4α أعادت النشاط السكري وإنتاج الطاقة والسلوك الحركي، كما أن إضافة نواتج أيضية نهائية مثل اللاكتات أو α‑كيتوغلوتارات أيضًا أعادت الحركة. تجتمع هذه النتائج لتدل على أن HKDC1 هو مُمكِّن مركزي لاحق تعمل من خلاله P2‑HNF4α لإعادة برمجة الأيض لتغذية النقائل.
إيقاف المفتاح بدواء موجود
بما أن HNF4α ينتمي إلى عائلة من البروتينات التي غالبًا ما تُستهدف دوائيًا، اختبر الفريق ما إذا كان دواء معتمدًا قادرًا على حجب هذا المحور المؤيد للنقائل. كانوا قد حددوا سابقًا حمض المايكوفينوليك، الشكل النشط من دواء زراعة الأعضاء مايكوفينولات ميفيتيل (MMF)، كمضاد لـ HNF4α في سرطان الرئة. هنا، خفّض علاج MMF مستويات HKDC1 وحركة الخلايا في خطوط سرطان المعدة التي تعبر HNF4α بشكل مرتفع، لكنه كان له تأثير ضئيل في الخلايا ذات HNF4α المنخفض. في نماذج الفئران، قلّل MMF بشكل كبير من النقائل البطنية وخفض تعبير HKDC1 — لكن فقط عندما كانت الأورام غنية بـ P2‑HNF4α. يشير ذلك إلى أن HNF4α قد يكون هدفًا علاجيًا وبيوماركر لاختيار المرضى الأكثر احتمالًا للحصول على فوائد من استراتيجيات تعتمد على MMF.
ماذا يعني هذا لعلاج المستقبل
بعبارة بسيطة، تحدد هذه الدراسة نظام تحكم جزيئيًا في الوقود — P2‑HNF4α الذي يعمل عبر HKDC1 — يساعد خلايا سرطان المعدة على تشغيل آلتها الطاقية لتصبح أفضل في الانتشار. من خلال إظهار أن دواءً قائمًا يمكنه تعطيل هذا النظام وتقليل النقائل في نماذج قبل سريرية، تفتح الدراسة طريقًا واقعيًا نحو علاجات جديدة لسرطان المعدة المتقدم. إذا أكدت دراسات سريرية لاحقة هذه النتائج، فقد يساعد فحص نشاط HNF4α في الأورام على توجيه استخدام MMF أو عوامل ذات صلة لإبطاء أو منع الانتشار المميت لهذا المرض.
الاستشهاد: Xu, X., Wu, H., Shang, J. et al. HNF4α-HKDC1 axis orchestrates a metabolic rewiring to promote migration and metastasis in advanced gastric cancer. Cell Death Dis 17, 347 (2026). https://doi.org/10.1038/s41419-026-08627-y
الكلمات المفتاحية: نقائل سرطان المعدة, HNF4A, HKDC1, أيض السرطان, مايكوفينولات ميفيتيل