Clear Sky Science · ar
اعتماد الأرجينين في نقائل الصفاق لسرطان المبيض الظهاري يكشف عن ضعفه العلاجي
لماذا يهم هذا صحة النساء
يعد سرطان المبيض الظهاري من أخطر السرطانات التي تصيب النساء لأنه يُكتشف عادةً فقط بعد أن يكون قد انتشر بصمت في البطن. أحد الأماكن المفضلة لهذه الخلايا السرطانية المتنقلة هو مِئْزَر دهني من الأنسجة يُدعى الشبكة الكبرى (الomentum). تكشف هذه الدراسة عن ضعف خفي في تلك النقائل الشبكية: فهي تعتمد بدرجة غير اعتيادية على الحمض الأميني الغذائي الأرجينين. من خلال تتبع كيفية استخدام الخلايا المنتقلة للأرجينين لإصلاح حمضها النووي التالف والبقاء تحت الضغوط، يشير الباحثون إلى استراتيجيات علاجية جديدة قد تحرم النقائل من الغذاء أو تغلق مسارات نجاتها.
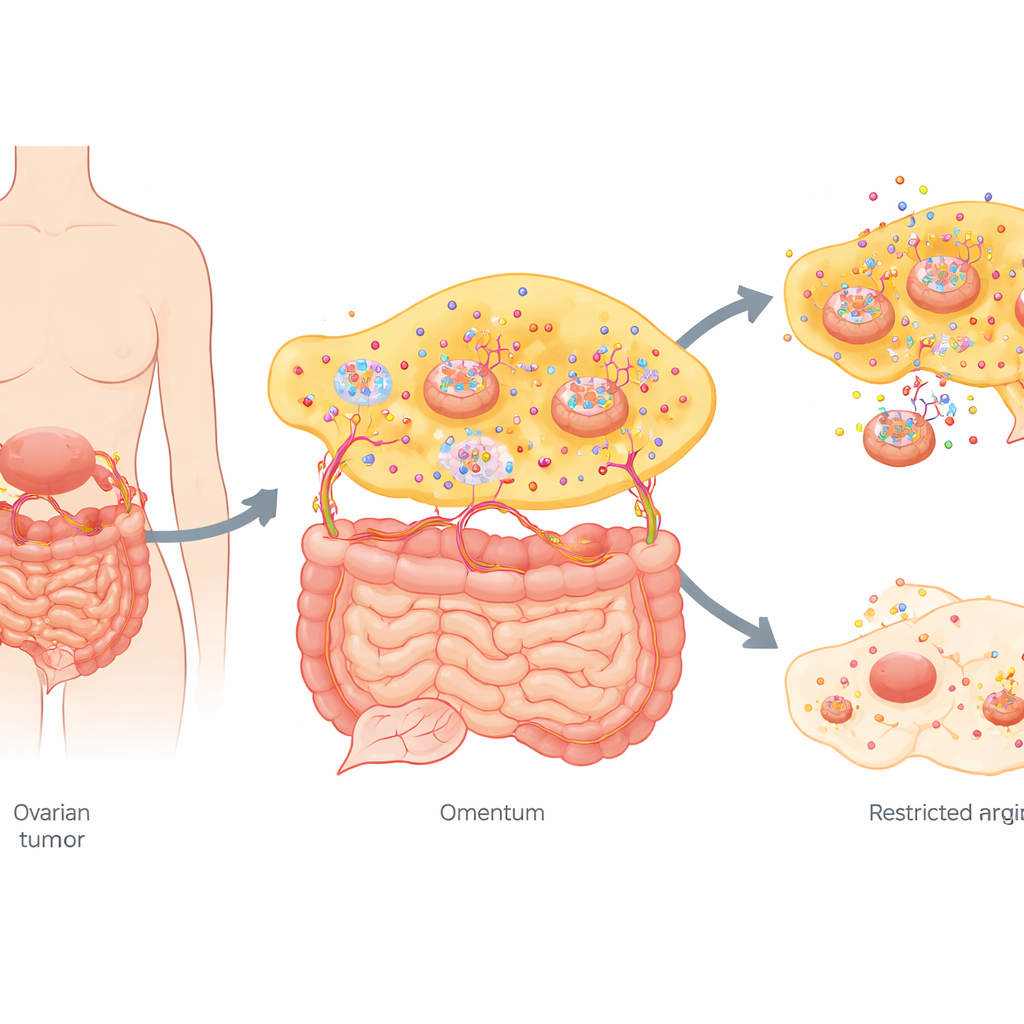
سرطان جائع للمغذيات في موضع خاص
غالبًا ما تزرع أورام المبيض المتقدمة مستعمرات صغيرة عبر تجويف البطن، خاصة في الشبكة الكبرى، وهي نسيج غني بالدهون يغطي الأمعاء. قارن الفريق الأورام المبيضية الأولية مع نقائلها المطابقة في الشبكة لدى نساء لم يخضعن للعلاج بعد. أظهر مسح شامل لمئات الجزيئات الصغيرة أن «البصمة» الأيضية للنقائل كانت مختلفة بشكل لافت. من بين التغيرات العديدة، برز واحد: تراكم الأرجينين في نقائل الشبكة كان أكبر بكثير منه في الأورام المبيضية الأصلية. في الوقت نفسه، انخفضت مستويات الإنزيمات اللازمة لصنع الأرجينين داخل الخلية، بينما ارتفعت بروتينات النقل التي تستورد الأرجينين من الخارج، مما يشير إلى أن الخلايا المنتقلة أصبحت معتمدة على الأرجينين من محيطها.
تجويع الأورام عن طريق قطع إمداد الأرجينين
لاختبار ما إذا كانت هذه الاعتمادية على الأرجينين مهمة فعلًا، استخدم الباحثون نماذج فأرية لسرطان المبيض. عندما وُضعت الفئران الحاملة للأورام على حمية خالية من الأرجينين، انكمشت كل من الأورام المبيضية الرئيسية والنقائل البطنية المنتشرة بشكل ملحوظ. أظهرت الصور إشارات ورمية أضعف، ونقاط نقيلية أقل حجماً وعددًا، وكمية سائل بطني أقل، وبقاءً أفضل مقارنةً بالفئران التي كانت على حمية عادية. في الأطباق، نمت خلايا سرطان المبيض البشرية ببطء، وتحركت أقل، وغزت بمعدل أدنى عندما كان الأرجينين نادرًا. رفع الأرجينين إلى مستويات مشابهة أو أعلى من تلك الموجودة لدى المرضى ذوي النقائل أعطى التأثير المعاكس، مسرعًا النمو والحركة. كما عزز إفراط التعبير عن ناقل الأرجينين هذه السلوكيات العدوانية، مما يوضح أن الأورام تزدهر عندما يتوفر الأرجينين بغزارة.
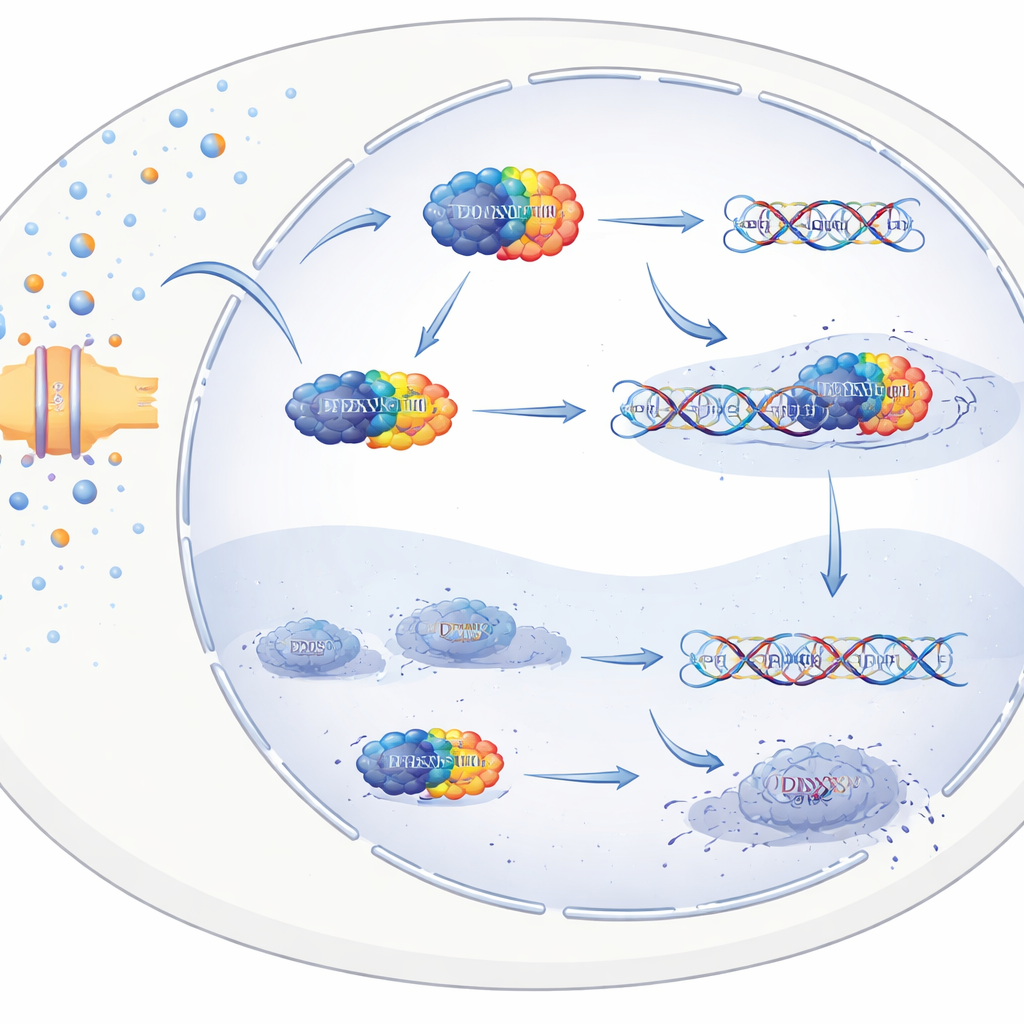
كيف يساعد الأرجينين خلايا السرطان على إصلاح حمضها النووي
سأل العلماء بعد ذلك كيف يغذي الأرجينين الانتقال على المستوى الجزيئي. استخدموا طُعمًا كيميائيًا لصيد البروتينات التي ترتبط فعليًا بالأرجينين وحددوا العديد من البروتينات المختصة بالتعامل مع الرنا، مع التركيز على بروتين واحد يُدعى DDX3X. كان هذا البروتين أكثر وفرة في النقائل منه في الأورام الأولية وكان مرتبطًا بنتائج أسوأ للمرضى. أظهرت التجارب المخبرية والمحاكاة الحاسوبية أن الأرجينين يركن إلى منطقة محددة في DDX3X ويغير مكانه داخل الخلية. عند ارتفاع مستوى الأرجينين، يتراكم DDX3X في نواة الخلية لأن الأرجينين يتداخل مع الإشارة التي تصدره عادةً عائدًا إلى السيتوبلازم. بمجرد دخوله النواة، يرتبط DDX3X بالحمض النووي ويعزز نشاط الجينات المشاركة في مسارات استجابة تلف الحمض النووي، وخصوصًا محور ATM–CHK2–p53 الذي يستشعر الكسور في الحمض النووي وينسق إصلاحها.
البقاء تحت الضغط في بيئة خطرة
تواجه الخلايا المنتقلة في الشبكة إجهادًا تأكسديًا شديدًا وتظهر عليها أضرار في الحمض النووي أكثر من الأورام الأولية، وهو ما ينبغي أن يهدد بقاءها. وجدت الدراسة أن النقائل الغنية بالأرجينين امتلكت أيضًا مستويات أعلى من مؤشرات إصلاح الحمض النووي النشط. عندما أضيف الأرجينين إلى خلايا تعرضت للمواد الكيميائية المضادة للسرطان أو للإجهاد التأكسدي، أُصلحت الكسور في الحمض النووي بكفاءة أكبر وماتت خلايا أقل. إزالة DDX3X، أو حجب بروتيني ATM أو CHK2 أسفل منه، أزال هذا التأثير الوقائي. بعبارة أخرى، يسمح الأرجينين لخلايا سرطان المبيض المنتقلة بأن تشعر ببيئتها المغذية ومن خلال DDX3X تُشغّل برامج إصلاح حمض نووي قوية تساعدها على تحمل كل من موضع الشبكة العدائي والعلاجات المضادة للسرطان.
تحويل شهية للمغذيات إلى فرصة علاجية
نظرًا لأن تقييد الأرجينين طويل الأمد لدى المرضى قد يكون صعبًا، استكشف المؤلفون استراتيجيات دوائية. في الفئران، أدى استنفاد الأرجينين في مجرى الدم بواسطة إنزيم أو تثبيط DDX3X مباشرة بجزيء صغير إلى إبطاء نمو الورم، وتقليل انتشار النقائل، وإطالة البقاء. عمل الجمع بين استنزاف الأرجينين وتثبيط DDX3X بشكل أفضل، كما أن حجب DDX3X حسّن استجابة خلايا سرطان المبيض المقاومة للسيزبلاتين للعلاج الكيميائي، فصغر الأورام المقاومة في الفئران. معًا، تكشف النتائج أن نقائل الشبكة في سرطان المبيض مُدمنة أيضيًا على الأرجينين الخارجي، الذي تُمرّره عبر DDX3X للحفاظ على إصلاح الحمض النووي والبقاء. قد يفتح استهداف دائرة الأرجينين–DDX3X–إصلاح الحمض النووي، إما بتقليل الأرجينين أو بتثبيط DDX3X، طرقًا جديدة للوقاية أو علاج سرطان المبيض النقائلي وتغلب المقاومة الدوائية.
الاستشهاد: Tian, J., Lei, T., Du, Y. et al. Arginine dependency in omental metastasis of epithelial ovarian cancer reveals a therapeutic vulnerability. Cell Death Dis 17, 354 (2026). https://doi.org/10.1038/s41419-026-08606-3
الكلمات المفتاحية: سرطان المبيض, استقلاب الأرجينين, انتقال السرطان, إصلاح ضرر الحمض النووي, DDX3X