Clear Sky Science · ar
ثَبط كيناز مرتبط بالڤاكسينيا 2 يكشف عن ضعف في أيض الغلوتاثيون في سرطان البنكرياس
لماذا يهم هذا بالنسبة لسرطان البنكرياس
يُعد سرطان البنكرياس من أكثر السرطانات فتكا، ويرجع ذلك جزئياً إلى فشل العلاجات القياسية في كثير من الأحيان. تكشف هذه الدراسة نقطة ضعف خفيّة في بعض أورام البنكرياس: اعتمادها على «درع» خلوي ضد نواتج الأكسدة السامة. من خلال فهم متى يكون هذا الدرع هشا، وكيف يعززه جين سرطاني يدعى VRK2، يقترح الباحثون طرقا جديدة لتسميم الخلايا السرطانية بشكل انتقائي مع الحفاظ على الأنسجة السليمة.
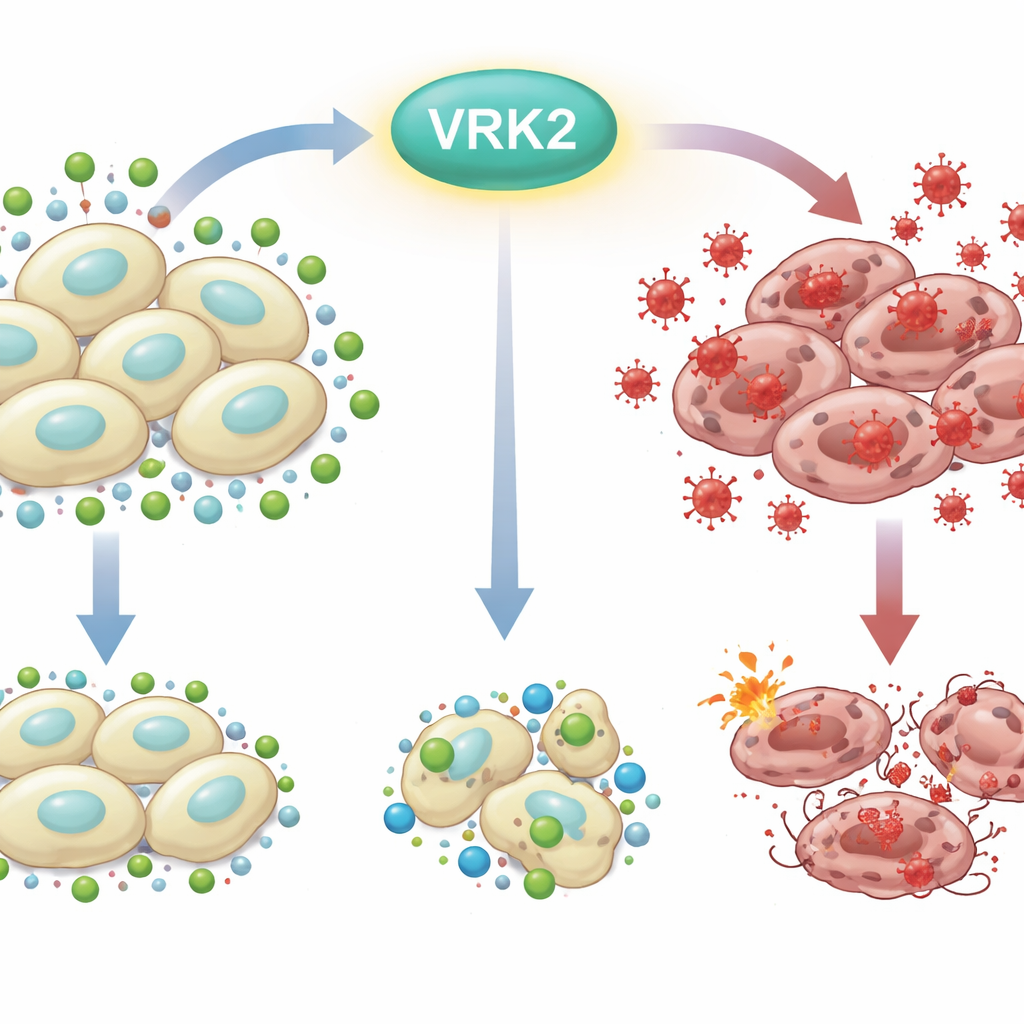
مشكلة الصدأ داخل الخلية
تقاوم كل خلية باستمرار «الصدأ من الداخل» الناتج عن مركبات الأكسجين التفاعلية—أشكال أكسجين عالية التفاعل يمكنها إتلاف الحمض النووي والدهون والبروتينات. للبقاء على قيد الحياة، تستخدم الخلايا دفاعات كيميائية، ويُعد الغلوتاثيون واحدا من أهم هذه الدروع. خلايا سرطان البنكرياس، التي تعيش في ظروف قاسية وتنمو بسرعة، تعتمد كثيرا على حيل أيضية للحفاظ على مستويات كافية من الغلوتاثيون. إن إزعاج هذا التوازن بين المؤكسدات الضارة ومضادات التأكسد الوقائية يمكن أن يدفع الخلايا السرطانية إلى حافة الموت الخلوي.
اكتشاف نقطة ضعف خفية
بدأ الباحثون بإيقاف عمل VRK2، وهو جين يسهِم في السرطان وكان مرتبطا سابقا بنتائج سيئة في سرطان البنكرياس، ثم اختبروا 281 مركبا يستهدف العمليات الأيضية. اكتشفوا أن الخلايا التي تفتقر إلى VRK2 كانت حساسة بشدة للأدوية التي تمنع إنتاج الغلوتاثيون. في هذه الخلايا المنقوصة من VRK2، انخفضت مستويات الغلوتاثيون بينما ارتفعت المركبات المؤكسدة، ما أدى إلى موت الخلايا. إن تزويدها بمضادات أكسدة إضافية أو بجزيئات تشبه الغلوتاثيون أنقذها، مما أكد أن نقطة الضعف الأساسية تكمن في عدم قدرتها على إزالة السموم الناتجة عن الإجهاد التأكسدي.
كيف يساعد VRK2 الخلايا السرطانية على المقاومة
بعد ذلك، سأل الفريق لماذا يغير VRK2 أيض الغلوتاثيون. ركزوا على بروتين ناقل يسمى SLC7A11، يتوضع في الغشاء الخارجي للخلية وينقل السيستين، وهو لبنة لازمة لصنع الغلوتاثيون. ومن المدهش أن VRK2 لم يغير كمية SLC7A11 التي تنتجها الخلية إجمالا؛ بل كان يتحكم في ما إذا كان هذا الناقل يصل بنجاح إلى سطح الخلية. في الخلايا السليمة التي يعمل فيها VRK2، ينتقل SLC7A11 من الشبكة الإندوبلازمية إلى جهاز جولجي ثم إلى الغشاء. يعزز VRK2 هذا النقل عبر تعديل كيميائي لبروتين فرز الحمولة المسمى Sec24C، الذي يساعد في تحميل SLC7A11 داخل حويصلات النقل. عندما يغيب VRK2 أو يُثبط، يعلق SLC7A11 داخل الخلية، ويصل عدد أقل من الناقلات إلى السطح، ويضعف درع الغلوتاثيون.
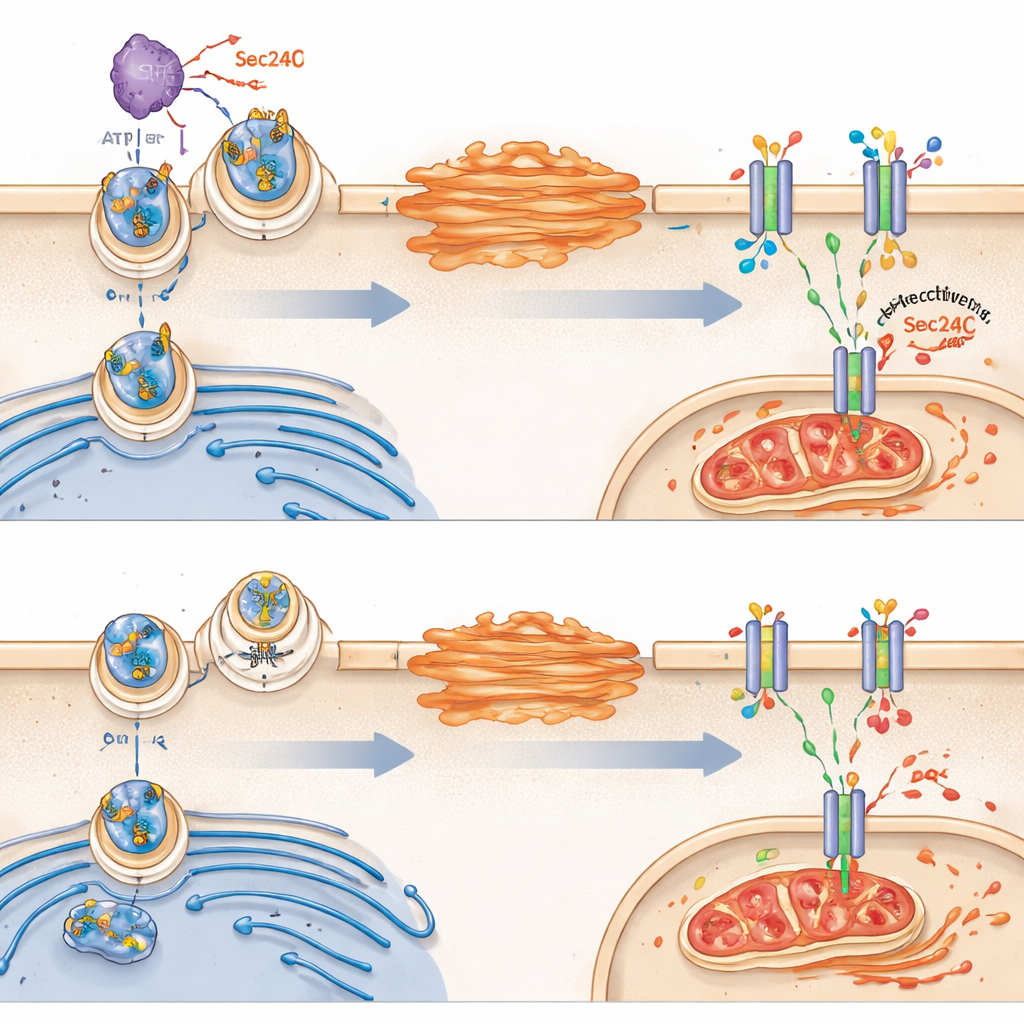
من الدرع المكسور إلى الفيروبتوز
بدون كمية كافية من SLC7A11 على الغشاء، تكافح الخلايا المعيبة في VRK2 لاستيراد السيستين والحفاظ على الغلوتاثيون. هذا يجعلها عرضة بصورة خاصة لشكل من موت الخلايا المعتمد على الحديد يسمى الفيروبتوز، الذي يتسم بأكسدة مفرطة لدهون غشاء الخلية وتلف الميتوكوندريا. أظهرت الدراسة أن الأدوية التي تقطع تصنيع الغلوتاثيون أثارت سمات الفيروبتوز في الخلايا المنقوصة من VRK2، بما في ذلك تشوهات الميتوكوندريا وتراكم منتجات تأكسد الدهون. إن حجب الفيروبتوز، وليس أشكال الموت الخلوي الأخرى، حمى هذه الخلايا، مما يبرز أن نقطة ضعفها الأساسية هي عجزها عن احتواء الأضرار التأكسدية.
توجيه اختيارات العلاج المخصص
أخيرا، انتقل الباحثون إلى نماذج حيوانية وخلايا مستمدة مباشرة من مرضى. تقلصت الأورام منخفضة مستويات VRK2 عند معالجتها بعقار يستهدف الغلوتاثيون، بينما كانت الأورام ذات التعبير العالي عن VRK2 مقاومة لذلك إلى حد كبير. ومع ذلك، عندما أعطي للأورام ذات VRK2 العالي أيضا مركب مثبط لـ VRK2، استعادت حساسيتها لتثبيط الغلوتاثيون. هذا يشير إلى أن مستويات VRK2 يمكن أن تصنف المرضى إلى مجموعات: أولئك الذين تكون أورامهم عرضة بطبيعتها للعلاج المستهدف للغلوتاثيون، وأولئك الذين قد يستفيدون من استراتيجية ثنائية الخطوات تفكك VRK2 أولا ثم تهاجم أيض الغلوتاثيون.
ماذا يعني هذا للمرضى
ببساطة، تُظهر هذه الدراسة أن بعض سرطانات البنكرياس تبقى حية باستخدام VRK2 للحفاظ على درعها المضاد للأكسدة قويا. أزل VRK2، فيضعف الدرع؛ وأزل الغلوتاثيون بعد ذلك، فتنهي الخلايا السرطانية تحت ضغط الإجهاد التأكسدي. لذلك يمكن لقياس VRK2 في الأورام أن يساعد الأطباء على تحديد من هم الأكثر احتمالا للاستفادة من أدوية تعطل أيض الغلوتاثيون، ومن قد يحتاج أولا إلى خطوة استهداف VRK2. ومع الحاجة إلى مزيد من الاختبارات على البشر، ترسم الدراسة مسارا واضحا نحو علاجات مخصّصة مبنية على الأيض لسرطان بحاجة ماسة إلى خيارات أفضل.
الاستشهاد: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
الكلمات المفتاحية: سرطان البنكرياس, أيض الغلوتاثيون, VRK2, الفيروبتوز, SLC7A11