Clear Sky Science · ar
قمع EGFR بواسطة البيغوانيد الجديد 4C عزّز حساسية سرطان المبيض لمثبطات PARP عبر تثبيط BRCA2 و Rad51
لماذا يهم هذا البحث
بالنسبة لكثير من الأشخاص الذين يُشخَّص لديهم سرطان المبيض، تعمل الأدوية الموجهة الحالية فقط على أقلية صغيرة من المرضى الذين تحمل أورامهم عيوباً جينية محددة. يستكشف هذا البحث وسيلة لتوسيع فوائد فئة مهمة من الأدوية تُسمى مثبطات PARP إلى مجموعة أكبر بكثير من المرضى الذين تفتقر أورامهم إلى تلك الطفرات. من خلال إقران مركب تجريبي جديد مع أدوية موجودة، يُظهر الباحثون استراتيجية لدفع خلايا السرطان إلى مأزق قاتل مع الحفاظ على الأنسجة السليمة.
عقبة في علاج سرطان المبيض الحالي
غالباً ما يُكتشف سرطان المبيض في مراحل متأخرة ويظل واحداً من أكثر السرطانات فتكاً بين النساء. يمكن أن تكون مثبطات PARP، مثل الأولاباريب، فعالة بشكل لافت، لكن ذلك يحدث أساساً لدى المرضى الذين تحمل أورامهم أعطاب في مسار إصلاح الحمض النووي المرتبط بجينات BRCA1 وBRCA2. ومع ذلك، تظل آليات الإصلاح سليمة في معظم الأورام ويمكنها إصلاح الضرر الذي تُحدثه هذه الأدوية، مما يسمح لخلايا السرطان بالبقاء. جزء رئيسي من طاقم الإصلاح هذا يتضمن بروتينين، BRCA2 وRad51، اللذين يساعدان في صِيانة شُظايا الحمض النووي عبر عملية تُسمى إعادة التركيب المتجانس. قد يجعل إيجاد طرق لإضعاف هذا المسار الإصلاحي انتقائياً في خلايا السرطان مثبطات PARP مفيدة لعدد أكبر بكثير من المرضى.
دور مفتاح نمو معروف
ركز الفريق على جزيء مرتبط بالسرطان معروف، مستقبل عامل نمو البشرة (EGFR)، الذي يوجد على سطح العديد من خلايا الورم ويحفز نموها. وجدوا أن EGFR يفعل أكثر من مجرد إرسال إشارات نمو: في خلايا سرطان المبيض ذات جينات BRCA الطبيعية، ارتبطت المستويات العالية من EGFR بسوء بقاء المرضى ومقاومة لمثبطات PARP. عندما نُقصَّ أو أُوقف EGFR في مزروعات خلوية وفي الفئران، أصبحت الأورام أكثر عرضة بشكل كبير للأولاباريب. أظهر الباحثون أن EGFR يساعد في نقل BRCA2 وRad51 إلى نواة الخلية بعد حدوث ضرر في الحمض النووي، حيث يمكنهما إصلاح الكسور وتخفيف تأثير العلاج. لم يكن مجرد تثبيط نشاط إنزيمي لـEGFR كافياً؛ بل كان لا بد من خفض كمية بروتين EGFR الإجمالية لتعطيل هذا المسار الإصلاحي بشكل ملموس.
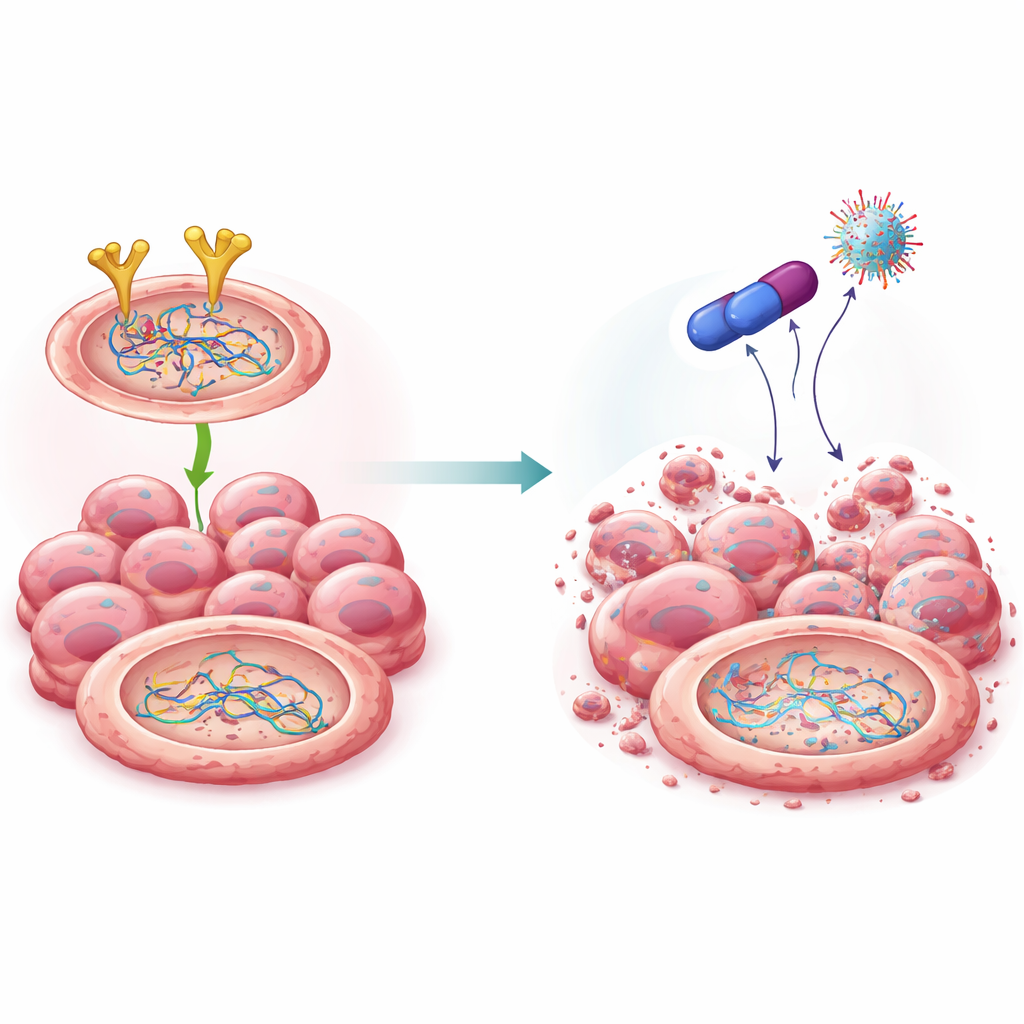
مركب جديد يعرقل طاقم الإصلاح
بناءً على أعمال سابقة مع عائلة أدوية تعرف بالبيغوانيدات، سنت العِلماء عدة مركبات كيميائية شقيقة وحددوا جزيئاً بارزاً سُمِّي 4C. كان هذا المركب ساماً بشدة لخلايا سرطان المبيض ومع ذلك رقيق التأثير على الخلايا الطبيعية نسبياً. أشارت النمذجة الحاسوبية والاختبارات المخبرية إلى أن 4C يرتبط مباشرةً بـEGFR ويعلّمه ليتعرض للتدمير في آلات تكسير البروتين داخل الخلية. على عكس بعض أدوية EGFR الموجودة، خفض 4C مقدار EGFR الكلي بدلاً من إسكات نشاطه فقط. مع انخفاض مستويات EGFR، تراجعت أيضاً ثباتية BRCA2 وRad51: فقد طُلِبت إشارات للتخلص منهما، وتحطمتا ولم تعدا قادرتين على دعم إصلاح الحمض النووي بكفاءة. والأهم أن هذا الانتقاص حدث على مستوى البروتين دون تغيير الجينات الأساسية.
حجب مسار إنقاذ داخل الخلية
كشف البحث سلسلة أحداث أكثر تفصيلاً تربط بين تلف الحمض النووي وبقاء الورم. بعد أن تتلف مثبطات PARP الحمض النووي، يرسل بروتين حساس آخر يسمى ATM رسالة من النواة إلى جسم الخلية. استجابة لذلك، يتعاون EGFR مع BRCA2 وRad51 ويساعد في انتقالهما إلى النواة حيث يصلحان الضرر. اكتشف الباحثون أن بروتين ثالث، c-Cbl، يعمل عادة كوسم للتخلص من BRCA2 وRad51. يتنافس EGFR مع c-Cbl على الوصول إلى هذه البروتينات الإصلاحية، مما يقيها من أن تُعلَّم للتدمير. عندما يخفض 4C مستويات EGFR، يمكن لـc-Cbl الارتباط بسهولة أكبر بـBRCA2 وRad51، مما يؤدي إلى وسمهما وتحللهما وفقدانهما. مع تقلص أعداد البروتينات الإصلاحية في النواة، تتراكم آفات الحمض النووي وتصبح خلايا السرطان أكثر حساسية بكثير لمثبطات PARP.
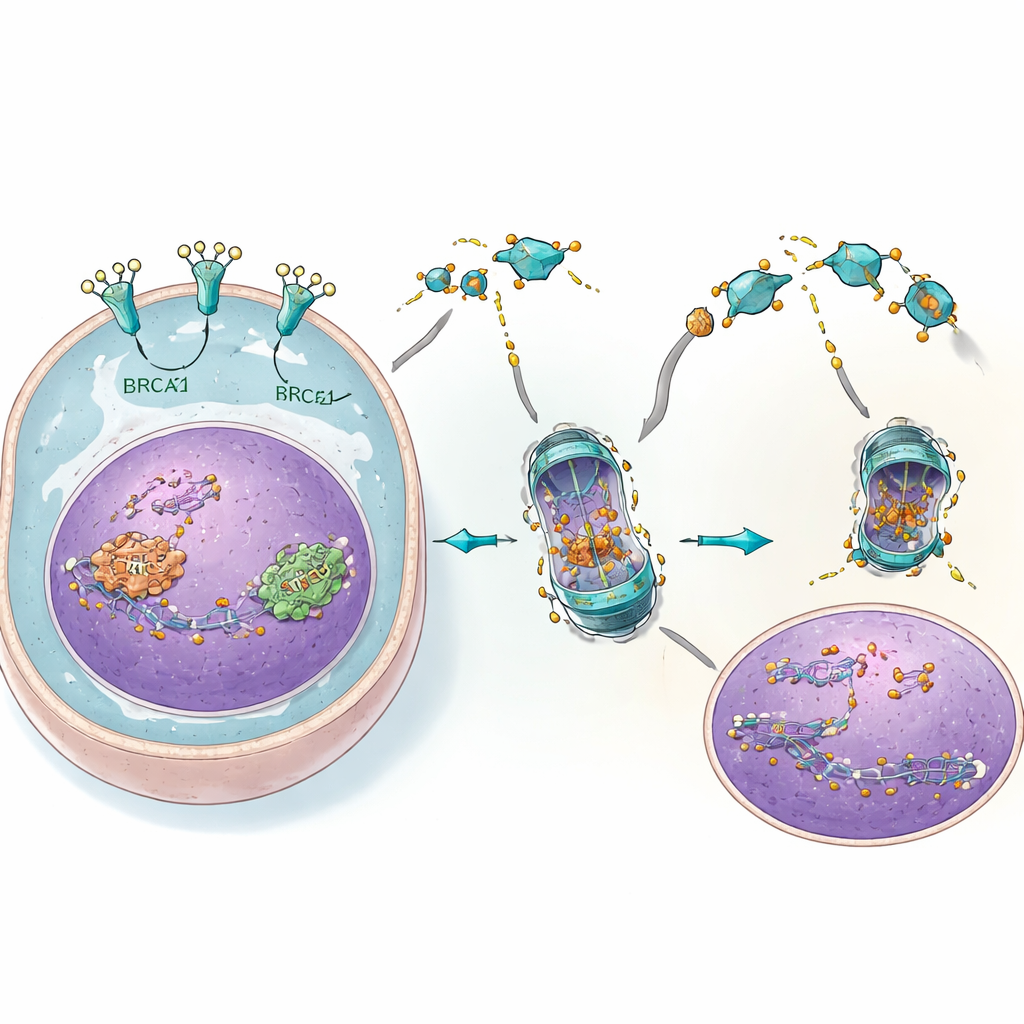
من الخلايا إلى الحيوانات: اقتران قوي
في كل من الخلايا المزروعة ونماذج الفئران، أدى دمج 4C مع مثبطات PARP إلى ضربة قوية مزدوجة. تقلصت الأورام ذات جينات BRCA الطبيعية والتي كانت تقاوم كل دواء بمفرده بشكل دراماتيكي أو توقفت عن النمو عند تعرضها لكليهما معاً. ارتفعت مؤشرات تلف الحمض النووي بشكل حاد، متوافقة مع الفكرة القائلة بأن آلية الإصلاح كانت غارقة. في الوقت نفسه، أظهرت الخلايا الطبيعية والأعضاء الأساسية مثل الكبد والكليتين أدلة قليلة على الضرر، على الأرجح لأن مستويات EGFR فيها أقل بكثير وتعتمد أقل على هذا المسار الإصلاحي المحدد. امتدت فوائد هذا التركيب أيضاً إلى تقليل انتشار خلايا سرطان المبيض في الجسم.
ماذا قد يعني هذا للمرضى
يقترح هذا العمل طريقة لتحويل قوة خلية السرطان إلى نقطة ضعف. من خلال استهداف EGFR بالمركب الجديد 4C، يجرد الباحثون الحماية التي يوفرها BRCA2 وRad51، مما يجعل الأورام التي تمتلك إصلاح حمض نووي طبيعي تتصرف أكثر مثل السرطانات ذات طفرات BRCA في استجابتها لمثبطات PARP. قد توسع هذه القابلية المفروضة، المعروفة بـ"الفتك التركيبي"، نطاق الأدوية الحالية ليشمل عددًا أكبر من النساء المصابات بسرطان المبيض، مع إبقاء الآثار الجانبية ضمن مستوى يمكن التحكم به. وعلى الرغم من أن 4C لا يزال تجريبياً وسيتطلب اختبارات واسعة في نماذج أكثر تقدماً وتجارب سريرية، فإن الدراسة تقدم مخططاً واضحاً لكيفية تحسين نتائج العلاج عبر تفكيك مساعدي الإصلاح المحددين في خلايا الورم.
الاستشهاد: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
الكلمات المفتاحية: سرطان المبيض, مثبطات PARP, EGFR, إصلاح الحمض النووي, العلاج الموجَّه