Clear Sky Science · ar
إشارة اللبتين—LEPR في نقي العظم تعيد برمجة الاستقلاب التأكسدي الميتوكوندري لتمنح مقاومة كيميائية في اللوكيميا النخاعية الحادة
لماذا يهم وجود الدهن في نقي العظم لعلاج اللوكيميا
يعلم كثير من الناس أن الدهون في الجسم يمكن أن تؤثر في أمراض مثل السكري ومشاكل القلب، لكن القليل يدرك أن الدهون المختبئة داخل عظامنا قد تؤثر أيضاً في استجابة سرطانات الدم للعلاج. تستكشف هذه الدراسة كيف يساعد هرمون تفرزه الخلايا الدهنية، يُدعى اللبتين، خلايا اللوكيميا النخاعية الحادة على التحصن ضد العلاج الكيميائي القياسي. قد يشير فهم هذا النظام الوقائي الخفي إلى طرق جديدة لجعل الأدوية الحالية أكثر فعالية للمرضى.
هرمون يغيّر الكفة ضد العلاج الكيميائي
بدأ الباحثون بدراسة عينات نقي العظم من بالغين تم تشخيصهم حديثاً باللوكيميا النخاعية الحادة. قاسوا مستويات اللبتين في النقي وفحصوا مدى اختفاء خلايا اللوكيميا بعد حصول المرضى على دواء كيميائي شائع يُدعى سيتارابين. المرضى الذين كانت لديهم مستويات أعلى من اللبتين في النقي ومستويات أعلى من مستقبلاته على خلايا اللوكيميا كانوا أقل استجابة للعلاج وعمرهم التوقعي أقصر. وحتى بعد احتساب عوامل خطر أخرى، ظل اللبتين مؤشراً قوياً على فشل العلاج الكيميائي. وهذا يوحي أن هرمون المصدر الدهني لا يقتصر دوره على كونه علامة لشدة المرض، بل مرتبط فعلياً بالمقاومة.
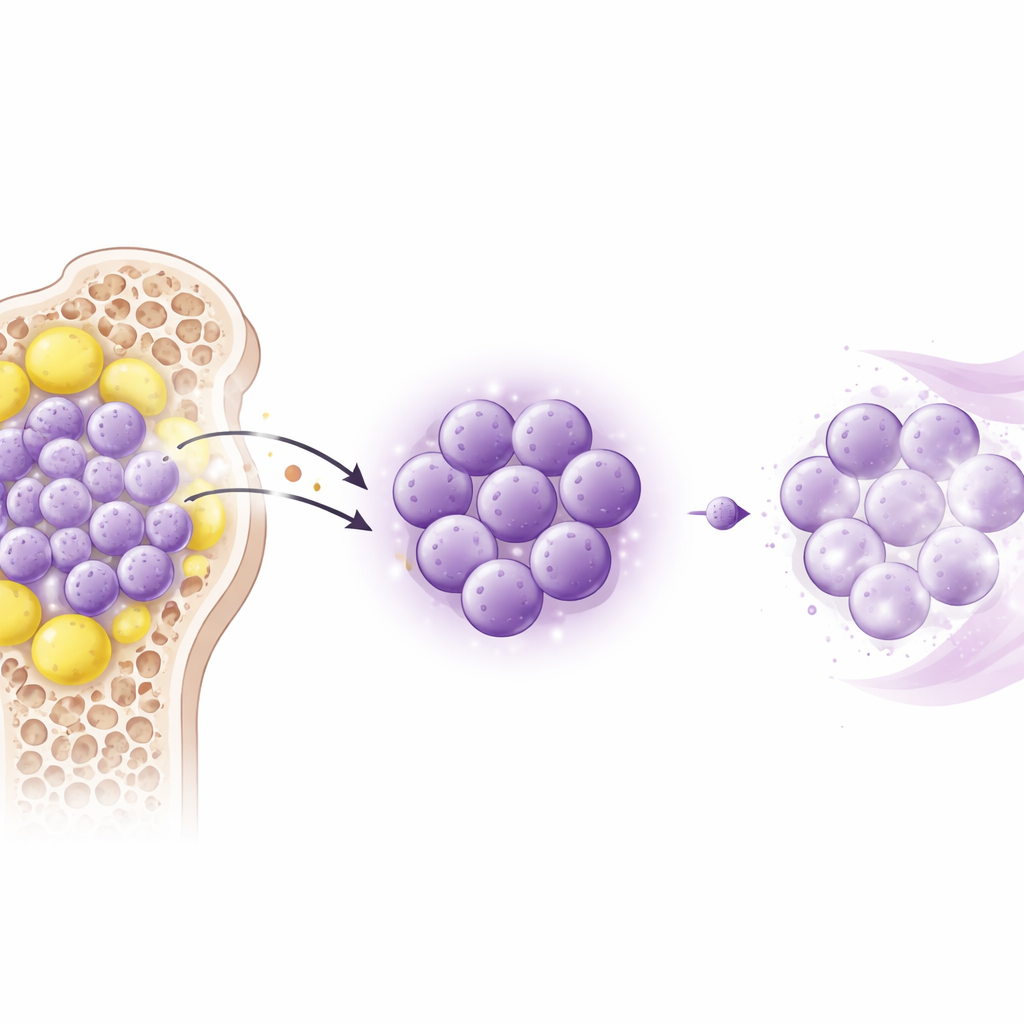
نماذج حيوانية تكشف عن درع خفي
لاختبار ما إذا كان اللبتين يتسبب فعلاً في مقاومة الدواء، لجأ الفريق إلى نموذجين فأريين للوكيميا النخاعية الحادة يحاكان المرض البشري عن كثب. نالت الفئران سيتارابين وحده، أو سيتارابين مع إضافة لبعدين إضافي من اللبتين، أو سيتارابين مع ببتيد صغير يعيق مستقبل اللبتين. إضافة اللبتين قللت مدة البقاء، وكبرت الطحال والكبد، وسمحت لخلايا اللوكيميا بغزو هذه الأعضاء رغم العلاج الكيميائي. بالمقابل، إعاقة المستقبل لم تُبطئ نمو اللوكيميا بمفردها لكنها عززت بشكل كبير تأثير السيتارابين، مصغرةً الأعضاء المرضية ومقللةً عبء اللوكيميا. تبرز هذه النتائج أن التأثير الرئيسي لللبتين ليس تسريع نمو السرطان مباشرة، بل جعل خلاياه أصعب في الاستهداف والقتل عند تطبيق العلاج الكيميائي.
تشغيل مراكز طاقة الخلية
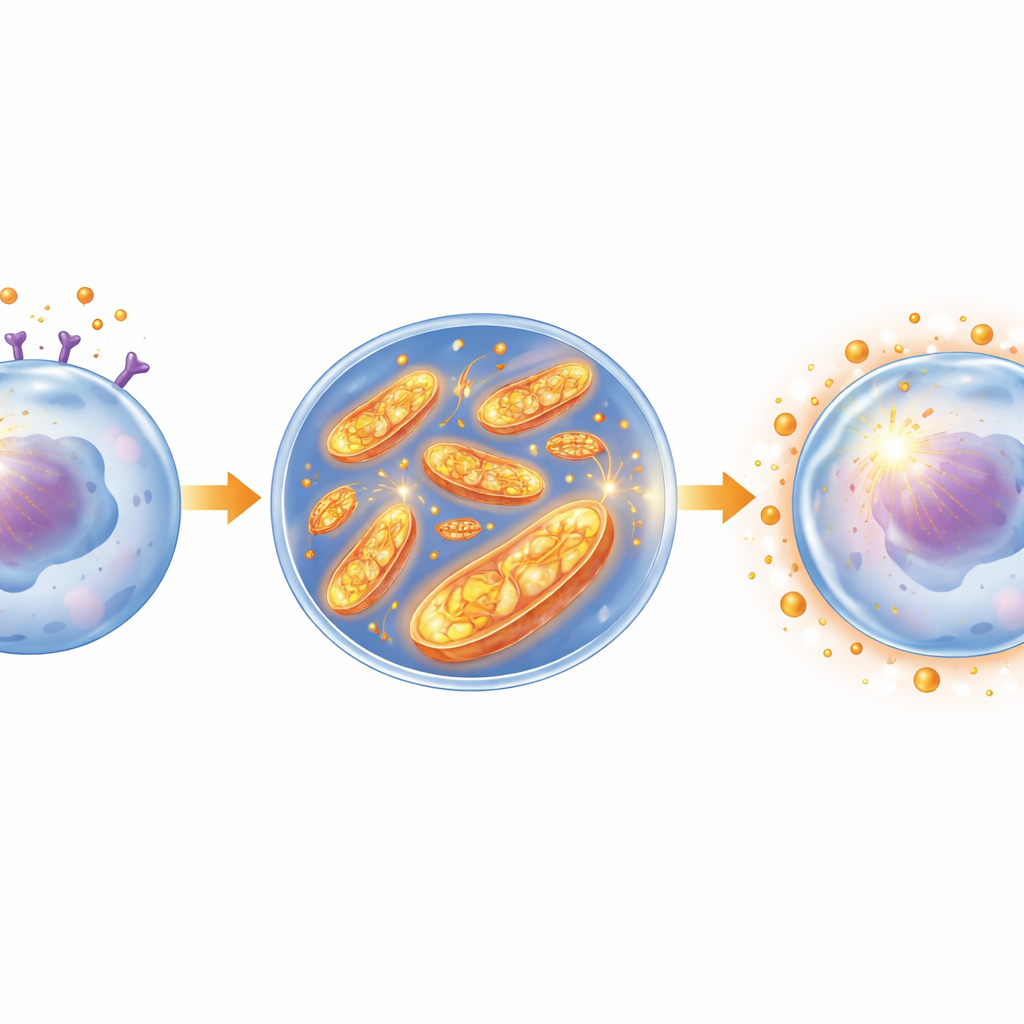
بتعمق أكبر، درس العلماء كيف يغير اللبتين استقلاب خلايا اللوكيميا. وجدوا أن اللبتين يشغل سلسلة إشارية داخل الخلية تُعرف باسم JAK2/STAT3، والتي بدورها تنشط الميتوكوندريا — مصانع الطاقة الصغيرة التي تولّد الطاقة. في خلايا اللوكيميا الفأرية وسلالات خلايا اللوكيميا البشرية، عزز اللبتين نشاط مكون ميتوكوندري رئيسي واحد، المركب الأول، وزاد الاستقلاب التأكسدي العام. هذا التحول ولد المزيد من أنواع الأكسجين التفاعلية داخل الميتوكوندريا. وبشكل مفارقي، بدلاً من إتلاف الخلايا، أدت هذه الزيادة المستمرة في الجزيئات التفاعلية إلى استجابة تكيفية: رفعت خلايا اللوكيميا دفاعاتها المضادة للأكسدة، مثل الغلوتاثيون وإنزيمات إزالة السموم، لتكوّن درعاً داخلياً قوياً.
عندما يصبح الإجهاد درعاً
أظهر الفريق أن هذا الدرع محوري للمقاومة الكيميائية. أبدت الخلايا المعالجة باللبتين قدرة مضادة للأكسدة كلية أعلى وكانت أقل تأثراً بالسيتارابين ودواء آخر، الداونوروبيسين. حذف مستقبل اللبتين بواسطة تعديل جيني أضعف هذه الشبكة المضادة للأكسدة، وخفض مستويات الجزيئات الواقية، وجعل الخلايا أكثر حساسية للعلاج بكثير، حتى من دون وجود اللبتين. أكدت تجارب إضافية أن دفعة حادة من الإجهاد الميتوكوندري يمكن أن تطلق برنامجاً وقائياً مشابهاً، بينما كان اقتناص هذه الجزيئات التفاعلية ينسف الدرع ويعيد حساسية الدواء. والأهم من ذلك، أن حجب إشارة JAK2/STAT3 أو مستقبل اللبتين نفسه منع تنشيط المركب الأول، وخفّض إشارات الإجهاد الميتوكوندري، وأدّى إلى انهيار الحاجز المضاد للأكسدة، وجعل العلاج الكيميائي فعالاً مرة أخرى.
تحويل نقطة ضعف إلى نهج علاجي جديد
رسالة الدراسة للمرضى هي أن خلايا اللوكيميا يمكن أن تستغل هرموناً تصنعه الخلايا الدهنية المجاورة للبقاء على قيد الحياة أثناء العلاج الكيميائي. يلتصق اللبتين القادم من دهن نقي العظم بمستقبله على خلايا اللوكيميا، ويعيد برمجة ميتوكوندريا هذه الخلايا لتصبح منتجين للطاقة بصيغة عالية، ويستخدم الإجهاد منخفض المستوى الناتج لتشغيل شبكة أمان مضادة للأكسدة. هذه الشبكة تحمي الخلايا من الضرر الأعنف الذي تسببه أدوية السرطان. عن طريق حجب مستقبل اللبتين أو إشارة ما بعده، قد يصبح بإمكان الأطباء يوماً نزع هذا الحِماية والسماح للعلاجات الكيميائية الحالية بالعمل كما ينبغي، دون الحاجة بالضرورة لزيادة جرعات الأدوية. وبهذه الطريقة، قد يُترجم فهم أفضل لكيفية تواصل دهون نقي العظم مع خلايا اللوكيميا مباشرةً إلى هزائم أطول أمداً للأمراض لدى الأشخاص المصابين باللوكيميا النخاعية الحادة.
الاستشهاد: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, اللبتين, المقاومة الكيميائية, الميتوكوندريا, الإجهاد التأكسدي