Clear Sky Science · ar
الميوسين النووي 1 يربط البنية الجينومية بإعادة تشكيل النسيج الدهني، الالتهاب الأيضي والسمنة في الفئران
لماذا هيكل الخلية مهم للدهون في الجسم
غالبًا ما تُحمّل السمنة على عاتق ما نأكله ومدى نشاطنا، لكن في أعماق خلايانا، طريقة حزم وقراءة الحمض النووي يمكن أن تزيح الميزان أيضًا. تكشف هذه الدراسة أن بروتينًا محركًا صغيرًا، الميوسين النووي 1 (NM1)، الذي يساعد في تنظيم الحمض النووي داخل نواة الخلية، يلعب دورًا مفاجئًا في كيفية تكوّن الخلايا الدهنية وتخزين الطاقة وإثارة الالتهاب. عبر دراسة فئران تفتقد هذا البروتين، كشف الباحثون رابطًا مباشرًا بين البنية الفيزيائية لجيناتنا وتطور الدهون الحشوية غير الصحية والمشكلات الأيضية.
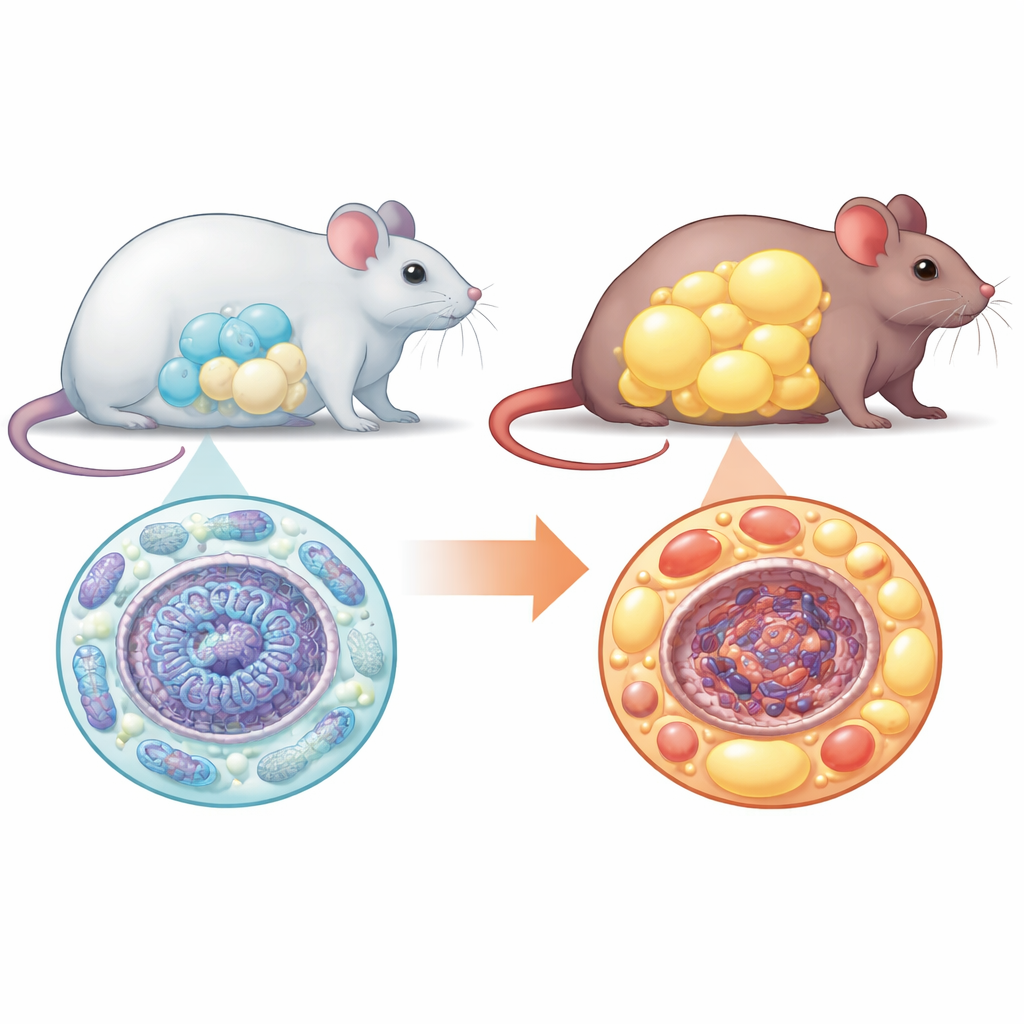
من الخلايا الجذعية إلى الخلايا الدهنية
تتطوّر الخلايا الدهنية من سوابق متعددة الاستخدام تُسمى الخلايا الجذعية الميزنشيمية. عادةً تتكاثر هذه السوابق، وتغيّر استخدام الطاقة، وتنضج إلى العديد من الخلايا الدهنية الصغيرة والفعّالة التي تخزن السعرات الزائدة بأمان. وجد الفريق أنه بدون NM1، يتفكك هذا المسار المنتظم. عندما زرعوا خلايا جذعية من فئران طبيعية وفئران منزوعة NM1 في المختبر وحفزّوها لتصبح خلايا دهنية، أكملت نسبة أقل بكثير من الخلايا الانتقال في غياب NM1. وكانت الخلايا التي نضجت أكبر بكثير من المعتاد، ومليئة بالدهون ولكنها تفتقر إلى العلامات الجينية والبروتينية المعتادة للخلايا الدهنية الصحية. هذا النمط — عدد أقل من الخلايا لكن كل واحدة أكبر — هو سمة مميزة للنسيج الدهني غير الصحي.
كيف يشكّل تكديس الجينات سلوك الخلايا الدهنية
يعمل NM1 في النواة، حيث يساعد في إبقاء مقاطع من الحمض النووي متاحة بحيث يمكن تشغيل الجينات المهمة. لفهم كيف يغيّر فقدانه سلوك الخلية، وضع الباحثون خرائط لمناطق الحمض النووي المفتوحة فوق قياسات نشاط الجينات في خلايا بوجود وبدون NM1. لاحظوا أن العديد من الجينات اللازمة لتكوين الخلايا الدهنية، ومعالجة القطرات الدهنية، وصيانة الميتوكوندريا فقدت كلًا من إمكانية الوصول والنشاط عندما غاب NM1. في الوقت نفسه، أصبحت جينات أخرى مرتبطة بمسارات النمو والإشارة أكثر انفتاحًا ونشاطًا. يشير هذا إلى أن NM1 يعمل كمتصرف رئيسي: يساعد على الحفاظ على توازن بين مناطق الحمض النووي المفتوحة والمغلقة بحيث تقود الشبكات الجينية الصحيحة تطور الخلايا الدهنية الصحية والتمثيل الغذائي المتوازن.
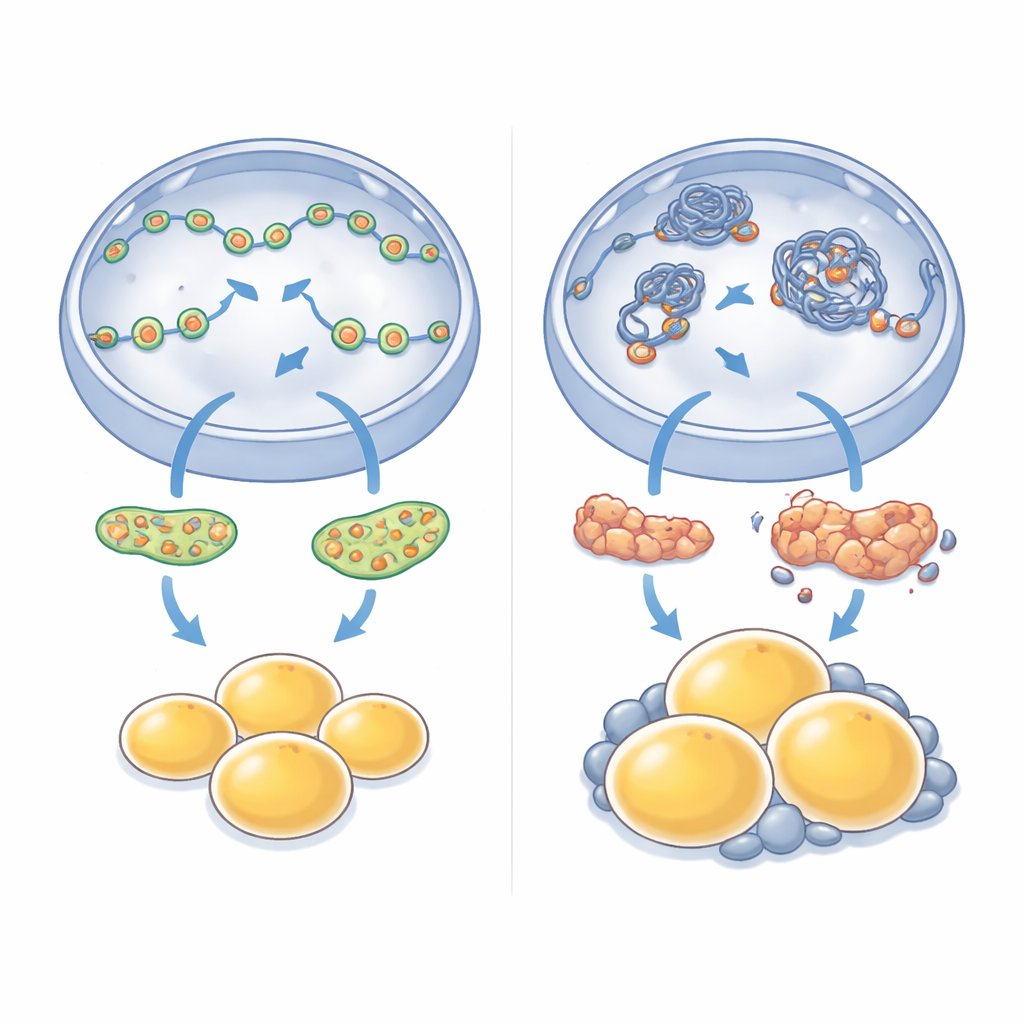
عندما تتحول التغيرات المحلية إلى زيادة وزن على مستوى الجسم
لم تقتصر عواقب فقدان هذا المحرك النووي المفرد على الخلايا في الأطباق الزجاجية. أصبحت الفئران الخالية من NM1 أثقل تدريجيًا من أشقائها الطبيعيين، على الرغم من أنها لم تتناول طعامًا أكثر. أظهرت الفحوصات وتحليلات الأنسجة تراكمًا واضحًا للدهون، خاصة حول الأعضاء الداخلية في البطن، وكانت الخلايا الدهنية الفردية في هذه الأماكن متضخمة بشكل لافت. عندما قاس الباحثون الجينات المرتفعة أو المنخفضة في هذه الدهون الحشوية، وجدوا تغييرات واسعة النطاق: أعيدت برمجة مسارات متعلقة باستخدام الطاقة، وإشارات الإنسولين، وإعادة تشكيل الأنسجة. غالبًا ما ارتفعت الجينات المرتبطة بنمو وتوسع الخلايا الدهنية، بينما كُبِحَت عدة عناصر تحكم مركزية في تكوين الخلايا الدهنية الصحية، مما عكس العيوب التي رُصدت في الخلايا الجذعية المزروعة.
الدهون الملتهبة ومحركات الطاقة المضطربة
إلى جانب الحجم الصافي، أظهر نسيج الدهون في الفئران ذات نقص NM1 علامات على الالتهاب والضغط الأيضي. سلط تحليل المسارات التفصيلي الضوء على تنشيط قوي لإشارات مناعية يقودها جزيئات مثل الإنترفيرون-غاما والعامل النخر الورمي، المعروفة بمساهمتها في مقاومة الإنسولين والمرض الأيضي. في الوقت نفسه، تم قمع المنسّقين الذين يدعمون نسيج دهني هادئ وفعّال من حيث الطاقة. ربطت الدراسة أيضًا فقدان NM1 باضطراب في الميتوكوندريا — محركات الطاقة في الخلية. جينات كانت عادةً تشرف على مراقبة جودة الميتوكوندريا والتحول بين إنتاج الطاقة الفعّال والاستقلاب اللاهوائي مُنظَّمة بشكل غير سليم، مما يوحي بأنه عند غياب NM1، تعتمد الخلايا الدهنية استراتيجية طاقة أقل كفاءة وأعرض للتوتر.
إشارات مشتركة بين الفئران والبشر
لسؤال ما إذا كان هذا المسار المحوري النووي قد يكون مهمًا عند البشر، فحص المؤلفون مجموعات بيانات جينية كبيرة من الدهون الحشوية البشرية. ركزوا على قريب بشري من NM1 يُدعى MYO1C ونظروا في شبكات المتغيرات التي تضبط نشاط الجينات المجاورة. وجدوا أن العديد من الموضوعات نفسها التي لوحظت في الفئران — التحكم الهيكلي الخلوي، الإشارات المناعية، والتنظيم الأيضي — ظهرت في شبكات الجينات البشرية المرتكزة على MYO1C. عدة جينات متغيرة في دهون الفئران الخالية من NM1 كانت أيضًا جزءًا من هذه الشبكات البشرية وارتبطت بإعادة تشكيل النسيج الدهني والتمثيل الغذائي. يشير هذا التداخل عبر الأنواع إلى أن آليات نووية مماثلة قد تؤثر على خطر السمنة لدى البشر.
ماذا يعني هذا للسمنة والصحة الأيضية
بالجمع بين النتائج، تُظهر الدراسة أن NM1 أكثر من مساعد نووي؛ إنه محور مركزي يربط تنظيم الحمض النووي بكيفية نمو الخلايا الدهنية وتخزينها للطاقة وتواصلها مع الجهاز المناعي. عند فقدان NM1، تُضبط مفاتيح الجينات في سوابق الخلايا الدهنية بشكل خاطئ، وتعمل الميتوكوندريا بشكل سيئ، وتكبر الخلايا الدهنية بدلًا من التكاثر، وتصبح الدهون الحشوية ملتهبة — مزيج يشبه النسيج الدهني غير الصحي المرصود في السمنة ومقاومة الإنسولين. للقراء غير المتخصصين، الرسالة أن الترتيب الفيزيائي للحمض النووي ومَن يساعده داخل النواة يمكن أن يميل بالأنسجة نحو توسع دهني صحي أو ضار. قد تصبح بروتينات مثل NM1 ونظيرها البشري MYO1C يومًا ما أهدافًا لعلاجات تسعى لإعادة تشكيل النسيج الدهني من الداخل إلى الخارج، مقدّمة طريقة أكثر دقة لمواجهة أمراض مرتبطة بالسمنة.
الاستشهاد: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
الكلمات المفتاحية: تكوين الخلايا الدهنية, الكروماتين, الميتوكوندريا, الدهون الحشوية, الالتهاب الأيضي