Clear Sky Science · ar
ثلاثي ميثلة الليسين 36 على هستون H3 بواسطة SETD2 يشكل مشهداً وراثياً حَدَثِيّاً في الخلايا الجذعية المعوية لتنظيم أيض الدهون وتخفيف شيخوخة الخلايا
لماذا تهم الخلايا الجذعية المعوية مع تقدمنا في العمر
في عمق بطانة أمعائنا تعمل خلايا جذعية صغيرة بلا انقطاع لتجديد النسيج الذي يساعدنا على هضم الطعام وامتصاص المغذيات. مع التقدم في العمر تتعب هذه الخلايا الجذعية، ما يجعل الأمعاء أكثر عرضة للأمراض وأبطأ في الشفاء. تستكشف هذه الدراسة كيف تساعد وسمات كيميائية دقيقة على بروتينات تغليف الحمض النووي في الحفاظ على شباب الخلايا الجذعية المعوية، وكيف يؤدي فقدانها إلى تعطيل حرق الدهون داخل الخلايا، وكيف قد تُبطئ أدوية مختارة هذا التدهور في المستقبل.
خلايا مسنة في بيئة متطلبة
السطح الداخلي للأمعاء هو أحد أسرع الأنسجة تجديدًا في الجسم. تنقسم الخلايا الجذعية الموجودة في قاع التجاويف الصغيرة المسماة الحفريات لاستبدال مليارات الخلايا كل بضعة أيام. يتطلب هذا العمل المستمر إمدادًا مستمرًا من الطاقة، يعتمد كثيرًا على تكسير الدهون. وفي الوقت نفسه، تُسيَّر هذه الخلايا الجذعية بواسطة رمز "فوق جيني"—علامات كيميائية على بروتينات الهستون تساعد في تحديد أي الجينات نشطة أو صامتة. ركز المؤلفون على إحدى هذه العلامات، المعروفة بثلاثي ميثلة H3K36، التي تضعها إنزيم يُدعى SETD2، وتساءلوا ما إذا كانت التغيرات في هذه العلامة قد تفسر فقدان الخلايا الجذعية المعوية لحيويتها مع التقدم بالعمر.
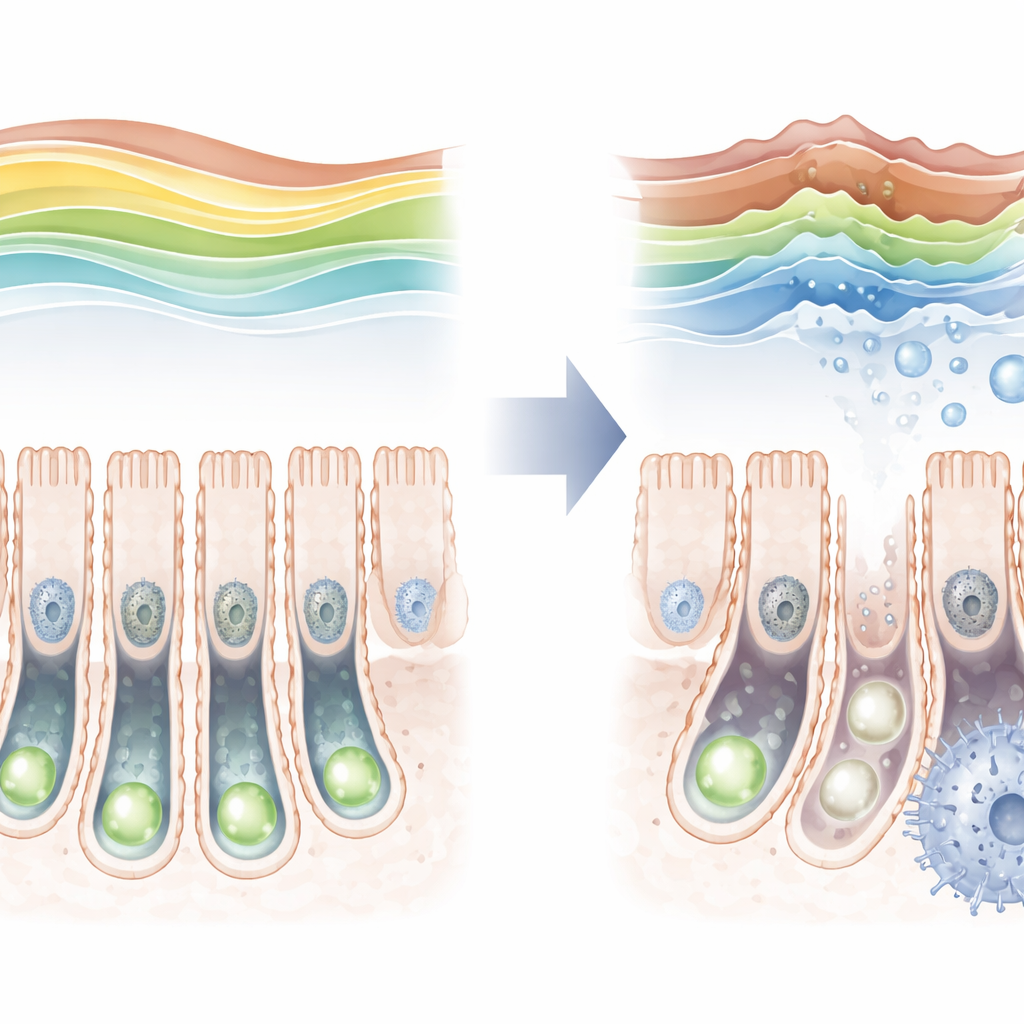
وسم وقائي يتلاشى مع العمر
من خلال فحص أمعاء الفئران على مدار العمر وجد الباحثون أن وسم ثلاثي ميثلة H3K36 ليس ثابتًا. يكون منخفضًا نسبيًا بعد الولادة مباشرة، ثم يرتفع إلى ذروته في البالغين الشباب قبل أن ينخفض مجددًا في الشيخوخة. ومع تراجع هذه العلامة في الحيوانات المسنة، ازدادت علامات الشيخوخة الخلوية في الخلايا الجذعية، مما يوحي بوجود صلة بينهما. لاختبار ذلك بشكل أكثر مباشرة، صنع الفريق فئرانًا يُستبعد فيها SETD2 فقط من الخلايا الجذعية المعوية. عند حذف هذا الإنزيم، تكاد تختفي العلامة الوقائية، انخفضت وتيرة انقسام الخلايا الجذعية، وواجهت صعوبة في إنتاج الطيف الكامل للأنواع الخلوية المتخصصة في الأمعاء.
كيف تؤدي التغيرات فوق الجينية إلى تعطيل حرق الدهون
أدى فقدان هذه العلامة المفردة للهستون إلى سلسلة من التغيرات داخل الخلايا الجذعية. أظهرت قياسات نشاط الجينات أن العديد من الجينات المرتبطة بدورة الخلية ونسخ الحمض النووي انخفض نشاطها، بينما ارتفع نشاط الجينات المرتبطة بالإجهاد والشيخوخة. لافت للنظر أن أقوى إشارة أشارت إلى اضطراب في معالجة الدهون: الجينات التي تدعم عادة أكسدة الأحماض الدهنية—الحرق المنظم للدهون للحصول على الطاقة—تراجعت، وبدأت الدهون تتراكم داخل الحفريات. أكدت تحليلات المستقلبات تراكم الأحماض الدهنية طويلة السلسلة، وهو دليل على تعطّل مسارات معالجة الدهون الاعتيادية. في الوقت نفسه تغيرت طريقة تعبئة الحمض النووي في النواة، حيث أصبحت مناطق كثيرة أكثر انكشافًا أو أكثر انغلاقًا، معيدة تشكيل نطاق الجينات التي يمكن للخلية استخدامها بسهولة.
معادِلات الكروماتين ومسيرة نحو الشيخوخة الخلوية
لفهم كيف تنشأ هذه التغيرات في تغليف الحمض النووي، خريطة المؤلفون كل من مناطق الكروماتين المفتوحة ومجموعة من علامات الهستون الأخرى على مستوى الجينوم. عند فقدان ثلاثي ميثلة H3K36 اكتسبت مساحات واسعة من الحمض النووي علامات "نشطة" وأصبحت أكثر وصولًا، لا سيما قرب الجينات المرتبطة بالأيض والشيخوخة. لاعب رئيسي في هذا الانتقال كان مركب إعادة تشكيل الكروماتين SWI/SNF المدفوع بواسطة وحدة أساسية تُدعى SMARCA4. في الخلايا الجذعية الخالية من SETD2 ارتفعت مستويات SMARCA4، وبدا أن المركب يساعد في فتح مناطق تُفعّل برامج الشيخوخة الخلوية. عندما خفّض الباحثون نشاط SMARCA4 وراثيًا أو بمثبط مستهدف، استعادت الخلايا الجذعية بعض قدرتها على تكوين أمعاءات صغيرة صحية في الأطباق، وانخفضت علامات الشيخوخة—مما يشير إلى أن إعادة التشكيل المفرطة تدفع هذه الخلايا نحو حالة متعبة وشيخوخة.
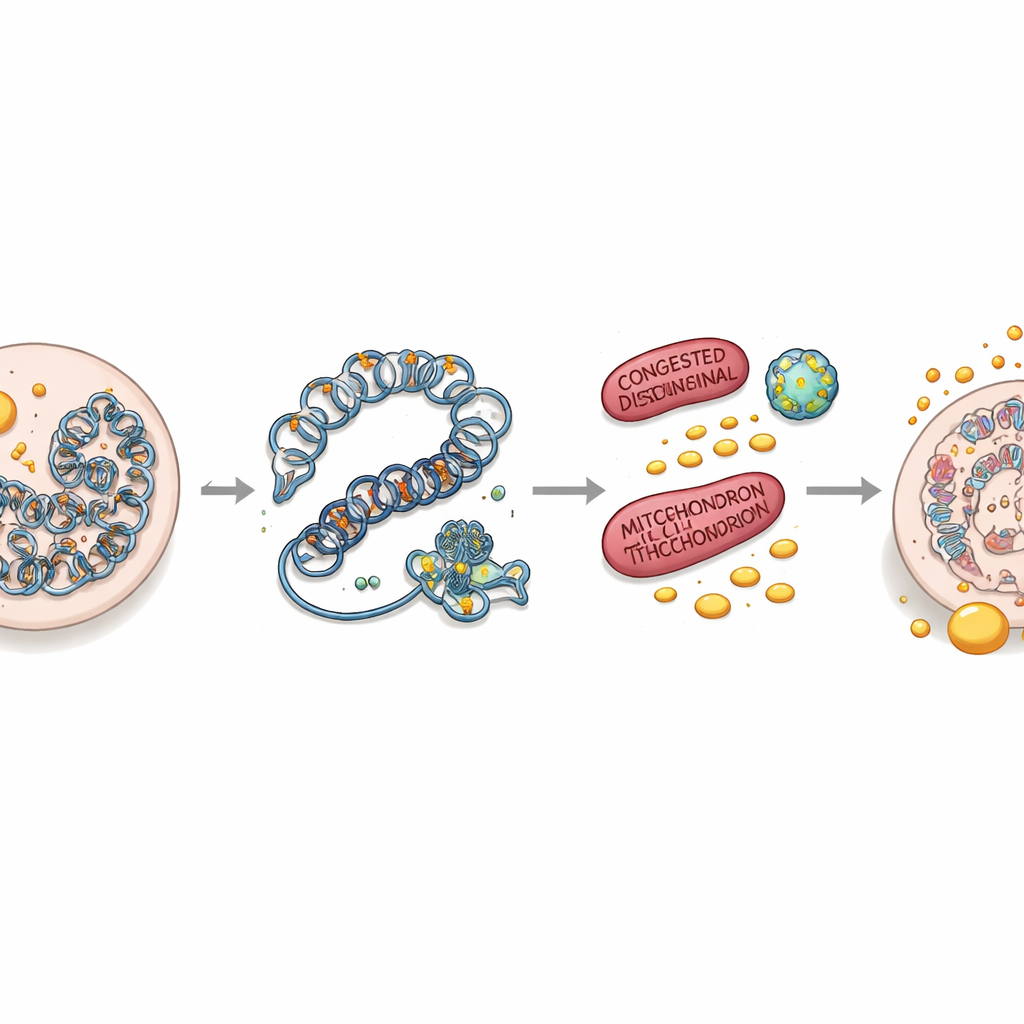
إعادة إيقاظ مسارات الطاقة لإنقاذ الخلايا الجذعية
بما أن تعطّل حرق الدهون برز كمشكلة مركزية، اختبر الفريق ما إذا كان تعزيز هذا المسار يمكن أن يعاكس شيخوخة الخلايا الجذعية. استخدموا دواءً ينشط PPARα، وهو منظم رئيسي لأكسدة الأحماض الدهنية. في الأعضاء المصغرة المزروعة من خلايا جذعية ناقصة SETD2 زاد هذا العلاج من النمو، أعاد الزوائد النموذجية للخلايا الجذعية النشيطة، وخفف تراكم الدهون. في الفئران الحية أدى نفس التدخل إلى تجديد جزئي للمخزون الخلوي الجذعي، خفض علامات الشيخوخة، وعاد تراكم الدهون في الحفريات إلى وضع أكثر طبيعية. تضع هذه النتائج أكسدة الأحماض الدهنية كحلقة وصل حاسمة بين التحكم فوق الجيني وصحة الخلايا الجذعية.
ما الذي يعنيه هذا للشيخوخة الصحية
مجملاً، تُظهر الدراسة أن علامة هستونية محددة يضعها SETD2 تساهم في الحفاظ على مشهد فوق جيني متوازن في الخلايا الجذعية المعوية. عندما تتلاشى هذه العلامة يُعاد تشكيل الكروماتين بشكل غير طبيعي، تتعطل مسارات حرق الدهون، تتراكم الليبيدات، وتنزلق الخلايا إلى حالة شيخوخة تقلل من قدرة الأمعاء على الإصلاح. سواء من خلال تخفيف ماكينة إعادة التشكيل المفرطة أو استعادة أيض الدهون بأدوية مستهدفة، قد يكون بالإمكان الحفاظ على وظيفة الخلايا الجذعية وصحة الأمعاء في المراحل المتقدمة من الحياة. وبينما تستند هذه النتائج إلى دراسات على الفئران، فإنها تتناغم مع أنماط لوحظت في اضطرابات الأمعاء لدى البشر، مما يثير احتمال أن علاجات أيضية مضبوطة بعناية قد تساعد يومًا ما في مكافحة التدهور المرتبط بالعمر في خلايانا الجذعية المعوية.
الاستشهاد: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
الكلمات المفتاحية: الخلايا الجذعية المعوية, الوراثة فوق الجينية, أكسدة الأحماض الدهنية, شيخوخة الخلوية, SETD2