Clear Sky Science · ar
حمض نووي ريبوزي مرتبط بـ Lamp2a تفرزه خلايا جذعية دهنية يمنع التغذية الراجعة بين لاكتلة ENO1–التحلل–التحلل السكري والسلوك الخبيث للخلايا في سرطان الثدي ثلاثي السلبية
لماذا يهم هذا المرضى
يُعد سرطان الثدي ثلاثي السلبية أحد أكثر أشكال سرطان الثدي عدوانية ولا يحتوي على مستقبلات الهرمونات أو عوامل النمو التي تجعل الأنواع الأخرى أكثر قابلية للعلاج. تكشف هذه الدراسة كيف تعيد هذه الأورام برمجة استهلاكها للطاقة للبقاء في بيئات منخفضة الأكسجين وتصف طريقة مبتكرة لمهاجمة هذه الشبكة الأيضية. للقارئ، توفر الدراسة لمحة عن كيفية أن فهم استقلاب السرطان يمكن أن يقود إلى علاجات جديدة ومحددة جداً تختلف جذرياً عن العلاج الكيميائي التقليدي.
كيف تغذي هذه الأورام نفسها
تعتمد العديد من السرطانات بشكل كبير على طريقة سريعة لكنها غير فعالة لإنتاج الطاقة تُسمى التحلل السكري، التي تحول السكر إلى ناتج جانبي هو اللاكتات. من خلال فحص عينات المرضى، وقواعد بيانات جينية عامة، وعدة خطوط خلايا لسرطان الثدي، يظهر الباحثون أن الأورام ثلاثية السلبية تميل إلى الاعتماد على التحلل السكري أكثر من أنواع سرطان الثدي الأخرى. إنزيم رئيسي في هذا المسار، ENO1، موجود بمستويات مرتفعة بشكل خاص في هذه الأورام ومرتبط بسوء البقاء. عندما تم خفض مستويات ENO1 في خلايا ثلاثية السلبية مُنموة مختبرياً، تحولّت الخلايا بعيداً عن التحلل السكري نحو إنتاج طاقة أكثر طبيعية في الميتوكوندريا، نما إيقاعها أبطأ، وكانت أقل قدرة على الغزو أو تكوين مستعمرات.
حلقة تغذية راجعة خطيرة داخل الخلايا السرطانية
عند التعمق أكثر، اكتشف الفريق أن اللاكتات بنفسها يقوّي ENO1 ويقفل الخلايا السرطانية في دائرة شريرة. يمكن للاكتات أن يغيّر البروتينات كيميائياً في عملية تُسمى اللاكتيلة. في الخلايا ثلاثية السلبية، زاد اللاكتات الإضافي من لاكتيلة ENO1، مما عزّز نشاط واستقرار الإنزيم، مسرّعاً بذلك التحلل السكري ومنتجاً مزيداً من اللاكتات. تحت ظروف منخفضة الأكسجين—التي تكون نموذجية للأورام الصلبة—تصاعدت قوة هذه الحلقة، مما ساعد الخلايا السرطانية على مقاومة موت الخلايا والاستمرار في التكاثر. إعاقة نشاط ENO1 بمثبّت جزيء صغير، أو تقليل إنتاج اللاكتات، أضعف هذه الحلقة، وكبح التحلل السكري، وبطأ نمو الورم في الفئران.
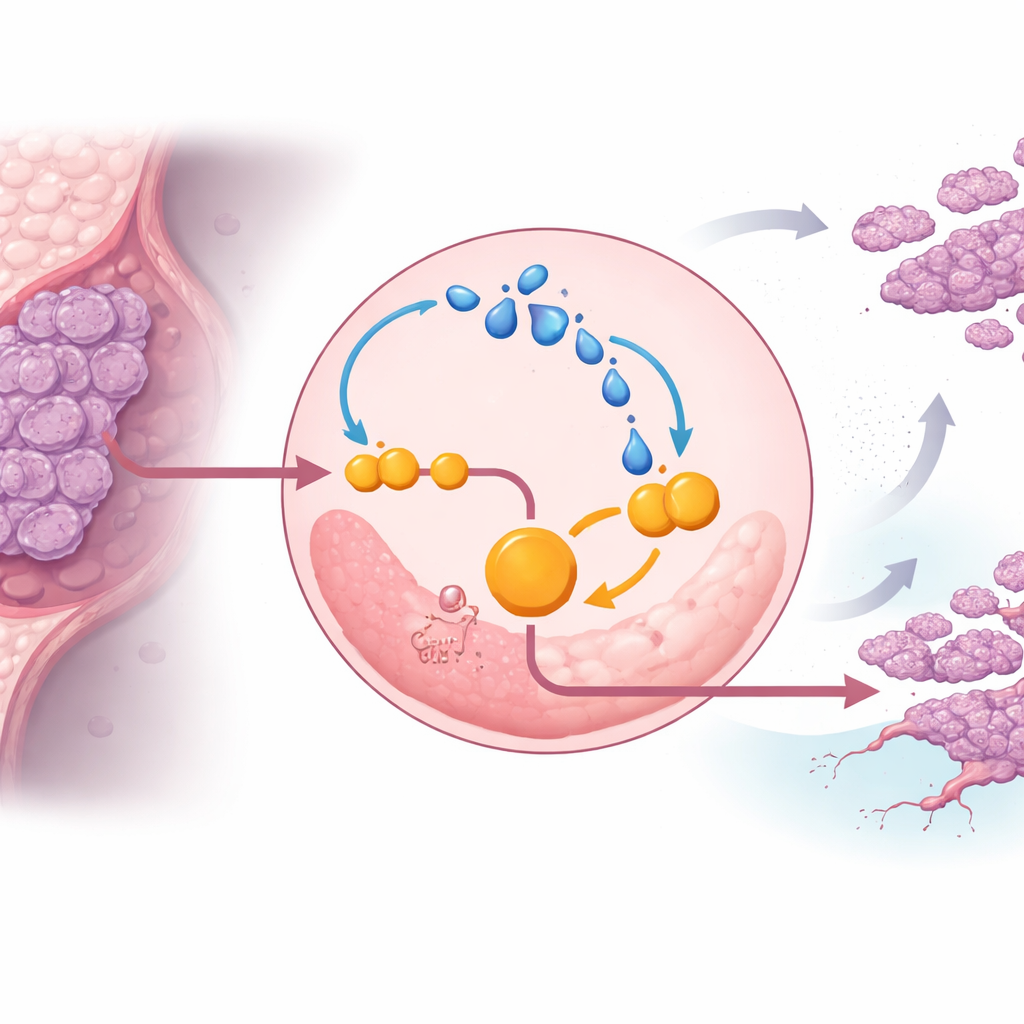
المفتاح الجزيئي الذي يحمي ENO1
حددت الدراسة نقطة تحكم محددة على ENO1 تجعل هذه الحلقة ممكنة. البروتين المعروف EP300 يضيف وسمات مبنية على اللاكتات إلى عدة مواقع في الليسين على ENO1، وكان أحد المواقع، المسمى K262، مهماً بشكل خاص. عندما طُوِّر هذا الموقع بحيث لا يمكن لاكتيلته، تم نقل ENO1 بسرعة إلى مراكز إعادة التدوير في الخلية، الليسوسومات، وتم تكسيره. من دون هذا الوسم الحامي، فقدت الخلايا ثلاثية السلبية جزءاً كبيراً من دافعها التحللي وقدرتها على تكوين أورام ونقائل في نماذج حيوانية. هذا يميّز لاكتيلة ENO1 عند K262 كمفتاح جزيئي يحمي الإنزيم من التحلل ويحافظ على استقلاب السرطان المعدّل.
طريقة جديدة لوصم ENO1 للتدمير
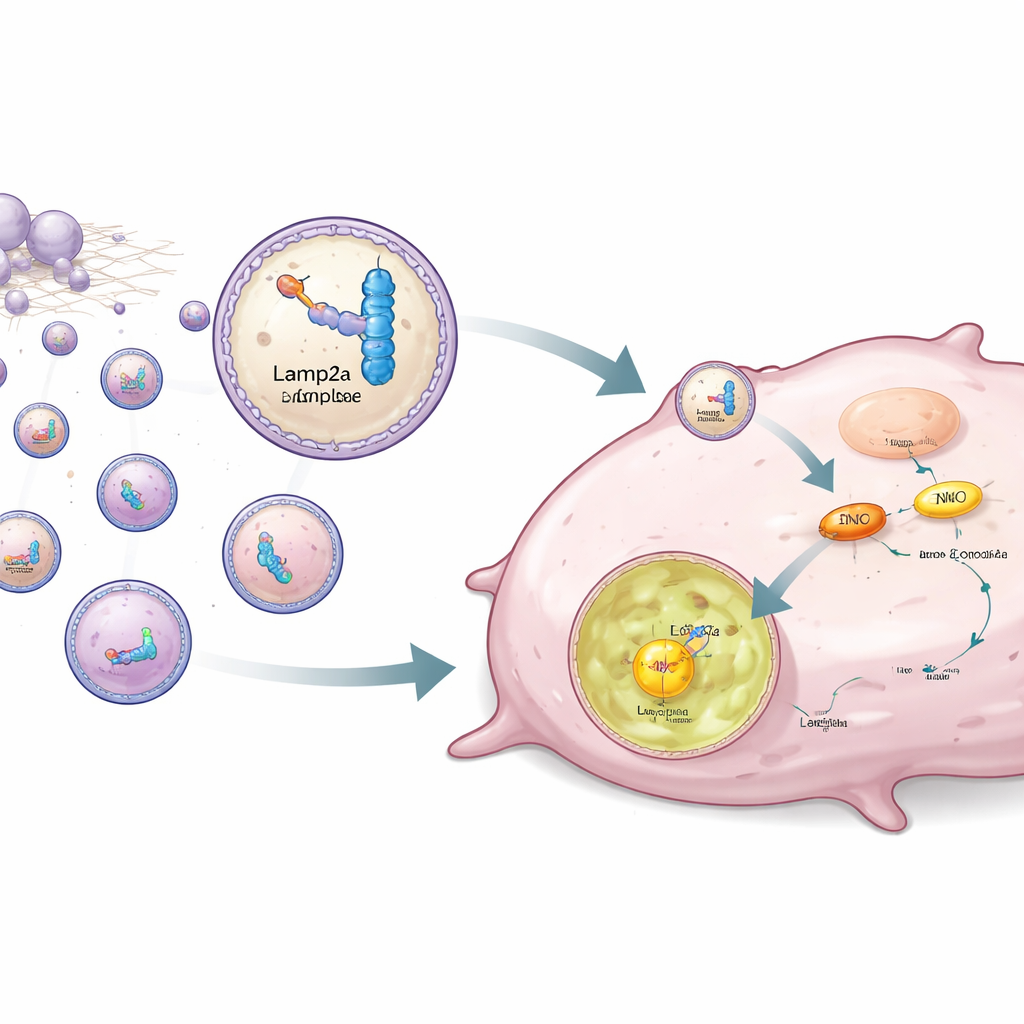
بدلاً من حجب ENO1 فقط، صمّم المؤلفون استراتيجية لإزالته بشكل انتقائي من الخلايا السرطانية. يعمل ENO1 أيضاً كبروتين رابط للحمض النووي الريبي، معرّفاً تسلسلات قصيرة محددة من الحمض النووي الريبي. قام الفريق بتصميم قطع حمض نووي ريبي تركيبية ترتبط بقوة بـ ENO1 ثم ربطوها بـ Lamp2a، وهو بروتين غشائي في الليسوسوم يشارك في تحلل البروتين المستهدف. تم تعديل خلايا جذعية بشرية مشتقة من الدهن وراثياً لإنتاج هذا الزوج من الحمض النووي الريبي–Lamp2a وتغليفه في حويصلات صغيرة تسمى الإكسوسومات. عندما أُضيفت هذه الإكسوسومات المهندسة إلى الخلايا ثلاثية السلبية، ارتبط الجزء الريبي بـ ENO1، في حين قاد جزء Lamp2a المجمع بأكمله إلى الليسوسومات، حيث تم تحلل ENO1 حتى لو كان يحمل وسم اللاكتيلة المستقر.
اختبار نهج التحلل الموجَّه في الحيوانات
للاقتراب بهذه الفكرة من علاج عملي، نما الباحثون الخلايا الجذعية المعدلة على سقالة قابلة للتحلل واغرسوا هذا البناء تحت جلد الفئران، قرب أورام ثلاثية السلبية. من هذا الموقع، أطلقت الخلايا الجذعية باستمرار إكسوسومات تحمل المجمعات المستهدفة لـ ENO1. أظهرت الأورام في هذه الفئران مستويات بروتين ENO1 أقل بكثير، وقلّ التحلل السكري، وعدد خلايا مقسمة أقل، ومزيد من علامات موت الخلايا مقارنةً بالحيوانات الضابطة. نمت الأورام بوتيرة أبطأ، وتراجع سلوكها الخبيث بوضوح، مما يبرهن أن توجيه ENO1 إلى الليسوسومات يمكن أن يجعل السرطان محروماً بفعالية من مسار الوقود المفضّل له.
ما الذي قد يعنيه هذا للعلاج المستقبلي
للجمهور غير المتخصص، الرسالة الأساسية هي أن هذا العمل يكشف عن ضعف وزاوية علاجية محتملة جديدة لسرطان الثدي ثلاثي السلبية. الضعف هو اعتماد الورم على حلقة طاقية معززة ذاتياً مبنية حول ENO1 واللاكتات، خصوصاً في المناطق منخفضة الأكسجين. زاوية العلاج هي نظام استهداف تحلل البروتين يستخدم حمضاً نووياً ريبياً مخصصاً وإكسوسومات مشتقة من خلايا جذعية لسحب ENO1 إلى آلية التخلص الخلوية. وعلى الرغم من أن التطبيق السريري لا يزال بعيداً، فإن هذا النهج يوضح كيف يمكن أن يُلهم الفهم العميق لخدع السرطان الأيضية علاجات دقيقة تهدف إلى تعطيل، بدلاً من تسميم، الخلايا الخبيثة.
الاستشهاد: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبية, استقلاب السرطان, إشارات اللاكتات, استهداف تحلل البروتين, إنزيم ENO1