Clear Sky Science · ar
الفوسفاتاز Shp1 ينظم استقرار بروتين CXCR2 والغزو المُتوسط بواسطة IL8 في سرطان الثدي
لماذا يهم هذا البحث لسرطان الثدي
لا يزال سرطان الثدي واحداً من الأسباب الرئيسة لوفيات النساء جراء السرطان، ويرجع ذلك إلى حد كبير إلى أن بعض الأورام تصبح غازية وتنتشر إلى أعضاء بعيدة. يكشف هذا العمل كيف يتواصل إشارة التهابية شائعة في الأورام تُسمى IL8 مع خلايا سرطان الثدي، وكيف يساعد «المكابح» الجزيئية المسماة Shp1 في حسم ما إذا كانت تلك الخلايا تبقى موضعية أم تصبح أكثر عدوانية. فهم هذه اللعبة الجزيئية قد يفتح سبلًا جديدة لإبطاء أو وقف انتشار أنواع سرطان الثدي صعبة العلاج، لا سيما المرض ثلاثي السلبي.
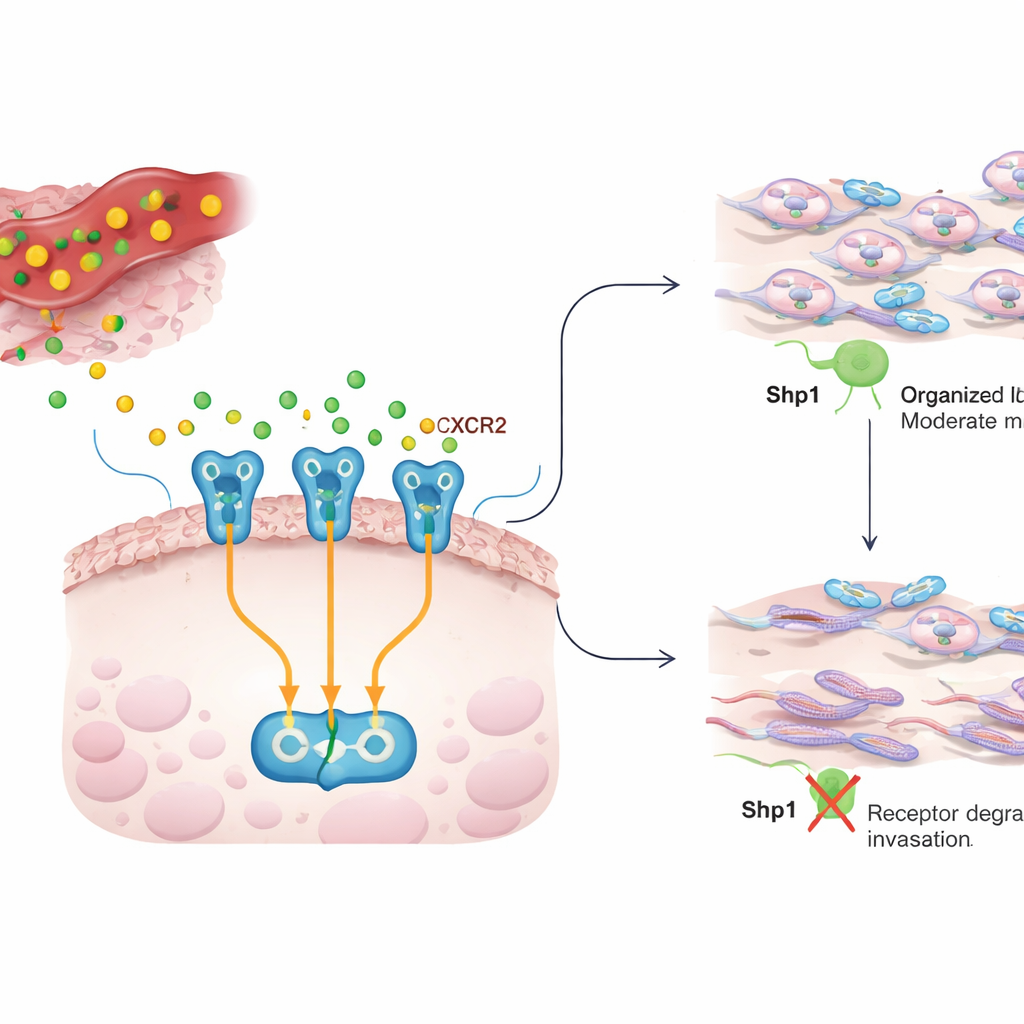
حوار بين الالتهاب وخلايا السرطان
داخل الورم، تحيط بالخلايا السرطانية خلايا مناعية وخلايا داعمة تطلق رسائل كيميائية تُسمى السيتوكينات. يعد IL8 أحد هذه الرسائل وغالباً ما توجد مستوياته مرتفعة في العديد من السرطانات، حيث يعزز النمو وتكوين الأوعية الدموية وقدرة الخلايا السرطانية على الحركة والغزو. يَنقل IL8 إشاراته عبر مستقبل على سطح الخلية يُدعى CXCR2. عندما يرتبط IL8 بـ CXCR2، يشغل عدة مسارات داخلية تعيد تنظيم هيكل الخلية، مما يساعد الخلايا على الزحف عبر الأنسجة والانتشار. يسأل العمل الحالي كيف يُحافظ على ضبط ذلك الحوار بين IL8 وCXCR2، وما إذا كان Shp1، وهو إنزيم يُنظر إليه عادةً كمكبح مكبح الأورام لإشارات النمو، يشكل أيضاً سلوك الغزو هذا.
الدور الخفي لـ Shp1 في حركة الخلايا
أولاً أزال الباحثون أو حجبوا Shp1 كيميائياً في خط خلايا سرطان ثدي لمعياري (MCF7) وقيَّموا قدرة الخلايا على التحرك والغزو عبر هلام يحاكي الأنسجة. من دون Shp1، أغلقت الخلايا السرطانية الجروح أسرع واندفعت عبر الهلام بكفاءة أعلى بمعدل مرتين إلى ثلاث مرات، ما يُظهر أن Shp1 يقيّد الحركة طبيعياً. باستخدام بيانات مرضى، وجدوا أيضاً أن النساء اللواتي عبرت أورامهن عن مستويات أقل من Shp1 كان لديهن بقاء أسوأ وزمن أقصر قبل الانتكاس. معاً، تشير هذه النتائج إلى أن Shp1 يحد من السلوك العدواني لخلايا سرطان الثدي وأن فقدان هذا المكبح مرتبط بنتائج أسوأ.
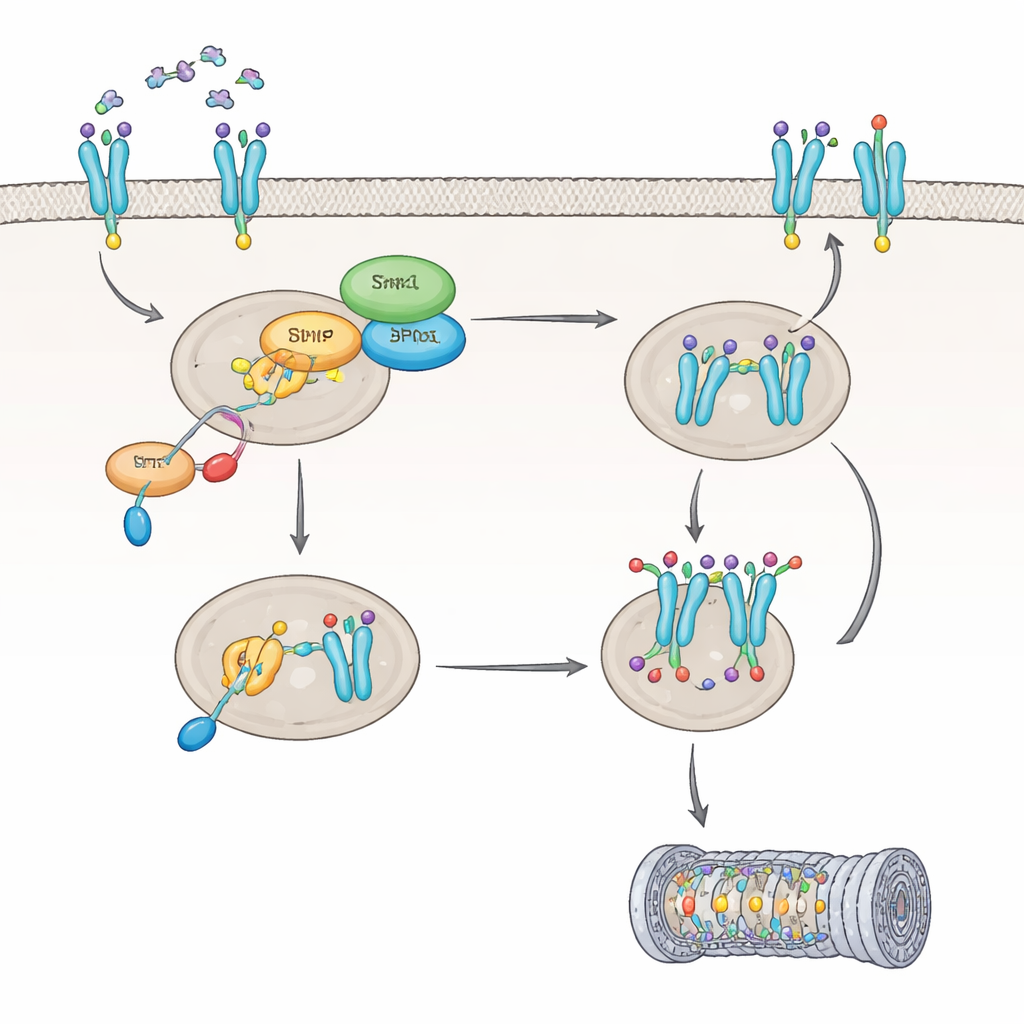
كيف يغيّر IL8 نشاط Shp1 ويعيد برمجة مستقبل رئيسي
بعد ذلك، درس الفريق كيف يؤثر IL8 على Shp1 نفسه. اكتشفوا أن IL8 يُنشط بروتيناً يُدعى PKC، الذي يعلّم Shp1 في موقع معين، مما يخفض نشاطه الإنزيمي بنحو 60 في المئة. عندما يُكبَّح Shp1 بهذه الطريقة، يصبح إنزيم آخر، PP2A، أقل نشاطاً، ويبقى مستقبل CXCR2 في حالة مُعدلة بشدة تغيّر مصيره داخل الخلية. بدلاً من أن يُنظف ويُعاد تدويره إلى سطح الخلية، يُوسَم CXCR2 للإنهاء، غالباً عبر آلية تكسير البروتين في الخلية، المسمّاة البروتيازوم. ثبت أن تعديلاً معيناً على CXCR2 في موقع حمض أميني اسمه Ser347 حاسم لإرفاق علامات التحلل هذه. في الخلايا التي تفتقد Shp1، كان CXCR2 أكثر وسمًا وتفتت بشكل أسرع، مما أدى إلى عدد أقل من المستقبلات على سطح الخلية واستجابة مخففة لـ IL8 بمرور الوقت.
أنواع سرطان الثدي المختلفة، توصيل عصبي مختلف
سرطان الثدي ليس مرضاً واحداً؛ تُصَنَّف الأورام إلى أنماط لومنال وHER2-إيجابي وثلاثي السلبي اعتماداً على نمط المستقبلات. اختبر الباحثون دائرة IL8–CXCR2–Shp1 في عدة خطوط خلوية تمثل كل نمط. في الخلايا اللمينال والثلاثية السلبية، شغّل IL8 سلسلة Shp1–PP2A–CXCR2، وكان حجب Shp1 يزيد الغزو الأساسي ويُلغي التأثير المعزز للغزو الذي يسببه IL8. في المقابل، استجابت الخلايا HER2-إيجابية لـ IL8، لكن حجب Shp1 لم يغير سلوكها كثيراً، مما يشير إلى أن Shp1 في هذه الأورام مرتبط بإشارات أخرى، مثل HER2، وأقل توفراً لتنظيم CXCR2. دعمت تحليلات التعبير الجيني واسعة النطاق هذه الصورة: تميل الخطوط الثلاثية السلبية إلى امتلاك مستويات Shp1 أقل وإشارات GPCR مُعدلة ومستويات أعلى من IL8، وهو ما يتوافق مع نمط أكثر عدوانية ومدفوعاً بالالتهاب.
ماذا يعني ذلك للعلاجات المستقبلية
لغير المتخصص، الرسالة الأساسية أن إنزيم Shp1 يعمل كمراقب مروري لمستقبل IL8، CXCR2، محدداً ما إذا كان المستقبل سيُعاد استخدامه أو يُدمَّر، وبالتالي مدى استجابة خلايا سرطان الثدي للإشارات الالتهابية. في سرطانات الثدي اللمينالية والثلاثية السلبية، يبدو أن هذه النقطة الضابطة مهمة بشكل خاص: عندما تكون مستويات Shp1 منخفضة أو يُحجب نشاطه، تصبح الخلايا أكثر غزوًا وتزداد سوء نتائج المرضى. وبما أنه يمكن تعزيز Shp1 أو تعديله بواسطة بعض الأدوية المتاحة حالياً، قد يوفر استهداف محور Shp1–CXCR2، ربما بالاشتراك مع مثبطات IL8 أو CXCR2، استراتيجية جديدة للحد من الغزو والانتقال النقيلي في أنواع سرطان الثدي العدوانية.
الاستشهاد: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
الكلمات المفتاحية: غزو سرطان الثدي, إشارة IL8, مستقبل CXCR2, الفوسفاتاز Shp1, سرطان الثدي ثلاثي السلبي