Clear Sky Science · ar
استهداف ضغوط النسخ في ورم الدماغ العصبي عن طريق استغلال القدرة التآزرية لمثبطات RRM2 وCHK1 من الجيل الثاني
إيقاف أورام الطفولة عند نقطة ضعفها
ورم الدماغ العصبي أحد أخطر سرطانات الأطفال، والعلاجات الحالية لا تزال تفشل مع عدد كبير من الأطفال. تَستكشف هذه الدراسة استراتيجية ذكية: بدلاً من مهاجمة الخلايا السرطانية بشكل عام، تستغل نقطة ضعف مدمجة في آلية نسخ الحمض النووي لدى هذه الخلايا. من خلال إقران نوعين جديدين من الأدوية اللذين يدفعان آلية التكرار في الخلايا السرطانية إلى ما وراء حدودها، يهدف الباحثون إلى قتل الأورام العدوانية بدقة أكبر مع تقليل الضرر على الأنسجة السليمة.
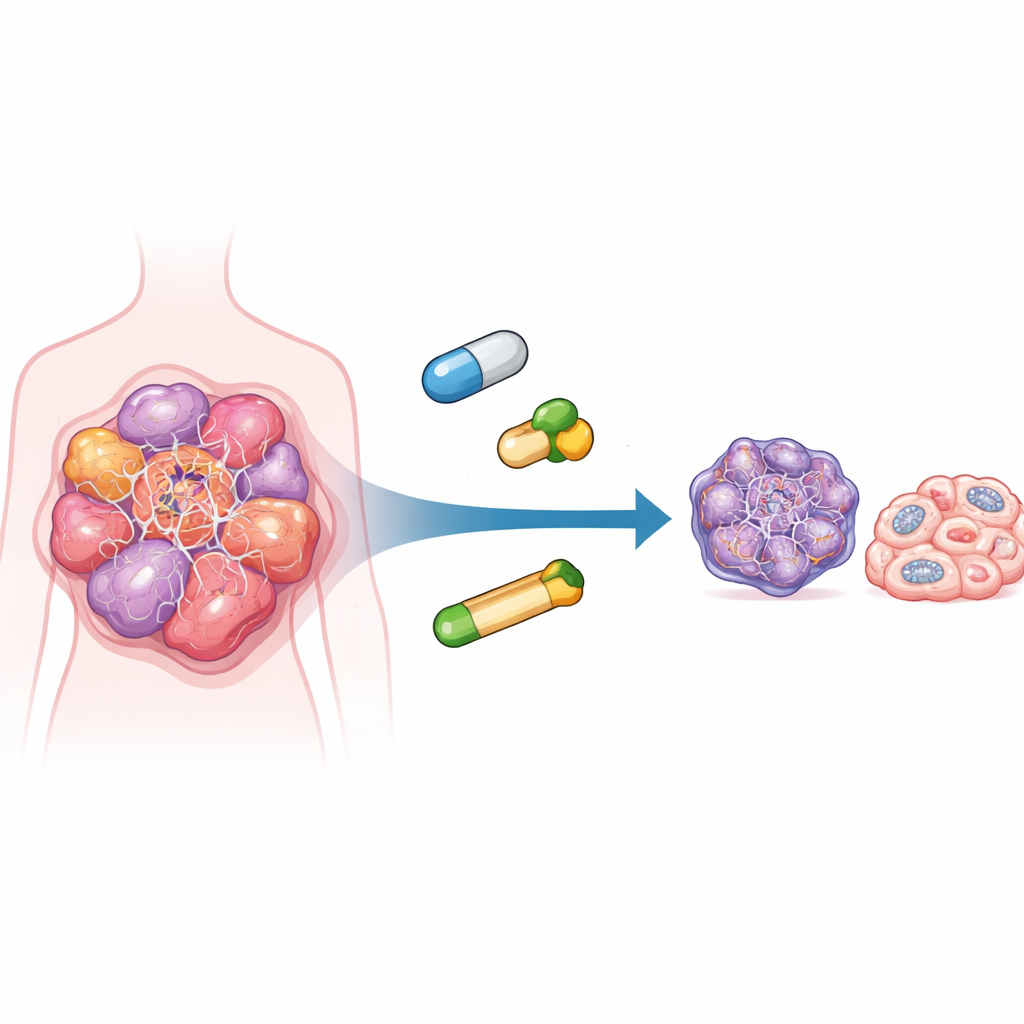
الخلايا السرطانية سريعة النمو تحت الضغط
تنمو الخلايا السرطانية وتنقسم بسرعة هائلة، ما يفرض ضغطاً كبيراً على عملية نسخ الحمض النووي. عندما يتباطأ هذا النسخ أو يتوقف، ينشأ ما يسميه العلماء ضغط التكرار. تعيش خلايا ورم الدماغ العصبي بالفعل بالقرب من هذه النقطة الحرجة، معتمدة بشكل كبير على أنظمة الإصلاح الطارئة للبقاء. أحد العوامل المساعدة الأساسية هو إنزيم يُدعى ريبونوكليوتيد ريدوكتاز، الذي يوفر اللبنات اللازمة لصنع حمض نووي جديد. مكوّن RRM2 فيه مهم بشكل خاص في الخلايا سريعة الانقسام، مما يجعله هدفاً جذاباً للعلاج المضاد للسرطان.
نوع جديد من الأدوية يستهدف لبنات الحمض النووي
أبقت الأدوية القديمة التي تتداخل مع RRM2، مثل الهيدروكسيوريا والترايابين، على أمل ولكنها سببت آثاراً جانبية خطيرة ومقاومة لدى المرضى. في هذا العمل، اختبر الفريق TAS1553، مركباً جديداً مصمماً خصيصاً لكسر الوصلة الفيزيائية بين نصفي إنزيم بناء الحمض النووي، RRM1 وRRM2. عند معالجة خلايا ورم الدماغ العصبي المزروعة في أطباق وفي "تومورويدات" ثلاثية الأبعاد، أبطأ TAS1553 النمو، وجوع الخلايا من لبنات بناء الحمض النووي، وأطلق إشارات واضحة لتضرر الحمض النووي والموت المبرمج للخلايا. والأهم أن الخلايا السليمة الضابطة تأثرت بدرجة أقل بكثير، مما يشير إلى نافذة علاجية يحتمل أن تكون فيها الخلايا الورمية أكثر عرضة من الأنسجة الطبيعية.
مجموعات العقارين تضرب الأورام بقوة أكبر
لأن الخلايا السرطانية غالباً ما تتكيف مع دواء واحد، ركز الباحثون على التركيبات. أقرنوا TAS1553 بأدوية تمنع CHK1، وهو بروتين يساعد الخلايا عادة على التوقف وإصلاح المشكلات أثناء تكرار الحمض النووي. باستخدام مثبطين مختلفين لـCHK1، بريكساسيرتيب والأكثر انتقائية SRA737، لاحظوا تآزرًا قويًا: معاً قللَت الأدوية نمو الخلايا الورمية أكثر بكثير من كل واحد بمفرده وعزَّزت بشكل حاد مؤشرات موت الخلايا. ظهر هذا التأثير ليس فقط في خطوط الخلايا القياسية، بل أيضاً في تومورويدات مشتقة من مرضى وفي نماذج ساركوما الأطفال، مما يوحي بأن النهج قد يكون مفيداً إلى ما وراء ورم الدماغ العصبي.
دليل أولي في زرد صغيرة حية
لاختبار ما إذا كان المزيج يعمل في كائن حي، زرع الفريق خلايا ورم دماغ عصبي بشرية في يرقات زرد صغيرة، مكونين أورام "أفاتار" يمكن مراقبتها تحت المجهر. أدى علاج هذه الأسماك بـTAS1553 مع أي من مثبطات CHK1، بجرعات لم تضر الحيوانات، إلى اندفاع من الخلايا السرطانية الميتة داخل الأورام المزروعة مقارنة بكل دواء على حدة. يقوّي هذا الدليل في الكائن الحي الفكرة القائلة إن الاستهداف المزدوج لبناء الحمض النووي وفحوص الأمان الخاصة به يمكن أن يدفع الخلايا الورمية التي تعاني بالفعل من الضغط إلى نقطة الانهيار مع إبقاء المضيف نسبياً دون أذى.
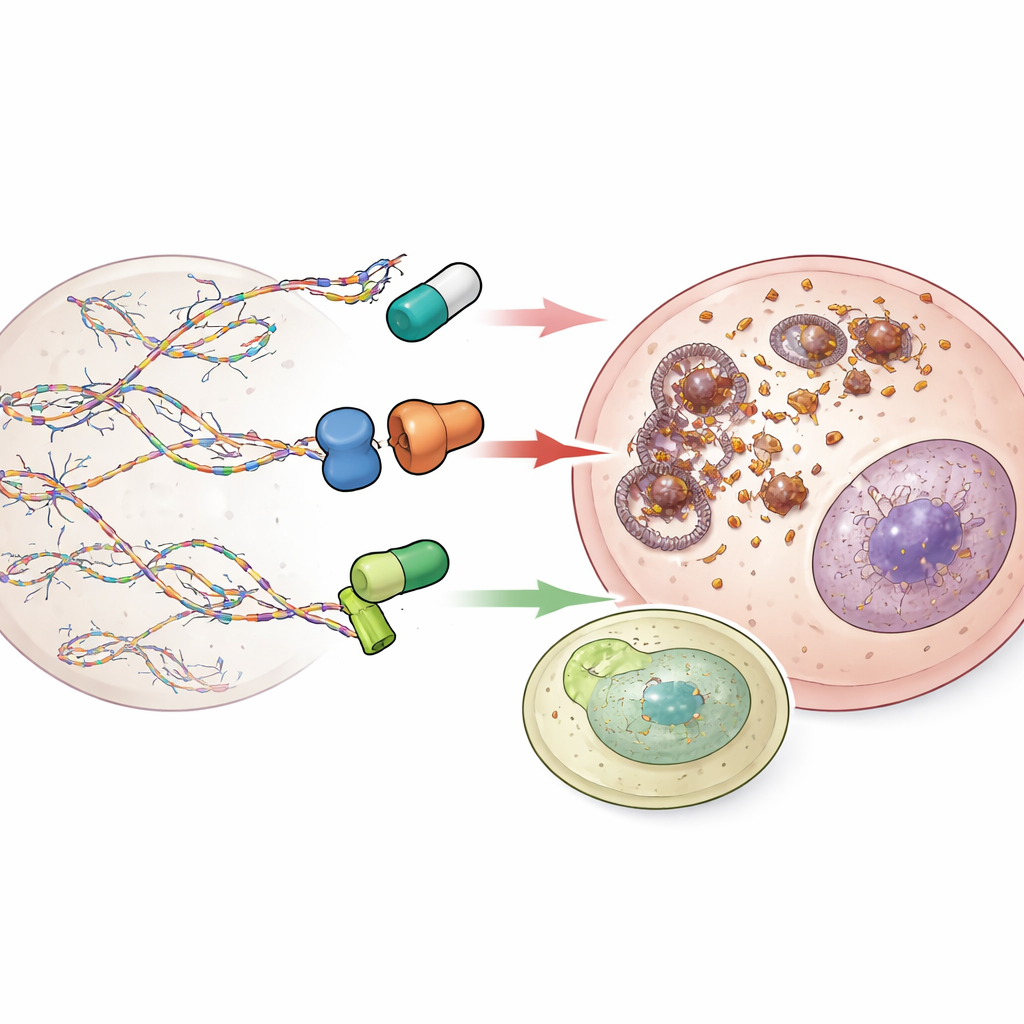
دلائل غير متوقعة في نشاط الجينات ومعالجة الحمض النووي الريبي
من خلال فحص الجينات التي أُنشطت أو كُبِحت بعد المعالجة، وجد الباحثون أن TAS1553 بمفرده وفي التركيبة فعّل مسارات موت الخلايا وضعّف البرامج التي يقودها MYC وMYCN، وهما جينان قويان محفزان للنمو وغالباً ما يرتفعان في السرطانات العدوانية. بشكل مفاجئ، خفّض TAS1553 أيضاً نشاط العديد من مكونات آلية قص الحمض النووي الريبي (السبلايسينغ)، التي تعدل الرسائل الجينية الأولية قبل استخدامها. وبما أن قصّ الحمض النووي الريبي المختل مرتبط بعدم استقرار الجينوم، فقد يضيف هذا الضغط الإضافي اختلالاً أكبر في الخلايا الورمية وقد يفتح الباب لتركيبات مستقبلية مع أدوية تستهدف آلة القص.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن ورم الدماغ العصبي والأورام الطفولية ذات الصلة يمكن مهاجمتها عن طريق قطع إمدادات بناء الحمض النووي وحجب مكابح الإصلاح الطارئ في آن واحد. يَدفع المُعطل الجديد لـRRM2، TAS1553، لا سيما عند الجمع معه بمثبطات CHK1 الحديثة مثل SRA737، الخلايا السرطانية إلى ما وراء قدرتها على التعامل مع ضغط التكرار، مما يؤدي إلى موت انتقائي للخلايا الورمية في نماذج المختبر والزرد. وبينما يلزم المزيد من العمل قبل أن تصل هذه التركيبات إلى الأطفال—لاسيما لتأكيد السلامة والفعالية في تجارب بشرية—توفر الأبحاث مساراً واعداً نحو علاجات أكثر ذكاءً واستهدافاً للأورام الطفولية عالية المخاطر.
الاستشهاد: Nelen, I.H., Leys, S., Bekaert, SL. et al. Targeting replication stress in neuroblastoma by exploiting the synergistic potential of second generation RRM2 and CHK1 inhibitors. Cell Death Dis 17, 263 (2026). https://doi.org/10.1038/s41419-026-08514-6
الكلمات المفتاحية: ورم الدماغ العصبي, ضغط تكرار الحمض النووي, العلاج التراكبي, مثبط CHK1, مثبط RRM2